
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Анализ процесса спиртового брожения и составление материальных соотношений
Титриметрический метод определения содержания этанола в бражке
Метод основан на окислении этанола в кислой среде бихроматом калия до уксусной кислоты. Количество избыточного бихромата калия, оставшегося после окисления спирта, определяют титриметрическим методом.
3С2Н5ОН + 2К2Сr2О7 + 8Н2SО4 → 3СН3СООН + 2Сr2(SО4)3 + 2К2SО4 + 11Н2О
К2Сr2О7 + 6КJ + 7Н2SО4 → 3J2 + Cr2(SO4)3 + 4K2SO4 + 7H2O
Избыток йода титруют тиосульфатом натрия:
J2 + Na2S2O3 → 2NaJ + Na2S4O6
Для отгонки этанола из бражки используют установку, изображенную на рисунке 13. В перегонную колбу отбирают 50 мл бражки. Жидкость в колбе 1 медленно нагревают до кипения и проводят отгонку водно-спиртовых паров в количестве 2/3 объема бражки. Пары конденсируются в холодильнике, и конденсат стекает в приемную колбу (предварительно нанести метку 30 мл на приемной колбе). По окончании перегонки выключают нагрев, затем охлаждающую воду, холодильник отсоединяют от перегонной колбы и промывают небольшими порциями дистиллированной воды в приемную колбу.
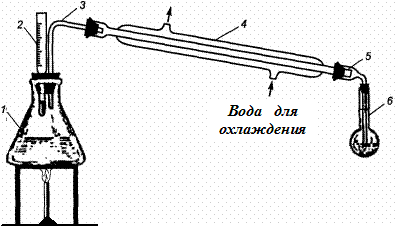
Рисунок 13 – Установка для отгонки этанола при атмосферном давлении:
1 – перегонная колба;
2 – термометр;
3 – отводная трубка;
4 – холодильник;
5 – алонж;
6 – приемная колба.
Содержимое приемной колбы количественно переносят в мерную колбу на 50 мл и доводят объем до метки 50 мл дистиллированной водой (это позволяет получить концентрацию спирта в водно-спиртовой смеси равную концентрации спирта в бражке). Далее производят разбавление: отбирают 2 мл в коническую колбу объемом 100 мл с предварительно нанесенной меткой 100 мл и доводят объем до метки дистиллированной водой.
Для анализа содержания этанола в бражке из конической колбы объемом 100 мл в колбу для опытного титрования отбирают 20 мл раствора, добавляют 20 мл 0,1 н раствора бихромата калия и 2 мл концентрированной серной кислоты. Спустя 5 минут в колбу добавляют 10 мл 10 % раствора йодида калия и 2-5 капель 1 % раствора крахмала (индикатор). Через 3-5 минут раствор титруют 0,1 н раствором тиосульфата натрия до изменения окраски раствора сине-коричневого цвета в зелено-голубой.
Параллельно ставят контрольную пробу для определения поправочного коэффициента k титра раствора тиосульфата натрия. Для этого к 20 мл 0,1 н раствора бихромата калия добавляют 2 мл концентрированной серной кислоты, 10 мл 10 % раствора йодида калия и 3-5 капель 1 % раствора крахмала (индикатор). Спустя 3-5 минут раствор титруют 0,1н раствором тиосульфата натрия как при опытном титровании, а затем рассчитывают поправочный коэффициент:
k = 20 / V3, (2.1)
где V3 – объем 0,1 н раствора Nа2S2О3, использованного на титрование контрольной пробы.
Концентрацию этанола (%, объем.) рассчитывают по формуле:
C = 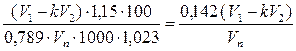 (2.2 )
(2.2 )
где V1 – объем 0,1 н раствора К2Сг2О7, мл;
V2 – объем 0,1 н раствора Nа2S2О3, мл;
k – поправочный коэффициент титра 0,1 н раствора Nа2S2О3;
1,15 – количество этанола, эквивалентное 1 мл 0,1 н раствора К2Сг2О7;
100 – коэффициент для пересчета в проценты;
1000 – коэффициент для пересчета мг в г;
0,789 – плотность этанола, г/мл;
1,023 – плотность бражки, г/мл;
Vп – объем анализируемой пробы, мл.
Количество этанола (в граммах), полученного из 100 мл бражки:
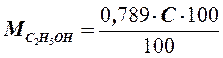
Количество СО2 (в граммах), полученного из 100 мл бражки:
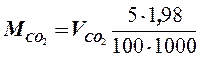 ,
,
где 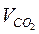 =объем этанола, полученного из 5 мл бражки (проба 1), мл;
=объем этанола, полученного из 5 мл бражки (проба 1), мл;
1,98 – плотность диоксида углерода, г/л;
1000 – коэффициент для пересчета мл в л.
Результаты расчетов заносят в таблицу 6.
Таблица 6 – Материальные соотношения процесса спиртового брожения
| Использован субстрат | Получены продукты | ||||
| Кол-во, г | Продукт | Кол-во, г | |||
| Крахмал | Углекислый газ | ||||
| Этанол |
Вопросы к коллоквиуму
по теме «Общая характеристика процессов ферментации. Спиртовое брожение как пример анаэробной ферментации»
1. Основные понятия о культивировании микроорганизмов: ферментация, биосинтез, биотрансформация, биоконверсия и др.
2. Анализ количества биомассы в процессе культивирования.
3. Глубинная ферментация.
4. Поверхностная, твердофазная и газофазная ферментация.
5. Продуценты этанола. Их характеристика.
6. Стадии и этапы спиртового брожения.
7. Энергетика спиртового брожения. Прирост биомассы в процессах брожения и аэробного биосинтеза дрожжевой биомассы.
8. Кривая брожения. Характеристика периодов спиртового брожения.
9. Промышленная реализация спиртового брожения.
10. Материльные соотношения процесса спиртового брожения.
Date: 2015-09-24; view: 1012; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |