
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Выполнение типового расчета и исследовательской задачи
Контрольно-курсовая работа по дисциплине «Транспортная экология» посвящена расчету термодинамических параметров рабочего цикла и характеристики токсичности бензинового двигателя внутреннего сгорания (ДВС) заданной марки. В процессе выполнения работы необходимо изучить следующий учебный материал: 1) физико-химические условия образования токсичных веществ в камере сгорания ДВС [6, с.42-49];
2) равновесие термодинамических систем с фазовыми и химическими превращениями [2, с.156-168; раздел «Краткая теоретическая часть»];
3) описание математических моделей ДВС [5, с.133-144]; 4) пример расчета характеристики токсичности бензинового ДВС [2, с.457-460].
Представим себе систему, находящуюся в состоянии механического и термического равновесия с окружающей средой, но с заторможенными внутренними степенями свободы. Это может быть, например, смесь горючих газов, не вступивших по каким-либо причинам в химическую реакцию. После снятия «торможения», т.е. в результате горения, установится новое состояние, существенно отличающееся от предыдущего. Во-первых, изменится состав вещества системы – вместо исходных газов образуются продукты сгорания. Во-вторых, выделение теплоты в результате горения послужит причиной изменения как температуры системы, так и её давления, объёма и др. параметров состояния.
В качестве объекта будем рассматривать материальные среды, состоящие из одной или нескольких фаз. Каждая фаза – это часть системы, имеющая чётко выраженные границы. Однофазные системы принято называть гомогенными, а многофазовые – гетерогенными. В зависимости от агрегатного состояния различают газообразные и конденсированные фазы. Каждая из них состоит из отдельных компонентов. Считается, что компонентами фаз являются индивидуальные вещества – химические соединения, находящиеся в газообразном либо конденсированном состоянии, имеющие кратное число образующих их атомов и характеризуемые определённой степенью (кратностью) ионизации.
Примером однофазной многокомпонентной среды может служить окружающий нас воздух, состоящий из азота N2, кислорода О2, углекислого газа СО2, и водяных паров Н2О. Эти молекулярные газы и являются компонентами системы. С повышением температуры в воздухе начинаются реакции диссоциации и ионизации, т.е. разрыв химических связей, приводящий к образованию радикалов, свободных атомов и ионов. Тогда в число компонентов воздуха добавляются такие индивидуальные вещества, как N, О, СО, ОН, N+, О+, NO и т.п.
Фазовые границы разделяют систему на отдельные подсистемы, но не запрещают возможности перехода химических элементов из одной фазы в другую. Более того, задача термодинамического анализа любой гетерогенной системы и заключается в том, чтобы определить, какие фазы образуются в равновесии и чему равно содержание компонентов в каждой из них. Обязательным при этом является только соблюдение условия материальной изолированности системы в целом от окружающей среды.
Для нахождения равновесных концентраций решается следующая система нелинейных уравнений:
 (i = 1, 2, …, k); (1)
(i = 1, 2, …, k); (1)
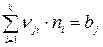 (j = 1, 2, …, m); (2)
(j = 1, 2, …, m); (2)
 (3)
(3)
где ni – молярное содержание компонентов равновесия, моль/кг;
lj – неопределённые множители Лагранжа;
p, T, u – давление, температура и удельный объём системы;
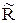 = 8,3144 Дж/(мольЧК);
= 8,3144 Дж/(мольЧК);
nji – число атомов j -го элемента в i -ом компоненте;
bj – молярное содержание j -го элемента в системе.
Термодинамические свойства каждого индивидуального вещества  – справочная величина, для вычисления которой используются значения приведённой энергии Гиббса (Фio) и теплоты образования DН¦о(0).
– справочная величина, для вычисления которой используются значения приведённой энергии Гиббса (Фio) и теплоты образования DН¦о(0).
 (4)
(4)
Система в которую вошли (1), (2), (3) уравнения получена дифференцированием функции Лагранжа:
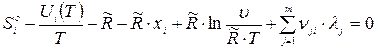 (i = 1, 2, …, k); (5)
(i = 1, 2, …, k); (5)
 (r = 1, 2, …, R); (6)
(r = 1, 2, …, R); (6)
 (j = 1, 2, …, m); (7)
(j = 1, 2, …, m); (7)
 ; (8)
; (8)
 . (9)
. (9)
Входящие в уравнения (5) и (6) комплексы свойств индивидуальных веществ 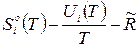 и
и  известны как полная и приведённая энергия Гиббса:
известны как полная и приведённая энергия Гиббса:

 ,
,
где 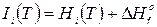 и
и 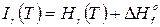 – полные энтальпии веществ.
– полные энтальпии веществ.
Полученная совокупность алгебраических соотношений связывает между собой равновесные значения количеств веществ всех компонентов ni (i = 1, 2, …, k), nr (r = 1, 2, …, R), термодинамических параметров p, T, u, u и неопределённых множителей Лагранжа lj (j = 1, 2, …, m). Общее число неизвестных, входящих в систему уравнений (5) – (9), равно, таким образом, k + R + m + 4.
Однако число уравнений оказалось на два меньше, чем число неизвестных. Это вызывает необходимость наложения ещё двух связей на соотношения между параметрами равновесия рассматриваемой системы. В простейшем случае ими могут быть заданные значения двух термодинамических параметров, таких, например, как давление и температура (p и T).
Это согласуется с известным положением термодинамики нереагирующих сред, согласно которому достаточно задать два параметра состояния, чтобы однозначно найти остальные свойства (параметры) системы.
Date: 2015-08-15; view: 206; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |