
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Ретроградный солидус
Рассмотрим случай максимальной растворимости выше температуры трехфазного равновесия, получивший название ретроградного солидуса.
Вид участка фазовой диаграммы с ретроградным солидусом при трехфазном эвтектическом равновесии показан на рис.6.
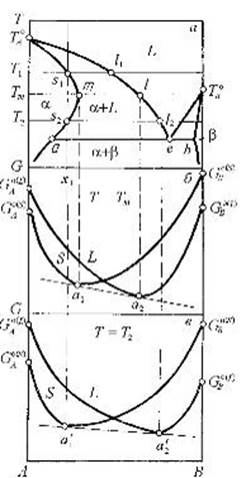
Рис.6. Ретроградный солидус в системе эвтектического типа (а) иотносительное расположение кривых концентрационной зависимости изобарно-изотермического потенциала твердой и жидкой фаз при различных температурах (б, в)
Как видим, максимальная протяженность области твердого раствора на основе компонента А, отмеченная на кривой солидуса буквой m, отвечает температуре Тm, которая выше температуры трехфазного эвтектического равновесия. Необычность представленной картины заключается в том, что если рассматривать процесс охлаждения из жидкости, например, сплава состава х 1, то оказывается, что после полного затвердевания жидкости состава l 1 при температуре T 1 в точке s 1 он в процессе дальнейшего охлаждения плавится при более низкой температуре в точке s 2 с выделением жидкости состава l 2, сопряженной с s 2 при температуре Т 2.
С позиций геометрической термодинамики принципиальная возможность существования ретроградного солидуса никаких возражений не вызывает. На рис.6, б и в показано положение кривых концентрационной зависимости изобарно-изотермического потенциала твердой и жидкой фаз при температурах Тm и Т 2 (причем Тт > Т 2 > Те).
Как видим, положение фигуративных точек равновесных фаз на диаграмме Τ – x фиксируется однозначно путем проведения общих касательных a 1 a 2 и а′ 1 а' 2 к кривым G = f (xB) фаз, находящихся в равновесии при каждой температуре. Понижение температуры от Тm до Т 2 лишь смещает соответствующие кривые в область более высоких значений изобарно-изотермического потенциала в связи с общим ходом его температурной зависимости и увеличивает интервал концентраций между точками касания к кривым Gα = f (xB) и GL = f (xB). Однако видимых причин смещения кривых изобарно-изотермического потенциала вдоль оси концентраций на основании только геометрической термодинамики указать нельзя. Следует отметить, что ретроградный характер солидуса возможен не только при эвтектическом, но и при других возможных трехфазных равновесиях в двухкомпонентной системе, так как характер трехфазного равновесия в принципе не связан с сущностью рассматриваемого явления. Важно только, чтобы область двухфазного равновесия между твердым и жидким растворами была нисходящей.
Используемая литература
В докладе использовалась информация из книги Калин «Физическое материаловедение Том 2 Основы материаловедения» 2007, а так же материалы с сайта www.studfiles.ru
Date: 2015-07-10; view: 2127; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |