
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Особенности взаимодействия фенолов с альдегидами. Отверждение и строение фенолоальдегидных смол
Взаимодействие фенолов с альдегидами представляет собой реакцию поликонденсации. На образование смол и их свойства влияют: 1) химическое строение исходных продуктов; 2) мольное соотношение фенола и альдегида; 3) кислотность реакционной среды.
Химическое строение исходных продуктов. Фенолы и альдегиды в зависимости от химического строения обладают разной функциональностью и реакционной способностью.
Гидроксильная группа в бензольном ядре фенолов способствует большей подвижности атомов водорода, находящихся в орто- и пара-положениях к гидроксильной группе. Атомы водорода в метаположении практически не вступают в химические реакции при получении ФФС. Таким образом, благодаря наличию трех подвижных атомов водорода фенолы являются очень реакционно-способными трифункциональными соединениями:

По реакционноспособным центрам в молекулах фенолов происходит присоединение альдегидов и образование фенолоформальдегидных смол (олигомеров), способных в определенных условиях либо превращаться в неплавкое и нерастворимое состояние (термореактивные смолы), либо оставаться плавкими и растворимыми (термопластичные смолы). Термореактивпые смолы получают на основе трифункциональных фенолов, термопластичные смолы могут быть получены из сырья, содержащего дифункциональные фенолы: о- и п-крезолы; 2,3-, 2,5- и 3,4-ксиленолы.
Из альдегидов только формальдегид и фурфурол способны образовывать неплавкие и нерастворимые смолы с трифункциональными фенолами. Другие альдегиды (уксусный, масляный и т. п.) непригодны для получения термореактивных смол из-за пониженной активности и пространственных затруднений протекания реакции.
Процесс поликонденсации фенолов с альдегидами проходит как в кислой, так и в щелочной средах с образованием разных по строению продуктов.
Наиболее распространенными являются ФФС, полученные из фенола и формальдегида. Условия их образования и отверждения (превращения в неплавкое и нерастворимое состояние) определяются двумя основными факторами: мольным соотношением исходных компонентов и кислотностью реакционной среды.
Мольное соотношение фенол: формальдегид. Этим фактором в первую очередь определяется строение начальных продуктов реакции конденсации. Так, при соотношении фенол: формальдегид = 1:1 в начале реакции образуются главным образом о- и п-моногидроксибензиловые спирты, преимущественно о-гидроксибензиловый спирт (салигенин):
 |
Моногидроксибензиловые спирты, имеющие одну метилольную группу, способны вступать во взаимодействие между собой и с фенолом. В первом случае образуются термопластичные смолы линейного строения, а во втором — изомерные дигидроксидифенилметаны:
При мольном соотношении формальдегид: фенол = 2:1 и выше вначале образуются многоатомные метилолфенолы (фенолоспирты), из которых при дальнейшем нагревании получаются неплавкие и нерастворимые смолы:
 |
Кислотность среды. Этот фактор оказывает существенное влияние на ход процесса. В кислой среде (рН < 7) образующиеся из фенола и формальдегида фенолоспирты неустойчивы и быстро конденсируются друг с другом или с фенолом (особенно при нагревании), образуя термопластичные смолы. В щелочной среде (рН > 7) фенолоспирты устойчивы, дальнейшая их конденсация происходит лишь при нагревании или при добавлении кислых катализаторов.
При различных соотношениях фенола и формальдегида в щелочной среде образуются только термореактивные смолы, причем в случае недостатка альдегида часть фенола остается растворенной в смоле (в виде так называемого «свободного фенола»),
Новолачные смолы (НС) получают конденсацией формальдегида как с три- так и с дифункциональными фенолами в присутствии кислого катализатора. Трифункциональиые фенолы необходимо брать в избытке: мольное соотношение фенол: формальдегид составляет 6:5 или 7:6. Уменьшение избытка фенола приводит к образованию резольной смолы даже в кислой среде, а увеличение его снижает молекулярную массу смолы.
Образование НС протекает через дигидроксидифенилметаны, из которых при дальнейшей реакции с формальдегидом и фенолом получается смола:

Смолы состоят из разветвленных молекул различной длины, получаемых конденсацией в орто- и пара-положениях к гидроксилу фенольного ядра.
При фракционировании смолы обнаруживается большой разброс молекулярных масс отдельных фракций. Например, из смолы со средней молекулярной массой 640 можно получить ряд фракций с молекулярной массой 200-8000. В НС фенольные ядра связаны метиленовыми мостиками. Гидроксильные группы не участвуют в реакции образования смолы, а эфирные связи почти отсутствуют.
Образование НС может быть представлено следующим образом:

При поликонденсации фенола с формальдегидом (например, в отношении 1:0,5) в присутствии солей двухвалентных металлов (Mn, Cd, РЬ, Zn и др.) при рН 4-7 образуются НС линейного строения (ортоноволаки), в которых до 80% фенольных ядер связаны метиленовыми мостиками в орто-ортоположении.
Ортоноволаки также образуются при нагревании до температуры кипения смеси фенола с параформом. Все они отличаются от обычных НС повышенной скоростью отверждения при добавлении уротропина (в 4-5 раз) и используются для изготовления быстропрессующихся пресс-материалов.
На основе некоторых алкилированных фенолов, например п-третбутилфенола, также получаются НС линейного строения:
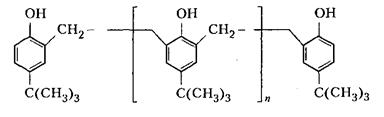
В зависимости от условий получения НС различаются по фракционному составу, размеру молекул и их разветвленности, а следовательно, но температуре плавления, содержанию свободного фенола, растворимости и вязкости растворов. Цвет смолы зависит от чистоты сырья и от применяемого катализатора. Минеральные кислоты (соляная и серная) вызывают потемнение смол, тогда как при использовании органических кислот (щавелевая) получаются светлые продукты.
Наличие свободных реактивных центров в НС (в орто- и пара-положении к гидроксилу фенольного ядра) определяет способность этих смол переходить в неплавкое и нерастворимое состояние при обработке формальдегидом или гексаметилентетрамином (ГМТА). Следы воды, содержащиеся в новолачных смолах разлагают ГМТА до образования аммиака и формальдегида, а также вызывают гидролиз ГМТА с образованием аминометилольных соединений NH(CH2OH)2 и N(CH2OH)3. Взаимодействуя с фенольными ядрами аминометилольные соединения образуют вторичные и третичные бензиламины.
На первой стадии отверждения НС образуются промежуточные продукты, содержащие диметилениминовые мостики -СН2-NH-СН2-. Установлено, что НС, содержащая свободный фенол, реагирует с ГМТА таким образом, что сначала из свободного фенола и гексаметилентетрамина образуются производные дибензиламина и аммиак, а затем уже смола взаимодействует с производными дибензиламина с выделением аммиака и сшитых продуктов. Наличие свободного фенола в смоле, таким образом, облегчает ее сшивание. Термически отвержденные смолы содержат до 6 % химически связанного азота, в том числе в форме азометиновых групп (-CH=N-), которые ответственны за желтый цвет продуктов реакции.
Строение отвержденных НС может быть представлено следующим образом:

Резольные смолы (PC) получают при конденсации фенола с избытком формальдегида в присутствии оснований. Обычно при мольном отношении фенол: формальдегид = 6:7 на 1 моль прореагировавшего фенола приходтся до 1,5 моль формальдегида. Образуются моно-, ди- и триметилолфенолы и часть фенола остается непрореагировавшей. На количество присоединенного формальдегида большое влияние оказывает катализатор: в присутствии сильных оснований (NaOH, КОН) в реакцию вступает больше формальдегида, чем в присутствии аммиака.

При низких температурах (20-70°С) в щелочной среде образовавшиеся фенолоспирты не вступают в дальнейшую реакцию конденсации, но при температурах выше 70°С фенолоспирты взаимодействуют друг с другом по схеме:
Резольная смола — смесь линейных и разветвленных олигомеров с молекулярной массой от 400 до 1000. Общая формула PC:

В PC, полученной в присутствии едкого натра или едкого кали, имеется некоторое количество простых эфирных связей -СН2-О-СН2- и при нагревании ее выделяется формальдегид.
В случае применения аммиака простые эфирные связи не возникают и при нагревании смолы до 200°С формальдегид не выделяется. Нагревание способствует постепенному переходу PC сначала в резитол, а затем в резит.
Стадия А (резол) — смола жидкая (содержит воду) или твердая (не содержит воды), растворяется в спирте, ацетоне и водных растворах щелочей; при нагревании переходит в неплавкое и нерастворимое состояние.
Стадия В (резитол) — смола твердая и хрупкая на холоду, но эластичная, способная растягиваться в длинные нити при 120-125°С; лишь частично растворяется в спирте и ацетоне. Это свидетельствует о низкой концентрации поперечных связей. При 135°С образуется больше поперечных связей. При длительном нагревании резитол переходит в неплавкое и нерастворимое состояние. При 170 °С образуется продукт с высокой концентрацией поперечных связей в виде метиленовых мостиков. Все ранее возникшие эфирные связи -СН2-О-СН2- разрушаются и также переходят в метиленовые мостики.
Стадия С (резит) — смола представляет собой твердый и хрупкий, неплавкий и нерастворимый продукт. Низкомолекулярные, растворимые фракции в ней отсутствуют или имеются в относительно небольших количествах. Строение резита можно представить следующим образом:
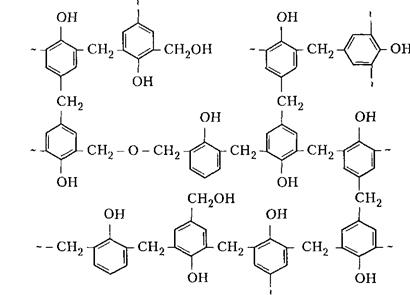
В отвержденной резольной смоле остается часть свободных метилольных групп, которые при дополнительном нагревании при высокой температуре реагируют друг с другом.
Отверждение — поликонденсационный процесс, сопровождающийся выделением побочных продуктов реакции (воды, формальдегида). Протекание таких реакций обусловливает меньшую скорость отверждения по сравнению с НС. Чтобы повысить скорость отверждения PC, необходимо добавлять некоторые вещества: гексаметилентетрамин, окислы кальция и магния, минеральные кислоты, сульфокислоты и др. Предполагают, что в процессе горячего прессования они связывают гидроксильные группы фенольных ядер и являются, таким образом, дополнительным сшивающим агентом:

Таким образом, НС получают при рН < 7 при взаимодействии бифункциональных фенолов с формальдегидом или трифункциональных фенолов с формальдегидом в условиях недостатка последнего. PC образуется при рН > 7 в результате взаимодействия трифункциональных фенолов с формальдегидом, а также при рН < 7 из трифункциональных фенолов и формальдегида в условиях избытка последнего. НС превращается в резольную при обработке формальдегидом (в случае получения НС на основе трифункциональных фенолов), a PC — в новолачную при обработке фенолом в кислой среде.
Date: 2015-11-15; view: 2599; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |