
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры решения типовых задач. Пример 1. Укажите, какие из приведенных соединений HNO3, NO, NH3 могут проявлять только окислительные
Пример 1. Укажите, какие из приведенных соединений HNO3, NO, NH3 могут проявлять только окислительные, только восстановительные и как окислительные, так и восстановительные свойства.
Решение. HNO3 – всегда окислитель, так как содержит азот (N+5) в высшей степени окисления:
N+5 + 8 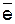 «N-3 (окислитель, процесс восстановления),
«N-3 (окислитель, процесс восстановления),
N+5 – 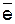 -/® (восстановительная способность отсутствует).
-/® (восстановительная способность отсутствует).
NO – может быть и окислителем, и восстановителем, так как содержит азот в промежуточной степени окисления (N+2):
N+2 «N+5 + 3 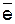 (процесс окисления, восстановитель),
(процесс окисления, восстановитель),
N+2 + 5 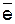 «N-3 (процесс восстановления, окислитель).
«N-3 (процесс восстановления, окислитель).
NH3 – всегда восстановитель, так как содержит азот в низшей степени окисления (N-3):
N-3 «N+5 + 8 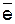 (процесс окисления, восстановитель)
(процесс окисления, восстановитель)
N-3 + 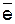 -/® (окислительная способность отсутствует).
-/® (окислительная способность отсутствует).
Пример 2. Объясните, возможны ли окислительно-восстанови-тельные реакции между следующими веществами: а) H2S и HJ; б) H2S и H2SO3; в) H2SO3 и HСlO4?
Решение.
а) Степень окисления серы в H2S равна – 2, степень окисления йода в HJ – (–1). Так как и сера, и йод находятся в низших степенях окисления, то оба вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут.
б) В H2S сера имеет низшую степень окисления S-2; в H2SO3 сера находится в промежуточной степени окисления S+4.
Следовательно, взаимодействие этих веществ возможно, причем H2SO3 является окислителем.
в) степень окисления серы в H2SO3 равна +4, хлор в HСlO4 имеет высшую степень окисления +7. Реакция между H2SO3 и HСlO4 возможна, H2SO3 в этом случае проявляет восстановительные свойства.
Пример 3. Составьте уравнение окислительно-восстановитель-ной реакции, протекающей по схеме:
KMnO4 + H3PO3 + H2SO4(среда)  MnSO4 + H3PO4 + K2SO4 +H2O.
MnSO4 + H3PO4 + K2SO4 +H2O.
Решение. Определяем степени окисления элементов в исходных веществах и продуктах реакции:
 Осуществляем выбор окислителя и восстановителя.
Осуществляем выбор окислителя и восстановителя.
Окислитель − KMnO4 (степень окисления марганца в реакции понижается).
Восстановитель − H3PO3 (степень окисления фосфора в ходе реакции повышается).
Составляем уравнения электронного баланса для окислителя и восстановителя:
 восстановитель 5 Р+3
восстановитель 5 Р+3  Р+5 + 2
Р+5 + 2 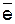 (процесс окисления),
(процесс окисления),
окислитель 2 Мn+7 + 5 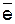
 Мn+2 (процесс восстановления).
Мn+2 (процесс восстановления).
 |
5Р+3 + 2Мn+7  5Р+5 + 2Мn+2.
5Р+5 + 2Мn+2.
Стехиометрические коэффициенты определяем методом электронного баланса с помощью электронных уравнений. Общее число электронов, отданных восстановителем, равно числу электронов, присоединяемых окислителем. Наименьшее общее кратное для отданных (2) и принятых (5) электронов равно 10. Для восстановителя и продукта его окисления получаем коэффициент 5, для окислителя и продукта его восстановления – коэффициент 2. Коэффициенты перед веществами, атомы которых не меняют свою степень окисления, находим методом подбора. Уравнение реакции будет иметь вид:
2КМnO4 + 5Н3РО3 + ЗН2SO4  2МnSO4 + 5Н3РО4 + К2SO4 + ЗН2O.
2МnSO4 + 5Н3РО4 + К2SO4 + ЗН2O.
Правильность подобранных коэффициентов определяем балансом кислорода в обеих частях уравнения (8+15+12=8+20+4+3).
Date: 2015-10-19; view: 478; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |