
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химическое равновесие. 4.14.1. Состояние равновесия
4.14.1. Состояние равновесия
Реакции, протекающие при одних и тех же условиях одновременно в противоположных направлениях, называютсяобратимыми.
Рассмотрим простую обратимую реакцию, которая протекает в закрытой системе
A + B «C + D.
Скорость прямой реакции описывается уравнением
 ,
,
где 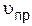 – скорость прямой реакции;
– скорость прямой реакции; 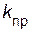 – константа скорости прямой реакции.
– константа скорости прямой реакции.
С течением времени концентрации реагентов А и В уменьшаются, скорость реакции снижается (рис.4.7, кривая 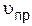 ).
).
Реакция между А и В приводит к образованию веществ C и D, молекулы которых при столкновениях могут вновь дать вещества А и В.
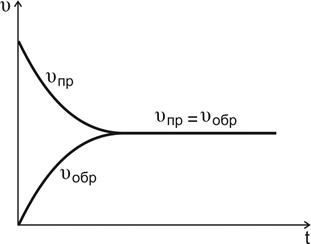
Рис. 4.7. Изменение скоростей прямой и обратной реакций во времени
Скорость обратной реакции описывается уравнением
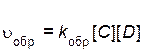 ,
,
где  – скорость обратной реакции;
– скорость обратной реакции; 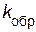 – константа скорости обратной реакции.
– константа скорости обратной реакции.
По мере того как концентрации веществ C и D возрастают, скорость обратной реакции увеличивается (рис.4.7, кривая  ).
).
В какой-то момент времени скорости прямой и обратной реакций становятся равными
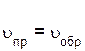 .
.
Такое состояние системы называется состоянием равновесия.
В состоянии равновесия концентрации всех его участников перестают меняться во времени. Такие концентрации называются равновесными.
Равенство скоростей прямой и обратной реакций – это кинетическое условие химического равновесия.
4.14.2. Константа равновесия
При равенстве скоростей прямой и обратной реакций
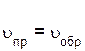
справедливо равенство
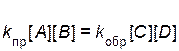 ,
,
где [ A ], [ B ], [ С ], [ D ] – равновесные концентрации веществ.
Поскольку константы скоростей не зависят от концентраций, равенство можно записать иначе:
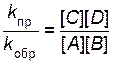 .
.
Отношение констант скоростей прямой и обратной реакций
(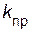 /
/ 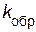 ) называют константой химического равновесия:
) называют константой химического равновесия:
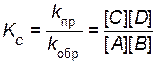 . .
| (4.19) |
Константа равновесия является постоянной величиной для данной реакции при данной температуре. Величина константы равновесия зависит от природы реагирующих веществ и температуры, но не зависит от концентрации реагирующих веществ.Она показывает соотношение между концентрациями продуктов реакции и исходных веществ, которое устанавливается при равновесии.
Рассмотрим сложную реакцию
aA + bB «cC + dD.
Любую сложную химическую реакцию можно представить в виде ряда простых реакций. Для каждой из простых реакций можно записать кинетическое уравнение прямой и обратной реакций и соответствующие им выражения для констант равновесия. Константа равновесия сложной реакции равна произведению констант равновесия простых реакций, описывающих ее механизм
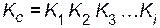 .
.
Поэтому в суммарное выражение для константы равновесия равновесные концентрации войдут в степенях их стехиометрических коэффициентов:
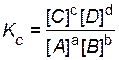 . .
| (4.20) |
Date: 2015-10-19; view: 454; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |