
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры решения типовых задач. Пример 1. При сгорании 1 кг метана выделилось 50137,5 кДж теплоты
Пример 1. При сгорании 1 кг метана выделилось 50137,5 кДж теплоты. Рассчитайте стандартную энтальпию образования метана ∆Н оСН4.
Решение.
1. Пересчитаем количество участвующего в реакции метана, выраженное в граммах, в моли (учитывая, что молярная масса СН4 равна 16 г/моль):
Количество СН4в молях n равно:
n СН4=  =62,5 моль.
=62,5 моль.
2. Рассчитаем количество теплоты, выделяющееся при сгорании 1 моля метана:
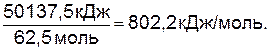
3. Запишем термохимическое уравнение реакции горения метана:
CH4(г) + 2О2(г) = CО2(г) + 2Н2О(г), Q р=802,2 кДж,
Q р=− ∆Н ор=(∆Н оСО2(г) +2 ∆Н оН2О(г))−(∆Н оСН4(г) +2 ∆Н оО2(г))=
=[(−393,5)+2(−241,8)−(∆Н оСН4(г))−2(0)]=−802,2 кДж.
Отсюда: ∆Н оСН4=(802,2−393,5−483,6)=−74,9 кДж/моль СН4.
Пример 2. Рассчитайте количество теплоты, которое выделится при полном сгорании 100 л этана, взятого в газообразном состоянии при н.у., если в результате реакции образуется СО2(г) и Н2О(г).
Решение.
1. Реакция горения этана выражается термохимическим уравнением
С2Н6(г) + З,5O2(г) = 2CO2(г) + 3Н2О(г); ∆Н р=−1559,87 кДж.
2. Переведем количество участвующего в реакции этана, выраженное в литрах (н.у.), в моли (учитывая, что 1 моль газа при н.у. занимает объем, равный 22,4 л):
Количество этана в молях n равно:
n С2Н6(г)=  =4,46 моль.
=4,46 моль.
3. Находим значения стандартных энтальпий образования (∆Н о298) для всех веществ, участвующих в реакции (Прил. табл. 2) и рассчитываем тепловой эффект в расчете на один моль С2Н6(г):
∆Н ореакции=(2 ∆Н оСO2(г) +3 ∆Н оН2O (г))−(∆Н оС2Н6(г) +3,5 ∆Н оO2(г))=
= [2(−393,5)+3(−241,8)]−[−84,7+3,5×0]=−1427,7 кДж/моль С2Н6(г).
Q р=− ∆Н ор=1427,7 кДж.
4. Пересчитаем полученный тепловой эффект на реальное количество этана, т.е. на 4,46 моля (100 л, н.у.):
Q р=− ∆Н ореальн.=1427,7×4,46=5767,42 кДж.
Пример 3. Не производя вычислений, определите знак изменения энтропии в следующих реакциях. Рассчитайте изменение энтропии для стандартных условий и сравните с результатом оценки.
1) 2NН3(г) = N2(г) + 3H2(г),
2) NH4NO3(тв) = N2O(г) + 2Н2О(г),
3) 2Н2(г) + O2(г) = 2Н2O(г),
4) 2Н2(г) + O2(г) = 2Н2O(ж).
Решение. Изменение энтропии реакции можно оценить качественно в случае реакции с участием газов. При переходе вещества в газообразное состояние происходит сильное увеличение энтропии, превышающее другие факторы, влияющие на энтропию. Поэтому по количеству вещества газов в правой и левой частях уравнения реакции можно определить, возрастает энтропия или уменьшается.
В первой реакции из 2-х молей вещества, находящегося в газообразном состоянии образуется 4 моля веществ, находящихся в газообразном состоянии, следовательно, S 1>0.
Изменение энтропии этой реакции в стандартных условиях (∆S о298) равно:
∆S о298= S оN2(г)+3 S оН2(г)−2 S оNН3(г)=191,5+ 3×130,5−2×192,7=197,6 Дж/К.
Во второй реакции 1 моль вещества в твердом состоянии образует 3 моля газообразных веществ, следовательно, ∆S 2>0. Изменение энтропии этой реакции в стандартных условиях (∆S о298) равно:
∆S о298= S оN2О(г)+2 S оН2О(г) – S оNН4NO3(тв) =219,8+2×188,7−151=446,2 Дж/К.
В (3) и (4) реакциях уменьшается как общее число молей, так и число молей газообразных веществ, так что ∆S 3<0 и ∆S 4<0, при этом D S 4 имеет более отрицательное значение, т.е. больше по абсолютной величине чем ∆S 3, так как S Н2О(г) > S Н2О(ж).
Пример 4. Установите возможность восстановления диоксида титана до свободного металла по следующей реакции при стандартных условиях и при 2500 К (зависимостью ∆H ори ∆S орот температуры пренебречь):
TiO2(тв) + 2С(тв) = Ti(тв) + 2СО(г).
Решение. Из второго закона термодинамики следует, что самопроизвольно протекают только такие реакции, которые сопровождаются уменьшением энергии Гиббса (∆G р<0).
1. Рассчитаем ∆ G ор для стандартных условий с учетом табличных данных (см. прил. табл. 2):
∆ G орекции=(2∆ G оСО(г)+∆ G оTi(тв))−(∆ G оTiO2(тв) +2 ∆G оС(тв)) =
= [2(−137,1)+0]−[(−888,6)−2×0] =614,4 кДж.
Поскольку ∆ G ор>0, реакция при 298 К невозможна.
2. Рассчитаем изменение энергии Гиббса этой реакции для 2500 К, для чего воспользуемся уравнением:
∆G т=∆ Hо p− T∆S оp.
Находим изменения ∆H оpи ∆S оpпри стандартных условиях:
∆H оpеакции=(2 ∆H оСО(г) + ∆H о Ti(тв))−(∆H о TiO2(тв)+2 ∆H о С(тв)) =
= [2(−110,5)+0]−[(−943,9)−2×0 ]=722,9 кДж=722900 Дж.
∆S оpеакции=(2 S оСО(г)+ S оTi(тв))−(S оTiO2(тв)+ S оС(тв))=
= [2×197,5+30,6]−[50,3-2×5,7 ]=363,9 Дж/К.
∆ Gт= ∆H ор− T∆ Sор=722900−2500×363,9=−186850 Дж.
∆G 2500=−186,85 кДж.
Поскольку ∆G 2500< 0, то реакция при 2500 К возможна.
Пример 5. Вычислите температуру, при которой в стандартном состоянии установится равновесии реакции:
2 NO2(г)  N2O4(г),
N2O4(г),
если известны: ∆Н ореакции=−55,3 кДж; ∆S ореакции=−175,8 Дж/К.
Решение. Используя для расчета стандартные значения функций состояния, имеем в виду стандартное состояние системы. Если одновременно это равновесное состояние, то ∆G ореакции=0. Применяем уравнение:
∆G ор= ∆H ор− T∆ Sор=0.
Преобразуем его и подставляем числовые значения:
 =314,56 К (41,4оС).
=314,56 К (41,4оС).
Система находится в равновесном стандартном состоянии при температуре 41,4 оС.
Date: 2015-10-19; view: 672; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |