
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Стр. 43
Поскольку имеется волновое движение, то для его математического описания должно существовать волновое уравнение. Так как для световых и звуковых волн уравнения движения известны, то можно найти такое уравнение и для электронных волн (волн де Бройля).
Э. Шредингер ввел некоторую функцию координат и времени, названную волновой функцией (пси-функцией), несущей при определенных условиях вероятностный смысл (квадрат ее модуля определял плотность вероятности нахождения электрона в данной точке пространства). Используя закон сохранения энергии для движущейся частицы, он записал волновое уравнение, решение которого определяло вид волновой функции.
По своему значению в квантовой механике уравнение Шредингера играет такую же роль, как второй закон Ньютона в классической механике. Подобно тому как в классической механике с помощью второго закона Ньютона решаются задачи, связанные с движением макроскопических тел, в квантовой механике с помощью уравнения Шредингера решаются задачи, связанные с движением микрообъектов.
Решения волнового уравнения показывают, что энергия микрочастиц может принимать строго определенные (дискретные) значения, позволяют для различных условий получить распределение плотности вероятности нахождения микрочастицы в пространстве (для электронов это орбитали, электронные облака).
Согласно решению волнового уравнения, электрон в атоме может находиться только в определенных квантовых состояниях, соответствующих разрешенным значениям его энергии связи с ядром. Для атома водорода энергия электрона может принимать только те значения, которые задаются выражением
En = -13,6 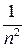 эВ,
эВ,
где п - главное квантовое число (и = 1,2,3,4,..., 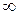 );
);
1эВ= 1,6  10-19 Дж.
10-19 Дж.
Графически энергию квантовых состояний и квантовых переходов можно изобразить с помощью схемы уровней энергии (рис. 7).
Квантовое состояние с наименьшей энергией (n = 1, Е1) называют основным. Остальные квантовые состояния с более высокими значениями энергии (E2, Е3, Е3,...) называют возбужденными.
Date: 2015-09-24; view: 347; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |