
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Энерго- и ресурсосбережение в переработке топлив
При расчете площади поверхности теплообмена в установках для нагрева жидкого топлива пользуются среднелогарифмической разностью температур, которая вычисляется по формуле:
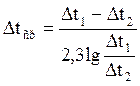
где Δtср - среднелогарифмическая разность температур, К;
Δt1 —разность температур теплоносителя (на входе) и нагреваемого вещества (на выходе);
Δt2 — разность температур теплоносителя (на выходе) и нагреваемого вещества (на входе).
Относительное движение теплоносителя и нагреваемого вещества рассматривается здесь и далее только противоточное, ибо это наиболее распространенный случай в процессах химической переработки топлива. Аналогично рассчитывается движущая сила адсорбции при улавливании продуктов химической переработки топлив.
В промышленности данные материального баланса процессов химической переработки топлив принято приводить в массовых долях, а состав образующейся при этом газовой фазы в объемных долях. Для того чтобы эти данные были сопоставимы, надо сначала найти среднюю молярную массу, газа (по аддитивности, с учетом доли каждого компонента), затем условное число молей газовой смеси.
М=∑ωi* Мi
где М— молярная масса газа, выраженная в кг/кмоль;
ωi - массовая доля компонента в газе, выраженная в долях единицы;
Мi - молярная масса компонента, выраженная в кг/кмоль.
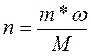
где п — условное число молей;
т — масса вещества, из которого получается газ, кг;
ω— массовая доля газа, выраженная в долях единицы;
М — средняя молярная масса газа (выраженная в кг/кмоль).
Природный и попутный нефтяной газы широко используются как топливо. Для расчетов в этом случае пользуются правилом аддитивности:
qн = ωi*qi
где ωi — массовая или объемная доля газа от исходного сырья, выраженная в долях единицы;
qi — удельная или объемная теплота сгорания компонента газа, выраженная в кДж/кг или кДж/м3.
Зная теплоту сгорания топлива, можно рассчитать нужную его массу или объем для обеспечения того или иного процесса по формуле:
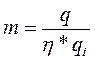
где т — масса или объем топлива, кг или м3;
q — необходимое количество теплоты для обеспечения процесса, кДж;
η — коэффициент полезного действия установки, в долях от единицы;
qi — удельная или объемная теплота сгорания топлива, кДж/кг или кДж/м3.
Пример 1. Определите среднелогарифмическую разность температур для второй ступени АВТ, где нефть нагревается от 380 К до 630 К дымовыми газами, имеющими на входе температуру 1200 К, а на выходе 620 К. Решение.
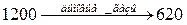 ; Δt1=1200 К - 630 К = 570 К
; Δt1=1200 К - 630 К = 570 К
 ; Δt2=620 К - 380 К = 240 К
; Δt2=620 К - 380 К = 240 К
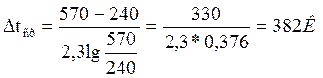
Пример 2. При каталитическом крекинге керосина массовая доля газа равна 18 % от сырья. Определите массу метана, которая получится из 1 т керосина, если объемные доли компонентов газа крекинга: H2=9; CH4=27; C2H6=12 C3H8=3,5; C2H4=25; C3H6=15; C4H8=8,5%.
Решение. Среднюю молярную массу смеси определяют по формуле:
М =0,09*2+0,27*16+0,12*30+0,035*44+0,25*28+0,15*42+0,085*56 =27,7кг/кмоль
Условное число молей смеси:
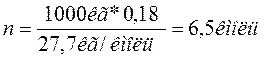
Масса метана в смеси:
m(СН4)=6,5 кмоль*16 кг/кмоль*0,27 = 28,08 (кг).
Date: 2015-09-24; view: 473; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |