
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Обработка экспериментальных данных
Опыт 1
1. Заполнить таблицу 7.
Таблица 7
Зависимость скорости реакции от концентрации тиосульфата натрия
| № пробирки | С (Na2S2O3) (относительные единицы) | ln C отн = ln(Ci / C 1) | Время реакции t, с | Скорость реакции v = 1/τ, с−1 |
| 0,693 | ||||
| 1,10 |
2. По данным таблицы 7 построить график зависимости скорости реакции от концентрации тиосульфата натрия.
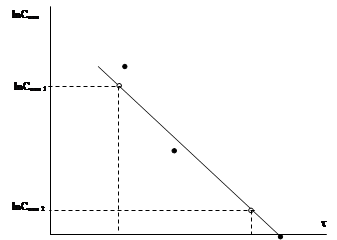
3. По данным таблицы 7 построить график зависимости в координатах ln C отн – t. Провести линию тренда – должна быть прямая зависимость. Определить тангенс угла наклона прямой. Значение тангенса угла наклона соответствует величине константы скорости реакции.
Как определять тангенс угла наклона!
Транспортиром не измерять!!!!!!!!!!
1. Выбрать на графике 2 точки подальше друг от друга.
2. По осям координат определить значения ln C отн и t для этих точек (см. рис.).
3. 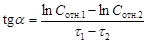 .
.

 4. Составить кинетическое уравнение, учитывая, что порядок реакции по обоим реагирующим веществам равен 1.
4. Составить кинетическое уравнение, учитывая, что порядок реакции по обоим реагирующим веществам равен 1.
Опыт 2
1. По данным таблицы 3 заполнить таблицу 8.
Таблица 8
Зависимость скорости реакции от температуры
| № п/п | Температура T, K | Время реакции t, сек. | Скорость реакции v = 1/τ, с−1 | g | Ea, кДж/моль | |
| T 1 | g1 | Ea, 1 | ||||
| T 2 | ||||||
| g2 | Ea , 2 | |||||
| T 3 |
2. Значение температурного коэффициента (коэффициента Вант-Гоффа) рассчитать по формуле:
 ,
,
рассматривая попарно Т 2 − Т 1 и Т 3 − Т 2.
3. Значение энергии активации рассчитать исходя из формулы:
 ,
,
рассматривая попарно Т 2 − Т 1 и Т 3 − Т 2.
4. Определить среднее значение коэффициента Вант-Гоффа gср.
5. Определить среднее значение энергии активации Ea , ср.
Содержание отчета по лабораторной работе
1. Название работы
2. Цель работы
3. Опыт 1
= название опыта
= экспериментальные данные (описание хода эксперимента, таблица 1 и таблица 2)
= обработка экспериментальных данных (таблица 7, графики, расчеты, значение константы скорости, кинетическое уравнение)
= вывод по опыту 1.
4. Опыт 2
= название опыта
= экспериментальные данные (описание хода эксперимента, таблица 3)
= обработка экспериментальных данных (таблица 8, расчеты)
= вывод по опыту 2
5. Опыт 3
= название опыта
= экспериментальные данные (описание хода эксперимента, таблица 4)
= написать уравнение соответствующей реакции. Почему скорость растворения мела в этих двух случаях различна?
= вывод по опыту 3
6. Опыт 4
= название опыта
= экспериментальные данные (описание хода эксперимента, таблица 5)
= Написать уравнения реакций взаимодействия хлорида железа (III) с тиоцианат калия, в результате которого образуется Fe(SCN)3 красного цвета и восстановления железа (III) в железо (II) тиосульфатом натрия, протекающую по уравнению:
2Fe(SCN)3 + 2Na2S2O3 = Na2S4O6 + 2Fe(SCN)2 + 2NaSCN
=Что являлось катализатором в данном опыте?
= вывод по опыту 4
7. Опыт 5
= название опыта
= экспериментальные данные (описание хода эксперимента, таблица 6)
= Написать уравнения реакции взаимодействия хлорида железа (III) с тиоцианатом калия, в результате которого образуется Fe(SCN)3 красного цвета;
= Как смещается равновесие при добавлении к реакционной системе хлорида железа и роданида аммония?
= Какой из реагентов больше смещает равновесие реакции в сторону образования продуктов реакции? Почему?
= Как влияет на положение равновесия добавление в систему тиоцианата аммония? В какую сторону смещается равновесие реакции?
= вывод по опыту 5
Date: 2015-09-24; view: 573; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |