
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Определение амилолитической активности микробных ферментных препаратов и ферментов солода
Цель работы: определить амилолитическую активность ферментных препаратов микробного и растительного происхождения.
Ферментные препараты обладают различной активностью.
Активность ферментного препарата (С) – скорость превращения субстрата, отнесенная на единицу массы ферментного препарата (т.е. удельная скорость превращения):
С = (ΔS/ t) /ΔФ
Единица активности фермента – это количество фермента, которое катализирует превращение 1 мкмоля субстрата в минуту при заданных условиях (температура, концентрация субстрата, рН). Обозначается буквой Е (единица).
1 Е = 1 мкмоль субстрата / мин
Амилолитическую активность или способность (АС) определяют по величине скорости ферментативной реакции гидролиза крахмала (как субстрата), отнесенной к количеству фермента, использованного для гидролиза.
Амилолитическая активность количественно характеризует способность ферментных препаратов катализировать расщепление крахмала, до декстринов с различной молекулярной массы и выражается числом единиц в 1 г препарата. Амилолитическая активность обусловлена, главным образом, присутствием α-амилазы в составе ферментных препаратов.
Декстрины очень разнообразны по молекулярной массе и физико‑химическим свойствам. В гидролизатах присутствуют амило-, эритро-, ахро-, флаво- и мальтодекстрины. Они дают окраску с йодом, отличную от крахмала. Амилодекстрины окрашиваются йодом в фиолетовый цвет, эритродекстрины – красно-бурый, ахродекстрины, флаводекстрины и мальтодекстрины – не окрашиваются йодом.
Значение амилолитической активности ферментного препарата выражают числом единиц в 1 г или в 1 (100) мл ферментного препарата.
За единицу амилолитической активности принимают такое количество фермента, которое катализирует гидролиз до декстринов 1 г растворенного крахмала (или катализирует расщепление 1 микроэквивалента гликозидных связей крахмала в минуту) в стандартных условиях.
Под стандартными условиями гидролиза крахмала для определения амилолитической активности ферментного препарата понимают:
- 1 % раствор крахмала;
- температура 30 °С;
- рН 4,7 для ферментных препаратов грибного происхождения, рН 6 – бактериального происхождения, рН 4,8-4,9 для ферментов солода;
- продолжительность гидролиза 10 минут (обеспечивает степень гидролиза крахмала от 5 до 25 %);
-концентрация субстрата в реакционной среде 0,667 %;
- объем реакционной смеси 15 мл (10 мл раствора крахмала и 5 мл 1 % раствора ферментного препарата).
Полученный гидролизат при реакции с йодом приобретает фиолетовый или красно-бурый цвет в зависимости от активности ферментного препарата, использованного для гидролиза. Степень гидролиза крахмала определяют по изменению окраски комплекса крахмала с йодом с применением фотоколориметрического метода, погрешность которого не превышает 5 %.
Исходя из оптической плотности гидролизатов рассчитывают массу гидролизованного крахмала, и далее по известным эмпирическим уравнениям рассчитывают активность ферментных препаратов. По этим уравнениям определяется амилолитическая активность (АСк, ед/г) ферментных препаратов различной природы:
- для ферментных препаратов грибного происхождения
АСк = 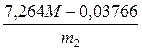 , (1.6)
, (1.6)
где M – масса гидролизованного крахмала, г;
m2 – масса ферментного препарата в реакционной среде, г;
- для ферментных препаратов бактериального происхождения
АСк = 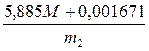 (1.7)
(1.7)
- для ферментов солода
АСк = 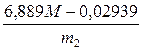 (1.8)
(1.8)
Объекты исследования и реактивы:
- основной раствор крахмала
- ферментные препараты солода (основной раствор и рабочий раствор)
- амилолитический ферментный препарат бактериального происхождения (АФП) (1 % раствор)
- амилолитический ферментный препарат грибного происхождения (ОФП) (1 % раствор)
- йод (основной раствор)
- йод (рабочий раствор)
- фосфатный буфер (рН 6,0; рН 4,7)
- кислота соляная (0,1 н раствор)
Лабораторное оборудование и посуда:
- водяная баня (термостат) шестиместная
- весы электронные
- электроплитка
- фотоэлектроколориметр
- конические колбы объемом 100 мл
- пипетки мерные объемом 2, 5, 10 мл
- цилиндры мерные объемом 10, 25, 100 мл
- стаканчики (бюксы) для взвешивания
- палочки стеклянные
- шпатели для взвешивания
Задание (может выполняться по бригадам с ферментными препаратами солода, бактериального и грибного происхождения):
1) Определить амилолитическую активность ферментных препаратов различного происхождения фотоколориметрическим йодометрическим методом.
Перед началом работы тестируют 1 % раствор крахмала: он должен иметь оптическую плотность не менее 0,3 при λ=670 нм и толщине рабочего слоя кюветы 5 мм.
Ферментативную реакцию гидролиза крахмала проводят при следующих условиях: температура реакции 30 оС, рН раствора 4,7-4,9 (для солода) или 6,0 (для АФП), рН 4,7 (для ОФП), продолжительность 10 минут, объем реакционной среды 15 мл.
Для анализа берут две колбы на 100 мл, вносят в каждую из них по 10 мл раствора крахмала и помещают в термостат при температуре 30 оС, где они выдерживаются 10-15 минут. Затем, не вынимая колб из термостата, в первую их них наливают 5 мл дистиллированной воды (контрольный раствор), а во вторую – 5 мл рабочего раствора ферментногопрепарата солода (опытный раствор). Содержимое колб хорошо перемешивают и выдерживают в термостате еще 10 минут. Затем колбы вынимают из термостата, отбирают от контрольного и опытного растворов по 0,5 мл, переносят их в колбы на 100 мл с предварительно налитыми в них 50 мл рабочего раствора йода и хорошо перемешивают. При этом растворы принимают окраску следующих цветов: контрольный – синего, опытный – фиолетово-коричневого различной интенсивности в зависимости от количества гидролизованного крахмала. Одновременно происходит инактивация фермента.
Затем на фотоэлектроколориметре определяется оптическая плотность окрашенных растворов в кюветах толщиной рабочего слоя 5 мм и длине волны λ= 670 нм. Колориметрирование проводят в сравнении с дистиллированной водой. Оптическая плотность контрольного раствора характеризует количество крахмала, использованного для ферментативной реакции, а оптическая плотность опытного раствора характеризует количество неполностью гидролизованного крахмала. Продукты неполностью гидролизованного крахмала в данном случае – это декстрины различной молекулярной массы, которые и обусловливают фиолетово-коричневую окраску раствора.
Аналогично проводят ферментативный гидролиз с использованием АФП и ОФП. Для этого используют растворы крахмала с рН 6,0 и 4,7 соответственно, далее гидролиз и анализ степени его полноты проводят по вышеприведенному описанию.
По полученным данным проводят расчет:
Массу гидролизованного крахмала (M) определяют по уравнению:
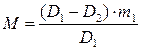 , г (1.9)
, г (1.9)
где m1 – масса крахмала, взятого на реакцию, г;
D1 – оптическая плотность контрольного раствора;
D2 – оптическая плотность опытного раствора.
Если в результате ферментативной реакции количество гидролизованного крахмала составляет от 0,02 до 0,08 г, то полученные данные используют для дальнейшего расчета амилолитической активности. Если нет, то процедуру гидролиза повторяют, причем для приготовления более концентрированного или более разбавленного рабочего раствора фермента берут большее или меньшее количество исходного основного раствора фермента.
Амилолитическую активность (АС) ферментных препаратов вычисляют по уравнениям (1-6), (1-7), (1-8) в зависимости от происхождения ферментных препаратов:
АСк = 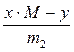 , ед/г (1.10)
, ед/г (1.10)
где х и у – коэффициенты, соответствующие ферментным препаратам грибного, бактериального или растительного происхождения; их значения указаны в уравнениях (1.6), (1.7) и (1.8) соответственно;
m2 – масса ферментного препарата в реакционной среде, г;
M – масса гидролизованного крахмала, найденная по уравнению (1.9).
Результаты измерений и расчетов заносят в таблицу 3.
Таблица 3 – Результаты эксперимента
| № | m2, г | Объем рабочего раствора фермента, мг | m1, г | D1 | D2 | M, г | АСк |
2). Определить амилолитическую активность ферментных препаратов различного происхождения визуальным колориметрическим методом
Амилолитическую активность ферментного препарата определяют также визуальным колориметрическим методом. В сравнении с йодометрическим фотоколориметрическим методом, в этом случае ферментативная реакция проводится до полного превращения крахмала в низкомолекулярные углеводы, не окрашивающиеся йодом. Активность ферментного препарата определяется временем, которое затрачивается на полный гидролиз крахмала.
Поскольку скорость каталитической реакции со временем убывает, величина амилолитической активности, измеренная при использовании визуального метода в среднем в 5 раз ниже, чем измереннаяинструментально (на фотоколориметре).
В колбу на 100 мл мерным цилиндром вносят 25 мл исходного раствора крахмала, смешивают с 15 мл дистиллированной воды и содержимое нагревают до 30 оС на водяной термостатируемой бане. Затем пипеткой вносят 10 мл рабочего раствора ферментного препарата солода и отмечают время начала гидролиза. С интервалом в одну минуту последовательно ставят йодную пробу. Для этого из колбы отбирают раствор (гидролизат) на предметное стекло, который смешивают по каплям с раствором йода. В результате такого визуального анализа проб отмечают время полного гидролиза крахмала, когда йод перестанет изменять окраску на границе соприкосновения капель (обычно это занимает от 10 до 20 минут).
Аналогично проводят ферментативный гидролиз с использованием АФП и ОФП. Для этого используют растворы крахмала с рН 6,0 и 4,7 соответственно, далее гидролиз и его анализ проводят по вышеприведенному описанию.
Величину амилолитической активности (АСвизуал.) вычисляют по формуле
АСвизуал . = 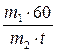 , ед/г (1.11)
, ед/г (1.11)
где m1 – масса крахмала в 25 мл анализируемого раствора, г;
60 – приведение времени к размерности минут;
m2 – масса ферментного препарата в растворе, г;
t – время полного гидролиза крахмала, мин.
Оценочно находят величину амилолитической активности для йодометрического фотоколориметрического метода с целью сравнения этого значения с экспериментально измеренным ранее:
АСк = 5 ·АСвизуал., ед/г (1.12)
Date: 2015-09-24; view: 4789; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |