
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Изучение нового материала
Класс 09.02.15
Тема: Самостоятельная работа по теме «Углеводороды»
Цель: выявить уровень учебных достижений по данной теме
Ход урока
Выполнение самостоятельной работы
1) Что такое гомологический ряд?
2) Напишите формулы 2-метилпропана, пропена, 3- метилбутина – 1
3) Какой объем хлора может присоединиться к 5л ацетилена?
4) Определите молекулярную формулу углеводорода, если массовая доля карбона в нем 90%, а относительная плотность по гелию равна 30
5) Вычислите объем воздуха, необходимый для сгорания смеси, состоящей из 5л этилена и 7л ацетилена (н.у.)
д/з повторить 19-23
Класс 13.02.15
Тема: Метанол, этанол, глицерин, их молекулярные, электронные и структурные формулы, физические свойства. Функциональная гидроксильная группа. Химические свойства: полное окисление, взаимодействие с натрием. Инструктаж по БЖД. Л.р.8 Опыты с глицерином: растворимость в воде, взаимодействие с купрум(II) гидроксидом. Д.14-15 Взаимодействие этанола, глицерина с натрием
Цель: сформировать понятия спирты, гидроксильная группа. Рассмотреть физические и химические свойства спиртов, пояснить различия между одноатомными и многоатомными спиртами. Привести примеры уравнений. Показать необходимость использования спиртов.
Ход урока
Изучение нового материала
Физические свойства метанола и этанола
Физические свойства спиртов объясняются особенностями строения их молекул. Атом Оксигена как более электроотрицательным оттягивает на себя электронную плотность связи O-H. В результате такого смещения эта связь поляризуется, на атоме водорода образуется частичный положительный заряд, а на атоме Оксигену - частичный отрицательный заряд. Частичный заряд сказывается греческой буквой d: CH3-Оd- Hd +. В таком случае говорят, что молекула полярная. Полярные молекулы спиртов образуют между собой
H-O... H-O... H-O...
| | |
R R R или с молекулами воды
H-O... H-O... H-O... H-O...
| | | |
R H R H водородные связи.
Именно водородными связями объясняется и растворимость спиртов в воде и высокие температуры кипения спиртов, и то, что среди спиртов есть газообразные вещества.
Метанол и этанол - при нормальных условиях жидкости, легче воды, имеют специфический запах, как полярные соединения, они хорошо растворимы в воде. Температура кипения метанола равна 65 ° С, этанола - 78 ° С.
Метиловый спирт - очень ядовитая жидкость. В случае попадания в организм 10 мл метанола вызывают слепоту, а 25 мл - смерть. Этиловый спирт по действию на организм является наркотиком, что в небольших дозах вызывает опьянения, в больших - смерть. Злоупотребление напитками, содержащими этанол (иначе алкоголь), вызывает заболевание - алкоголизм.
Метанол и этанол - очень похожи жидкости, различить их можно только химическим способом или температурой кипения.
Спирты - производные углеводородов, в молекулах которых есть одна или несколько гидроксильных групп OH.
Все спирты делятся на одноатомные и многоатомные
Одноатомные спирты - спирты, у которых имеется одна гидроксильная группа.
Бывают первичные, вторичные и третичные спирты:
- у первичных спиртов гидроксильная группа находится у первого атома углерода, у вторичных - у второго, и т.д.
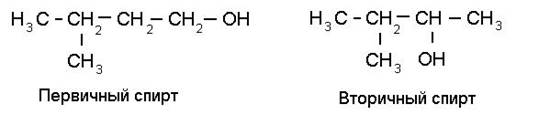
Свойства спиртов, которые являются изомерными, во многом похожи, но в некоторых реакциях они ведут себя по-разному.
Сравнивая относительную молекулярную массу спиртов (Mr) c относительными атомными массами углеводородов, можно заметить, что спирты имеют более высокую температуру кипения. Это объясняется наличием водородной связи между атомом H в группе ОН одной молекулы и атомом O в группе ОН другой молекулы.
При растворении спирта в воде образуются водородные связи между молекулами спирта и воды. Этим объясняется уменьшение объёма раствора (он всегда будет меньше, чем сумма объёмов воды и спирта по отдельности).
Наиболее ярким представителем химических соединений этого класса является этиловый спирт. Его химическая формула C2H5-OH. Концентрированный этиловый спирт (он же - винный спирт или этанол) получают из разбавленных его растворов путём перегонки; действует опьяняюще, а в больших доза - это сильный яд, который разрушает живые ткани печени и клетки мозга.
При этом нужно отметить, что этиловый спирт полезен в качестве растворителя, консерванта, средства понижающего температуру замерзания какого-либо препарата. Ещё один не менее известный представитель этого класса - метиловый спирт (его ещё называют - древесный или метанол). В отличии от этанола метанол смертельно опасен даже в самых малых дозах! Сначала он вызывает слепоту, затем просто "убивает"!
Многоатомные спирты - спирты, имеющие несколько гидроксильных групп OH.
Двухатомными спиртами называются спирты,содержащие две гидроксильные группы (группа ОН); спирты содержащие три гидроксильные группы - трёхатомные спирты. В их молекулах две или три гидроксильные группы никогда не оказываются присоединёнными к одному и тому же атому углерода.
Двухатомные спирты ещё называют гликолями, так как они обладают сладким вкусом, - это характерно для всех многоатомных спиртов
Многоатомные спирты с небольшим числом атомов углерода - это вязкие жидкости, высшие спирты - твёрдые вещества. Многоатомные спирты можно получать теми же синтетическими методами, что и предельные многоатомные спирты.
Date: 2015-09-22; view: 400; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |