
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Ход исследования
В две конические колбы на 250 см3 отобрать пипеткой или мензуркой по 100 см3 исследуемой воды. Внести в каждую по 2–3 капли метилоранжа. Одна из проб контрольная. Из бюретки по каплям приливать в одну колбу 0,1н раствор соляной кислоты до тех пор, пока от одной капли кислоты окраска перейдет из желтой в розовую. Сравните цвета растворов в колбах с исследуемой пробой и контрольной. Титрование повторите 2–3 раза. Взяв средний расход кислоты, рассчитайте карбонатную жесткость по формуле:
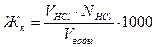 ,
,
где Жк – карбонатная (временная) жесткость, мэкв/л;
Vводы – объем воды, см3;
VHC1 – объем соляной кислоты, пошедшей на титрование, см3;
N НС1 – нормальность соляной кислоты, моль/л.
Опыт № 2. Определение общей жесткости воды
Общая жесткость воды определяется комплексонометрическим титрованием. Вода с солями жесткости титруется раствором комплексона, чаще всего раствором этилендиаминотетрауксусной кислоты (EДТА, комплексона II) или ее двунатриевой соли (комплексона III или трилона Б). Состав трилона Б выражается формулой:
 НООС – СH2 CH2COONa
НООС – СH2 CH2COONa
 N–CH2–CH2–N
N–CH2–CH2–N
НООС – CH2 CH2COONa
Реакции образования комплексных солей, происходящие при титровании воды, содержащей ионы Са2+, Mg2+ и др., трилоном Б, могут быть выражены следующими сокращенными уравнениями:
Na2H2 трил. + Ca2+ = Na2 [Ca трил.] + 2Н+;
Na2H2 трил. + Mg2+ = Na2 [Mg трил.] + 2Н+,
где трилон является лигандом.
В качестве индикатора применяется краситель – эриохром черный, ЭТ-00, образующий с ионами Mg2+, Са2+ и др. окрашенные малодиссоциирующие комплексные соединения. Эриохром черный представляет собой кислоту и действует как кислотно- основной индикатор с изменением окраски в зависимости от рН среды.
При титровании воды трилон Б сначала реагирует со свободными ионами Са2+, затем со свободными ионами Mg2+ и, наконец, извлекает Mg2+из его соединения с индикатором, изменяя окраску индикатора из вишнево-красной в фиолетовую, затем в синюю (окраска индикатора в щелочной среде при отсутствии ионов Mg2+).
Величина рН раствора около 10 является лучшей для титрования. Для создания такой среды к анализируемой пробе воды добавляют аммиачно-буферную смесь – NH4ОН +NH4C1. При рН = 10 переход окраски очень резкий, вследствие чего титрование осуществляется с большой точностью.
Date: 2015-09-24; view: 368; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |