
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Раздел 2. Типы химических реакций
Задание 4 (по вариантам)
1. Укажите тип химической реакции: N2 + O2 → 2NO; ΔH > 0.
2. Укажите химической реакции: H2 + ½ О2 → Н2О.
3. Укажите тип химической реакции: 2КМnO4 → K2MnO4 + MnO2 + О2.
4. Укажите тип химической реакции: Hg(NO3)2 + Cu → Нg↓ + Cu(NO3)2.
5. Укажите тип химической реакции: N2 + 3H2 ↔ 2NH3.
6. Определить ЭДС гальванического элемента Аu/Аu+//Мg/Мg2+ при концентрации солей 0,1 моль/л, температуре 273 К.
7. Определить ЭДС гальванического элемента Со/Со2+//Рb/Рb2+ при кон-центрации солей 1,5 моль/л, температуре 273 К.
8. Какая реакция среды будет при гидролизе солей Mg(СlO3)2, NН4NO2 в водном растворе, почему?
9. Какая реакция среды (рН<или>7) при гидролизе следующих солей: карбонат магния, сульфид цинка, ацетат бария, хлорид стронция.
10. Пойдет ли ионообменная реакция между Na2CO3 и Н2SO3? Напишите мо-лекулярное, ионные полное и краткое уравнения.
11. Пойдет ли ионообменная реакция между сульфидом калия и соляной кислотой? Напишите молекулярное, ионные полное и краткое уравнения.
12. Пойдет ли ионообменная реакция между карбонатом магния и соляной кислотой? Напишите молекулярное, ионные полное и краткое уравнения.
13. Пойдет ли ионообменная реакция между сульфидом кальция и серной кислотой? Напишите молекулярное, ионные полное и краткое уравнения.
14. Исходя из степени окисления йода и серы в соединениях Cr2(SO4)3; KJ; KJO3; Na2S и H2SO4, объясните, какие из них являются окислителями, какие восстановителями и какие могут проявлять как окислительные, так и восстановительные свойства?
15. Окисление или восстановление происходит при следующих превращениях: H2SO4 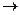 H2S; SO42-
H2S; SO42- 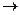 S2-; НClO4
S2-; НClO4 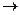 НCl; ClO4--
НCl; ClO4-- 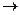 Cl-
Cl-
16. Окисление или восстановление происходит при следующих превращениях:
ClO2- 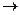 Cl2; Cr2O72-
Cl2; Cr2O72- 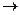 CrO32-; MnO42-
CrO32-; MnO42- 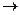 MnO4-?
MnO4-?
17. Какие металлы вытесняют водород из кислот? Дать развернутый ответ.
18. Какие металлы способны вытеснить медь из CuSO4? Дать развернутый ответ.
Date: 2015-09-22; view: 724; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |