
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основы биотехнологии 2 page
Весьма перспективным является использование тканей и органов животных, насекомых и растений как биореакторов. Наибольший интерес представляет использование молочных желез крупного рогатого скота с целью получения обогащенного специальными добавками молока или лишенного лактозы молока для лиц с дефицитом кишечной лактазы.
Понятие о метаболизме, метаболических путях, карте метаболизма. Совокупность химических превращений веществ в организме называют метаболизмом. Подавляющее большинство химических реакций в живых клетках катализируется ферментами. Вещества, участвующие в метаболизме, называются метаболитами. Метаболизм выполняет 4 функции: 1) Снабжение организма химической энергией, полученной при расщеплении богатых энергией пищевых веществ или путем преобразования энергии солнца. 2) Превращение пищевых веществ в строительные блоки, которые используются в клетке для биосинтеза макромолекул. 3) Сборка макромолекулярных (биополимеры) и надмолекулярных структур живого организма, пластическое и энергетическое поддержание его структуры. 4) Синтез и разрушение тех биомолекул, которые необходимы для выполнения специфических функций клетки и организма.
По форме усвояемого углерода все живые организмы делятся на 2 группы: 1) Автотрофные клетки ("сами себя питающие") усваивают СО2 воздуха в процессе фотосинтеза, и из него строят все свои углеродсодержащие биомолекулы (фотосинтезирующие бактерии, зеленые растения). 2) Гетеротрофные клетки ("питающиеся за счет других") получают углерод из сложных органических молекул, например, глюкозы (клетки высших животных и большинства микроорганизмов), т.е. они питаются продуктами жизнедеятельности других клеток. В биосфере автотрофы и гетеротрофы являются участниками кругооборота углерода и кислорода между животным и растительным мирами (рис. 3). По отношению к кислороду гетеротрофов делят: 1) Аэробы - требуют наличия кислорода для окисления питательных веществ. 2) Анаэробы - для окисления питательных веществ кислород не требуется. 3) Факультативные анаэробы - существуют в кислородной и бескислородной средах; 4) Облигатные анаэробы - живут только в бескислородной среде. Большинство гетеротрофов - факультативные анаэробы, которые при наличии кислорода используют аэробные метаболические пути.
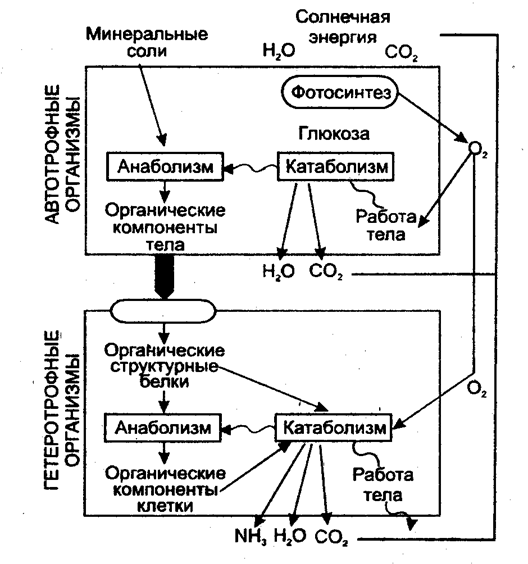
Рис. 3. Катаболизм и анаболизм у автотрофных и гетеротрофных организмов (Голубев В.Н., Жиганов И.Н., 2001).
Метаболические пути. В живой клетке многие тысячи метаболитов вступают в химические реакции. Реакционная способность метаболитов зависит от ряда условий и прежде всего, наличия соответствующих ферментов. Так, например, в мышечных клетках вся глюкоза реагирует только с АТФ и превращается в глюкозо-6-фосфат. Другие реакции не идут, т.к. нет ферментов, а некатализируемые реакции крайне медленны. Образовавшийся глюкозо-6-фосфат является заряженным веществом и поэтому не может покинуть клетку. Дальнейшие превращения глюкозо-6-фосфата определяются набором ферментов, катализирующих последовательные реакции. Т.о. получается ферментативная цепь реакций. Это и есть метаболический путь. Метаболические пути всех веществ связаны друг с другом общими метаболитами и образуют единую сетку реакций - карту метаболизма.
Ферменты и метаболизм. Понятие о регуляции метаболизма. Метаболизм регулируется за счет ферментов. Регуляция активности и количества ферментов лежит в основе метаболических процессов в норме и при патологии. Еще в прошлом веке Клодом Бернаром было установлено, что внутриклеточные константы сохраняются, невзирая на изменение окружающей среды. Это концепция гомеостаза в своей основе содержит координированную деятельность многих ферментативных реакций. Для идеализированной клетки используют камерную модель метаболизма. Исследователь судит о метаболизме, изучая входные и выходные параметры. Изучение самих метаболических путей затруднено. Здесь необходимы специальные приемы, например, изотопная техника. Регуляция метаболических путей осуществляется по Ленинджеру на трех уровнях: 1) Быстрое реагирование, связанное с действием аллостерических ферментов, каталитическая активность которых может меняться под влиянием особых веществ, оказывающих стимулирующее или тормозящее действие (эффекторы, модуляторы). 2) У высших организмов - гормональная регуляция, точнее - нейрогормональная регуляция. Это регуляция посредством дистантных гуморальных сигналов, действующих через мембраны, химическую модификацию или геном клетки. 3) Регуляция метаболизма (долговременная) связана с изменением концентрации данного фермента в клетке. Концентрация всякого фермента в любой данный момент определяется соотношением скоростей его синтеза и распада (индукция синтеза, например, диетой).
Катаболизм и анаболизм. Основные конечные продукты метаболизма. В наиболее употребительном значении термин "метаболизм" равнозначен "обмену веществ". В точном смысле "метаболизм" означает промежуточный обмен, т.е. превращение веществ внутри клеток с момента их поступления до образования конечных продуктов. Метаболизм складывается из двух фаз - катаболизма и анаболизма.
Катаболизм - это ферментативное расщепление крупных пищевых или депонированных молекул до более мелких с выделением энергии и запасанием ее в виде макроэргических соединений. Катаболизм идет в 3 стадии. Первая стадия - полимеры превращаются в мономеры (крахмал и гликоген - в глюкозу, белки - в аминокислоты, триацилглицерины - в жирные кислоты и др.). Вторая стадия (специфические пути катаболизма) - мономеры превращаются в общие продукты, чаще всего, ацетил-КоА. Третья стадия (общий путь катаболизма) - окисление ацетильной группы ацетил-КоА до СО2 и Н2О в реакциях цикла трикарбоновых кислот. Окислительные реакции общего пути катаболизма (ЦТК) сопряжены с цепями переноса электронов (рис. 4). При этом энергия (~ 40%) запасается в макроэргических связях АТФ.
Анаболизм - ферментативный синтез крупных полимерных молекул из простых предшественников с затратой энергии. Идет в 3 стадии, причем третья стадия катаболизма является первой стадией анаболизма.
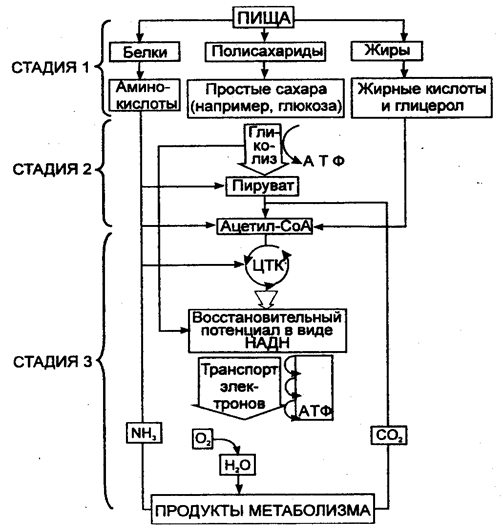
Рис. 4. Схема катаболизма.
Анаболизм и катаболизм не являются простым обращением реакций. Анаболические пути должны отличаться от путей катаболизма хотя бы одной из ферментативных реакций, чтобы регулироваться независимо. Например, специфический путь распада глюкозы до лактата (гликолиз) включает 11 реакций; синтез глюкозы из лактата включает 8 обратимых реакций распада глюкозы и 3 дополнительных реакции с новым набором ферментов. Именно на этих стадиях за счет регуляции активности ферментов регулируются суммарные скорости распада и синтеза глюкозы. Кроме того реакции катаболизма и анаболизма часто разделены мембранами и протекают в разных отсеках (компартментах) клеток. Например, распад жирных кислот идет в митохондриях, а их синтез в цитозоле. Конечные продукты метаболизма: Н2О, СО2, NН3.
Особенности метаболизма микроорганизмов представлены на рис.5.
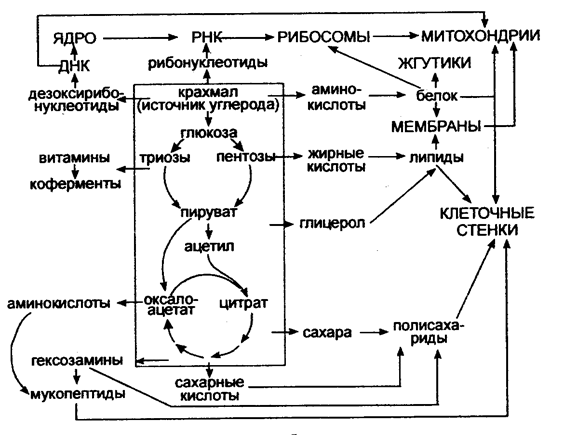
Рис. 5. Основные этапы метаболизма микроорганизмов (Голубев В.Н., Жиганов И.Н., 2001).
Большинство микроорганизмов и зеленые растения способны синтезировать все протеиногенные аминокислоты. Клетки животных не могут синтезировать все аминокислоты, в связи с чем для жизнедеятельности необходимо поступление незаменимых (не синтезируемых) аминокислот с пищей.
Исходным материалом для синтеза аминокислот микроорганизмами служат простые метаболиты (пируват, 2-оксоглутарат, оксалоацетат, фумарат, эритрозо-4-фосфат, рибозо-5-фосфат, АТФ). При синтезе большинства аминокислот аминогруппа вводится только на последнем этапе путем трансаминирования. Другие аминокислоты образуются в результате превращений других аминокислот (рис. 6). Синтезированные аминокислоты используются в процессе трансляции, т.е. синтеза белков на рибосомах с использованием генетического кода иРНК. Эти процессы лежат в основе первых успехов технологии рекомбинантных ДНК: синтез рекомбинантного инсулина клетками E.coli после введения в них гена человеческого инсулина. Синтез белков микроорганизмами, растениями, клетками насекомых, животными клетками является наиболее перспективным и разработанным методом молекулярной биотехнологии.
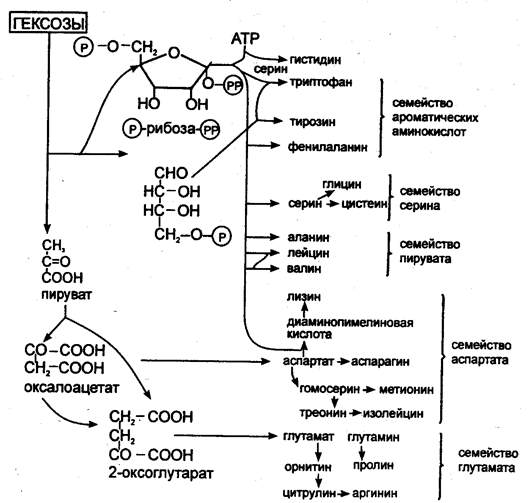
Рис. 6. Биосинтез аминокислот из молекул-предшественников (Голубев В.Н., Жиганов И.Н., 2001)
Продуценты и их селекция. Микроорганизмы, применяемые в микробиологической промышленности, принадлежат разным таксономическим группам (бактерии, фикомицеты, актиномицеты и др.). Из более чем 100000 известных видов микроорганизмов в промышленности используется около 100 видов, к которым принадлежат несколько тысяч штаммов. Промышленный штамм должен удовлетворять следующим требованиям (по Л.И.Воробьевой, 1987):
- расти на дешевых и доступных субстратах;
- обладать высокой скоростью роста биомассы и иметь высокую продуктивность целевого продукта при экономном потреблении питательного субстрата;
- проявлять направленную биосинтетическую активность при минимальном образовании побочных продуктов;
- быть генетически однородным, стабильным в отношении продуктивности и требований к питательному субстрату и условиям культивирования;
- быть устойчивым к фагам и другой посторонней микрофлоре;
- быть безвредным (не обладать патогенными свойствами) для людей и окружающей среды;
- желательно, чтобы продуценты были термофильными и ацидофильными (или алкалофильными), так как в этом случае легче предохранить ферментируемый субстрат от инвазии посторонней микрофлорой;
- целевой продукт биосинтеза должен иметь экономическую и народнохозяйственную ценность и должен легко выделяться из субстрата.
Большой интерес для производства представляют анаэробные микроорганизмы, поскольку при их культивировании не требуются энергоемкие аэрирующие устройства.
В промышленности применяют три вида штаммов микроорганизмов:
1) природные штаммы, улучшенные естественным и искусственным отбором (производство микробной массы микробного белка, использование в качестве бактериальных азотистых удобрений, биопестицидов, в производстве пищевых продуктов);
2) штаммы, измененные в результате индуцированных мутаций;
3) штаммы, полученные методами генетической или клеточной инженерии.
Принципы селекции микроорганизмов. Микроорганизмы, как объект селекции, имеют ряд особенностей (по В.Н.Голубеву, И.Н.Жиганову, 2001):
1. Выращивание микробной культуры из одной клетки – обычный для микробной селекции прием – приводит к тому, что в руках селекционера в качестве исходного материала селекции всегда оказывается особь клона (имеющего генетическую однородность). С другой стороны, клон микроорганизмов быстро достигает такой численности, что за счет естественных мутаций превращается в популяцию клеток с разными генотипами.
2. Большинство микроорганизмов гаплоидны, с одним набором хромосом, поэтому у них нет скрытой изменчивости, являющейся основой селекции высших организмов.
3. У большинства микроорганизмов, имеющих промышленное значение, до сих пор не известна способность к гибридизации (половому размножению). Это означает, что селекцию клеток можно вести только вегетативным путем.
4. Микроорганизмы характеризуются исключительно быстрой сменой поколений, поэтому возможностей для отбора положительных экземпляров у селекционера-микробиолога значительно больше. Оценку выбранного микроорганизма можно провести за считанные дни выращивания (в отличие от макроорганизмов, где результаты селекционной работы видны лишь через несколько лет).
5. Селекционер микроорганизмов имеет огромное число индивидуумов для отбора, что принципиально расширяет его возможности. Но оценка продуктивности каждого клона из сотен и тысяч образцов требуется такой трудоемкой работы, часто с применением ряда химических и биохимических исследований, которая вполне соизмерима с масштабами работы селекционера высших организмов.
Общая схема селекции микроорганизмов включает этапы:
1. Выбор объекта селекции.
2. Мутагенез или рекомбинация генов.
3. Отбор (естественный или искусственный).
4. Стабилизация свойств штаммов, полученных в результате селекции.
5. Консервирование различными способами.
Биотехнологическое сырье. В микробиологической промышленности использование сырья распределяется следующим образом:
- более 90% идет на производство этанола;
- 5% используется при производстве хлебопекарской продукции;
- 1,7% используется при производстве антибиотиков;
- 1,65% идет на производство аминокислот и других органических кислот.
В биотехнологических процессах 40-65% расходов приходится на сырье.
В принципе, микроорганизмы способны ассимилировать любое органическое соединение. Поэтому потенциальными ресурсами для микробиологической биотехнологии могут служить все мировые запасы органических веществ, включая первичные и вторичные продукты фотосинтеза, а также запасы органических веществ в недрах земли. Каждый конкретный вид микроорганизмов, используемый в биотехнологии, весьма избирателен к питательным веществам. В связи с этим органическое сырье (кроме лактозы, сахарозы и крахмала) без предварительной химической обработки практически не пригодно для микробного синтеза. Целлюлозосодержащее сырье после химического или ферментативного гидролиза и очистки от ингибирующих или балластных примесей (фенол, фурфурол, оксифурфурол и др.) может быть использовано в биотехнологическом производстве. Каменный уголь, природный газ и древесина могут служить сырьем для химического синтеза технических спиртов или уксусной кислоты. Последние, в свою очередь, являются отличным сырьем для микробиологической промышленности.
Традиционные источники углерода – кристаллическая глюкоза, техническая сахароза, техническая лактоза, гидрол (сиропообразная жидкость, содержащая глюкозу), крахмал, уксусная кислота, спирт этиловый синтетический, узкая фракция жидкого парафина. Низкомолекулярные спирты (метанол, этанол) можно отнести к числу перспективных видов микробиологического сырья, так как их ресурсы существенно увеличиваются благодаря успешному развитию технологии химического синтеза. Дрожжи родов Pichia, Candida, Torulopsis и др., некоторые виды бактерий (род Protaminobacter, Flavobacterium и др.) используют в качестве единственного источника углерода метанол и образуют биомассу с высоким содержанием белков (60-70%). В 1939 году В.О.Тоусоном была установлена способность разных видов микроорганизмов использовать в качестве единственного источника углерода и энергии н-алканы и некоторые фракции нефти.
Побочные продукты производства – высокомолекулярные парафины (ранее сжигались), вода после замачивания кукурузных зерен при выделении крахмала (раннее спускалась в канализацию, теперь упаривают), отходы химического производства (смеси карбоновых кислот, сульфитный щелок, зерновая и картофельная барда, меласса, соапсток, гидрол и др.) нашли применение в микробиологической промышленности как источники углерода. Так, для производства кормовых дрожжей используют сульфитный щелок, картофельную барду, зерновую барду, гидрол, солодовое сусло, молочную сыворотку, депротеинизированный сок растений, гидролизат древесных отходов и торфа. Побочные продукты производства являются сырьевым резервом для микробиологической промышленности. В нашей стране ежегодно остается неиспользованной около 1 млн. т лактозы, содержащейся в сыворотке и пахте. В США из 15 млн. т молочной сыворотки, ежегодно расходуемой на производство сыра, половина теряется со сточными водами, хотя известно, что из одной тонны сыворотки можно получить около 20 кг воздушно-сухой биомассы дрожжей. В микробиологической промышленности нашли широкое применение побочные продукты производства глюкозы из крахмала – меласса и гидрол. В мелассе содержится до 45% сахарозы, все незаменимые аминокислоты кроме триптофана, витамины и витаминоподобные вещества (биотин, пантотеновая кислота, инозит).
Источники минерального питания – неорганические и органические соли. При выращивании биомассы в концентрации 30-40 г/л потребность в добавках азотсодержащих солей обычно не превышает 0,3-0,4% от объема среды. Большинство дрожжей хорошо усваивает аммиачные соли; некоторые виды дрожжей испытывают потребность в нитратах. Часто источником азота в состав сред включают мочевину. При направленном биосинтезе, например, целлюлозолитических ферментов грибом Peniopora gigantea наивысшая биохимическая активность клеток наблюдается на средах с органическим азотом (аспарагин, пептон и др.). Микроорганизмы для построения своих компонентов и обеспечения энергетики требуют поступления фосфора, магния, кальция, железа и других элементов (10-3-10-4 М. Повышенная потребность микроорганизмов в микроэлементах возникает, если целевой метаболит содержит микроэлемент. Например, при биосинтезе витамина В12 в питательную среду включают кобальт. Избыточное введение некоторый ионов может изменить потенциал клеток (отрицательный в норме, 16-20 мВ), что нарушит их биологические и продуцентные свойства.
Комплексные обогатители сред необходимы для оптимизации роста и функционирования микроорганизмов: кукурузный экстракт, дрожжевой автолизат, экстракт, гидролизат, клеточный сок картофельных клубней, молочная сыворотка, экстракт пшеничных отрубей, экстракт солодовых проростков и др. Иногда добавляют мясной и рыбный пептоны. Для культивирования животных клеток используют экстракт плаценты, плазму крови животных. Для выращивания клеток растений или мицелия высших грибов применяют экстракты тыквы, листьев хлопчатника, отвар слив и др. Все эти добавки приносят витамины, аминокислоты, цитокинины и другие необходимые для роста биологически активные вещества.
Пеногасители и флокулянты. Процессы пенообразования и пеногашения необходимо регулировать при аэробном глубинном культивировании микроорганизмов. Для создания устойчивых режимов пенообразования применяют механические и химические пеногасители и их комбинации. Химические пеногасители (поверхностно-активные вещества – ПАВ) делятся на жировые и синтетические. Жиры проявляют пеногасящие свойства в относительно высоких концентрациях 0,2-1,0% от объема среды. Но их концентрация может изменяться из-за потребления микроорганизмами, а продукты их распада – жирные кислоты – могут закислять среду (нагрузка на буферную систему среды инкубации). Для пищевой промышленности выпускаются эффективные синтетические пеногасители: силиконы, пропинолы, контрамин, полиформаль и др. Для флокуляции (конгломеризации) клеток применяют химические флокулянты (хлорид кальция, соли фосфорной кислоты) или синтетические полиэлектролиты – катион-, анионактивные, неионогенные. Эффективность применения флокулянтов зависит от температуры культивирования, рН среды и физиологического состояния клеток.
Вода и кислород. Для биосинтеза 1 кг дрожжевой биомассы необходимо 1,0-2,5 кг кислорода. При интенсивном потреблении субстрата продуцент ассимилирует независимо от источника углерода 1,0-4,0 мг кислорода на 1 л среды в минуту. Растворимость кислорода относительно низкая и зависит от условий культивирования клеток. При давлении 0,1 МПа и температуре 30 ˚С в 1 л дистиллированной воды растворяется 7,5 мг кислорода. В реальной питательной среде растворимость кислорода составляет 2-5 мг/л. Запасов кислорода в среде культивирования хватает для обеспечения жизнедеятельности аэробных продуцентов в течение всего лишь 0,5-2 минут. При интенсивном перемешивании и во время интенсивного роста биомассы увеличивается потребление кислорода. Введено понятие о критической концентрации кислорода, при которой лимитируется дыхание клеток: при росте на сахаросодержащих средах критическая концентрация кислорода 0,05-0,1 мг/мл (3-8% от полного насыщения среды кислородом). Оптимальной для роста биомассы считается концентрация кислорода 50-60% от полного насыщения, для биосинтеза целевых метаболитов – 10-20%.
Вода составляет 80-90% биомассы микроорганизмов. Для приготовления питательных сред требуется чистая вода: не более 50 мг/л хлоридов и не более 60 мг/л сульфитов. Концентрации ионов металлов (мг/л) не должны превышать следующих значений: цинк – 5,0, медь – 3,0, фтор – 1,5, свинец – 0,2, мышьяк – 0,05.
Объектами молекулярной биотехнологии являются разнообразные биологические системы:
- микроорганизмы;
- клеточные линии насекомых;
- клеточные линии растений;
- клеточные линии животных;
- многоклеточные организмы (растения, домашние и лабораторные животные).
Во многих случаях генетически модифицированная самовоспроизводящая биологическая единица – микроорганизм, вирус, растение или животное – является конечным коммерческим продуктом. Среди множества биологических объектов, используемых в молекулярной биотехнологии, чаще применяются Escherichia coli, одноклеточные дрожжи Saccharomyces cerevisiae и различные клеточные линии животного происхождения. Все они играют важную роль в получении белков, кодируемых клонированными генами. Рассмотрим наиболее значимые молекулярно-биотехнологические системы.
Прокариоты и эукариоты. Все живые организмы делят на две группы: прокариоты и эукариоты. Прокариотические клетки (например, бактериальные): 1) хромосомная ДНК находится в цитоплазме, 2) клетка окружена ригидной клеточной стенкой, в состав которой часто входит пептидогликан (но не хитин или целлюлоза), 3) в клетке нет субклеточных цитоплазматических органелл. Эукариотическая клетка имеет: 1) ядро, отделенное от цитоплазмы ядерной мембраной, хромосомная ДНК находится в ядре, 2) клеточная стенка, если она есть, может содержать хитин или целлюлозу, но не пептидогликан, 3) в цитоплазме содержатся различные субклеточные органеллы (митохондрии, лизосомы, хлоропласты и др.).
Кишечная палочка (Escherichia coli) – один из наиболее хорошо изученных биотехнологических объектов (генетика, молекулярная биология, биохимия, физиология, общая биология). Это грамотрицательная непатогенная подвижная палочка длиной менее 1 мкм. Ее средой обитания является кишечник человека, но она также может высеваться из почвы и воды. Благодаря способности размножаться простым делением на средах, содержащих ионы натрия, калия, магния, кальция, аммония, хлора, фосфата, сульфата, микроэлементы и источник углерода (например, глюкозу), E.coli стала излюбленным объектом научных исследований. При культивировании E.coli на обогащенных жидких питательных средах, содержащих аминокислоты, витамины, соли, микроэлементы и источник углерода, время генерации (т.е. время между образованием бактерии и ее делением) в логарифмической фазе роста при температуре 37 ˚С составляет примерно 22 мин.
Для каждого живого организма существует определенный температурный интервал, оптимальный для его роста и размножения. При слишком высоких температурах происходит денатурация белков и разрушение важных клеточных компонентов, что ведет к гибели клетки. При низких температурах биологические процессы существенно замедляются или останавливаются совсем вследствие структурных изменений, которые претерпевают белковые молекулы. Исходя из температурного режима, который предпочитают те или иные микроорганизмы, их можно подразделить на термофилы (от 45 ˚С до 90 ˚С и выше), мезофиллы (от 10 ˚С до 47 ˚С) и психрофилы, или психротрофы (от -5 ˚С до 35 ˚С). Микроорганизмы, активно размножающиеся лишь в определенном диапазоне температур, могут быть полезным инструментом для решения различных биотехнологических задач. Например, термофилы часто служат источником генов, кодирующих термостабильные ферменты, которые применяются в промышленных или лабораторных процессах, а генетически видоизмененные психротрофы используют для биодеградации токсических отходов, содержащихся в почве и воде, при пониженных температурах.
E. coli можно культивировать как в аэробных (в присутствии кислорода), так и в анаэробных (без кислорода) условиях. Однако для оптимальной продукции рекомбинантных белков E.coli и другие микроорганизмы обычно выращивают в аэробных условиях. Если целью культивирования бактерий в лаборатории является синтез и выявление определенного белка, то культуры выращивают на сложных жидких питательных средах в колбах. Для поддержания нужной температуры и обеспечения достаточной аэрации культуральной среды колбы помещают в водяную баню или термостатируемую комнату и непрерывно встряхивают. Такой аэрации достаточно для размножения клеток, но не всегда – для синтеза белка. Рост клеточной массы и продукция белка лимитируются не содержанием в питательной среде источников углерода или азота, а содержанием растворенного кислорода: при 20 ˚С оно равно примерно девяти миллионным долям. Это становится особенно важно при промышленном получении рекомбинантных белков с помощью микроорганизмов. Для обеспечения условий, оптимальных для максимальной продукции белков, конструируют специальные ферментеры и создают системы аэрации.
Широкое применение клеток E.coli связано со следующим:
1. Эффект Лурия-Дельбрюка – устойчивость E.coli к бактериальным вирусам (бактериофагам) обусловлено именно произошедшими в них мутациями, а не реакцией бактерий на воздействие со стороны бактериофага.
2. Эффект Ледерберга-Татума – между членами генетически неоднородной популяции E.coli может происходить обмен генетической информацией (т.е. как и двуполых организмов, в результате физического обмена между хромосомами могут возникать новые генетические комбинации (генетическая рекомбинация). Ледерберг и Татум создали различные штаммы E.coli, индуцируя те или иные мутации и отбирая клетки с разнообразными наследуемыми дефектами метаболизма. Например, одна чистая культура могла синтезировать вещества А,В,С, но не D или Е (ее обозначили АВСde). Параллельно создали другую чистую культуру, abcDE. Смешав эти культуры, получили бактерии ABCDE. Ни в одной из чистых культур тип ABCDE не возникал спонтанно. Экспериментально исключив остальные возможные причины образования комбинации ABCDE, было доказано, что она возникает в результате физического обмена генетическим материалом между двумя хромосомами.
Микроорганизмы, используемые в молекулярной биотехнологии, делят на две группы:
1. Микроорганизмы как источники специфических генов (например, ген термостабильной ДНК-полимеразы, используемой в полимеразной цепной реакции).
2. Микроорганизмы, созданные генноинженерными методами для решения определенных задач (например, различные штаммы Corynebacterium glutamicum, которые были генетически модифицированы с целью повышения продукции промышленно важных аминокислот.
Дрожжи (Saccharomyces cerevisiae) – это непатогенные одноклеточные микроорганизмы с диаметром клетки около 5 мкм, которые во многих отношениях представляют собой эукариотический аналог E.coli. Их генетика, молекулярная биология и метаболизм детально изучены. S. cerevisiae размножаются почкованием и хорошо растут на такой же простой среде, как и E.coli. Их способность к превращению сахара в этанол и углекислый газ издавна использовалась для изготовления алкогольных напитков и хлеба. В настоящее время ежегодно во всем мире расходуется более 1 млн. тонн S. cerevisiae. Эти клетки являются наиболее удобной моделью для исследования других эукариот (например, многие гены, ответственные за регуляцию клеточного деления S. cerevisiae аналогичны таковым у человека). Это открытие способствовало идентификации и характеристике генов человека, отвечающих за развитие новообразований. В 1996 г. была определена полная нуклеотидная последовательность всего набора хромосом S. cerevisiae.
Синтезированный бактериальной клеткой эукариотический белок часто приходится подвергать ферментативной модификации, присоединяя к белковой молекуле низкомолекулярные соединения – во многих случаях это необходимо для правильного функционирования белка. К сожалению, E. coli и другие прокариоты не способны осуществлять эти модификации, поэтому для получения полноценных эукариотических белков используют S. cerevisiae и другие виды дрожжей.
Культуры эукариотических клеток. При всех различиях между типами эукариот методические подходы к культивированию клеток насекомых, растений и млекопитающих имеют много общего. Сначала берут небольшой кусочек ткани данного организма и обрабатывают его протеолитическими ферментами, расщепляющими белки межклеточного материала (при работе с растительными клетками добавляют специальные ферменты, разрушающие клеточную стенку). Высвободившиеся клетки помещают в сложную питательную среду, содержащую аминокислоты, антибиотики, витамины, соли, глюкозу и факторы роста. В этих условиях клетки делятся до тех пор, пока на стенках емкости с культурой не образуется клеточный монослой. Если после этого не перенести клетки в емкости со свежей питательной средой, то рост прекратится. Обычно удается переносить (перевивать, субкультивировать) и поддерживать до 50-100 клеточных генераций исходной (первичной) клеточной культуры, затем клетки начинают терять способность к делению и гибнут. Культивируемые клетки сохраняют некоторые свойства исходного клеточного материала, поэтому их можно использовать для изучения биохимических свойств различных тканей.
Date: 2015-09-27; view: 1420; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |