
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Глава 5. РАК ЖЕЛЧНОГО ПУЗЫРЯ И ВНЕПЕЧЕНОЧНЫХ ЖЕЛЧНЫХ ПРОТОКОВ
Первичный рак желчного пузыря составляет 2—8 % всех злокачественных новообразований и по частоте занимает пятое место среди опухолей органов пищеварения.
Женщины болеют чаще мужчин, соотношение колеблется в пределах 1: 2—1: 14, около 90 % больных старше 50 лет (И. Ф. Линченко, Н. С. Выродов, 1981; А. П. Даценко и соавт., 1985; В. П. Дудко, 1987).
Этиология и патогенез. Рак желчного пузыря и желчных протоков, как правило, развивается на фоне желчнокаменной болезни. Это находит свое отражение не только в том, что районы распространения этих заболеваний практически идентичны, но и в увеличении удельного веса больных раком пропорционально длительности течения желчнокаменной болезни (И. Ф. Линченко, Н. С. Выродов, 1981; С. А. Шалимов и соавт., 1991).
Среди причин взаимосвязи желчнокаменной болезни и рака желчного пузыря указывают на механическое раздражение слизистой оболочки при постоянном перемещении камней (Н. Н. Петров,1974).
Экспериментальными исследованиями доказано канцерогенное влияние желчи больных желчнокаменной болезнью (J G. Fortner, 1958). Возможно, это связано с действием глицина или таурина в сочетании с дезоксихолевой кислотой (Е. Vaittinen, 1970).
Повышенная заболеваемость раком желчных протоков отмечена у рабочих, имеющих контакт с бета-нафтиламином и бензиди-ном (Т. F. Mancuso, A. A. Attar, 1967).
Прогрессирование рака желчного пузыря и желчных протоков часто приводит к возникновению обтурационной желтухи. Однако желтухи может и не быть. Прогноз заболевания в большинстве случаев неблагоприятный — пятилетняя выживаемость не превышает 7 % (W. Neugebaner и соавт., 1979).
Особо неблагоприятно для прогноза прорастание опухоли за пределы подслизистого слоя стенки желчного пузыря (A. Andersson и соавт., 1976). Все наблюдавшиеся нами больные (21) с таким характером поражения умерли в течение 2,5 года после операции, несмотря на то, что первичная опухоль была удалена.
В то же время первичные опухоли желчных протоков отличаются более длительным течением, чем метастатические. Однако быстро присоединяющиеся обтурационная желтуха, холангит и печеночная недостаточность обычно приводят к летальному исходу еще до возникновения отдаленных метастазов (G. Klatskin, 1965; Okuda и соавт., 1977).
Патологическая анатомия. Под действием канцерогенного фактора эпителий желчного пузыря подвергается папиллярной или аде-номатозной гиперплазии. Кроме того, наблюдается метаплазия клеток слизистой оболочки (И. С. Дерижанова, 1966; В. В. Елисеев, 1977).
Морфологическое исследование 200 желчных пузырей, удаленных по поводу холелитиаза и холецистита, выявило гиперплазию эпителия в 83% наблюдений, атипическую' гиперплазию — в 13,5 %, рак in situ —в 3,5% (J- Albores-Saavedra и соавт., 1980).
Аденокарциномы составляют 95,3 % злокачественных опухолей желчного пузыря и 97,7 % — желчных протоков (W. Neugebaner и соавт., 1979).
Реже встречаются аденоакантома, рабдомиосаркома, анаплас-тический и недифференцированный рак (А. А. Шалимов и соавт., 1985; J. В. Blalock 1978; А. О'Меага, 1981). Слизистый рак диагностирован у 14 %, скирр — у 10 % больных злокачественными новообразованиями желчного пузыря (Г. И. Жидовинов, В. В. Кожанов, 1982).
Е. С. Футорян и Н. П. Забазиый (1979) обнаружили рак желчного пузыря у 56 оперированных больных, рак желчных протоков — у 97.
По данным Т. Tsuzuki, M. Uekusa (1978), V. Kinami и V. Miya-zaki (1982), опухоль локализовалась на уровне развилки печеночных протоков у 75—71 % больных, на уровне общего желчного протока — у 25—29 %.
В желчном пузыре опухоль чаще начинает расти в области тела и реже — в шейке и пузырном протоке.
Распространение рака желчного пузыря происходит в перихо-ледохеальные и панкреатодуоденальные лимфатические узлы, по мелким венам, нервам (A. Andersson и соавт., 1976); в печень, париетальную и висцеральную брюшину, большой сальник (J. S. Агnaud и соавт., 1979). Венозный отток из желчного пузыря идет одновременно в обе доли печени, а лимфоотток минует печень (А. П. Даценко и соавт., 1985; Н Schmidt и соавт., 1977). В этом авторы видят причину быстрой генерализации опухолевого процесса.
Выделяют узловой, инфильтрирующий и сосочковый типы роста опухолей желчных протоков, которые встречаются соответственно у 50, 43,8 и 6,2 % больных (F. Kinami, L. Miyazaki, 1982).
Клиника. Первые проявления рака желчного пузыря и протоков неспецифичны и характеризуются ухудшением самочувствия, общей слабостью, периодически возникающей тупой болью в правом подреберье, повышением температуры тела до субфебрильной. Прогрессирование болезни сопровождается более четким проявлением симптомов.
Мы наблюдали 105 больных раком желчного пузыря. У 55,8 % больных рак развился на фоне желчнокаменной болезни. Разнообразие и выраженность клинической семиотики рака желчного пузыря предопределяют значительный процент диагностических ошибок при направлении больных в клинику, а также при первичном осмотре на консультативном приеме (соответственно 80 и 65 %, по данным С. А. Шалимова и соавторов, 1990). То есть даже в условиях специализированного консультативного приема клинико-лабораторные данные позволяют заподозрить рак желчного пузыря только у 38 % больных.
Желтуха при раке желчных протоков отмечается у 97—100 % больных (Н. Н. Блохин и соавт., 1982, наши наблюдения). В тоже время при раке желчного пузыря мы наблюдали желтуху только у 57 % обследованных больных.
При раке желчных протоков желтуха развивалась в среднем через 1,5 мес после появления первых симптомов болезни. Чем ближе к воротам печени располагалась опухоль, тем менее выраженным болевым синдромом сопровождалось появление желтухи.
Злокачественные новообразования в области ворот печени характеризуются наиболее скудной симптоматикой. Длительность периода от появления первых симптомов болезни до развития желтухи не превышает 1,5 мес. Желтуха развивается исподволь, без боли. Температура тела не превышает 37,5 °С. По мере прогрессирования заболевания присоединяются признаки печеночной недостаточности— вялость движений, адинамия, замедление психических реакций. Осмотр и пальпация не выявляют каких-либо существенных дополнительных данных. Печень увеличена, плотной консистенции. В поздних стадиях болезни печень бугристая из-за множественных метастазов.
Опухоли общего желчного протока сопровождались достаточно выраженным болевым синдромом. У 33 % больных боль имела характер типичной печеночной колики. Одновременно повышалась температура тела до 38—39 °С, а через 2—4 сут появлялась желтуха. Диагностика осложнялась тем, что у 19 % больных ранее была выявлена желчнокаменная болезнь. Увеличенный, болезненный желчный пузырь удалось пальпировать у 4 больных.
Частоту клинических проявлений рака внепеченочных желчных протоков, исключая опухоли дистального отдела общего желчного протока, приводят W. R. Chitwood и соавторы (1982), обследовавшие 60 больных. Субъективные признаки: желтуха — 91,7 %, потеря массы тела — 71,7%, боль в животе — 65,0%, кожный зуд — 50 %, тошнота, рвота — 45,0 %, обесцвеченный кал — 28,3 %, темная моча — 25%, лихорадка, озноб — 16,7 %, отсутствие аппетита— 13,3%, боль в спине — 5%; объективные признаки: увеличение печени — 56,7%, инфильтрат в брюшной полости — 30%, напряжение мышц передней брюшной стенки— 18,3 %, увеличение селезенки — 5%. Мы наблюдали идентичные клинические признаки опухолей этой локализации. У больных раком желчного пузыря
желтуха возникала в среднем через 3 мес после появления первых симптомов болезни. Возникновению желтухи, как правило, предшествовали клинические признаки холецистита — тупая боль в правом подреберье, повышение температуры тела до 38 СС и более.
В соответствии с особенностями клинической картины рака желчного пузыря выделяют три группы больных (А. М. Ганичкин и соавт., 1979): 1-я группа — с преобладанием клинических симптомов желчнокаменной болезни и хронического холецистита; 2-я группа — с признаками острых осложнений желчнокаменной болезни— острым холециститом и (или) желтухой; 3-я группа — с признаками далеко зашедшего опухолевого процесса, метастазами в печень, карциноматозом брюшины, асцитом, кахексией.
Диагностика. До операции точный диагноз рака внепеченочных желчных протоков удается установить на основании клинической картины заболевания в сочетании с данными прямого контрастирования желчных протоков — чрескожной чреспеченочной и (или) эндоскопической ретроградной холангиографии. При невозможности выполнить прямое контрастирование желчных протоков, а также у больных с опухолями желчного пузыря обычно ограничиваются определением показаний к хирургическому лечению, а точный диагноз устанавливают во время операции. Диагноз рака желчного пузыря до операции удалось установить только у 20,7 % из 77 больных (Г. И. Жидовидов, В. В. Кожанов, 1982). Удаление опухоли оказалось возможным только у 20 больных, то есть у большинства была поздняя стадия процесса. Несомненно, что в начале заболевания правильная диагностика еще более затруднена.
Ввиду скудности клинико-лабораторной семиотики важное значение в диагностике рака желчного пузыря и желчных протоков приобретают инструментальные методы диагностики. Проведенная нами оценка информативности отдельных методов инструментального исследования с учетом инвазивности метода и степени его безопасности для больного показала, что наиболее информативными и неинвазивными являются методы двухмерной ультразвуковой эхотомографии и компьютерной томографии.
На эхотомограммах больных раком желчного пузыря выявлялось характерное увеличение размеров желчного пузыря, неравномерная плотность и утолщение его стенок, наличие дополнительных эхо-сигналов в его просвете, а также тесно связанных со стенкой плотных акустических масс без ультразвуковой тени.
Наряду с характерной эхографической картиной рака желчного пузыря ультразвуковое исследование позволяет выявить очаговые изменения в печени и метастазы. Под контролем ультразвуковой томографии в сомнительных случаях можно произвести прицельную диагностическую пункцию желчного пузыря, а также метастазов печени с последующей гистологической верификацией исследуемого материала. При первичных и метастатических опухолях желчных протоков ультразвуковое исследование позволяет выявить расширение внутрипеченочных протоков и дифференцировать характер желтухи.
По нашим данным, достоверность метода ультразвуковой эхо-томографии в диагностике рака желчного пузыря достигает 67— 68 %. Высокая информативность, неинвазивность, абсолютная безвредность и необременительность для больного, возможность многократного повторения исследований, выполнения пункции под его контролем делают этот метод незаменимым на первом этапе диагностики рака желчного пузыря, который мы условно назвали определяющим.
На втором этапе диагностики рака желчного пузыря и желчных протоков, который мы назвали уточняющим, основными задачами являются окончательная верификация диагноза, а также определение распространенности ракового процесса. Из всех многочисленных инструментальных методов исследования, применяющихся в этих целях, наиболее эффективными являются лапароскопия и прямое контрастирование желчных протоков при распространении рака желчного пузыря на желчные протоки с развитием механической желтухи.
По нашему мнению, лапароскопия играет главную роль в определении операбельности больного и может рассматриваться как альтернатива лапаротомии при неоперабельных опухолях. Только наличие канцероматоза брюшины, множественных метастазов в обе доли печени и отдаленные органы заставляют отказаться от лапаротомии.
При распространении рака желчного пузыря на желчные протоки и развитии механической желтухи, а также при первичных опухолях протоков необходимо уточнить характер желтухи, протяженность зоны поражения, а также состояние протоковой системы проксимальнее и дистальнее зоны поражения. Это достигается применением ультразвуковой эхотомографии в сочетании с методами прямого контрастирования желчных протоков. Исследование начинаем с ультразвукового томосканирования. На эхограммах печени больных с механической желтухой определяются характерные изменения.
Сразу же после установления характера механической желтухи производим ретроградную эндоскопическую панкреатохолангиографию. При этом после канюляции большого сосочка двенадцатиперстной кишки заполняем проксимальные отделы желчных протоков контрастным веществом. Раковая обтурация различных отделов желчных протоков представлена на рис. 107.
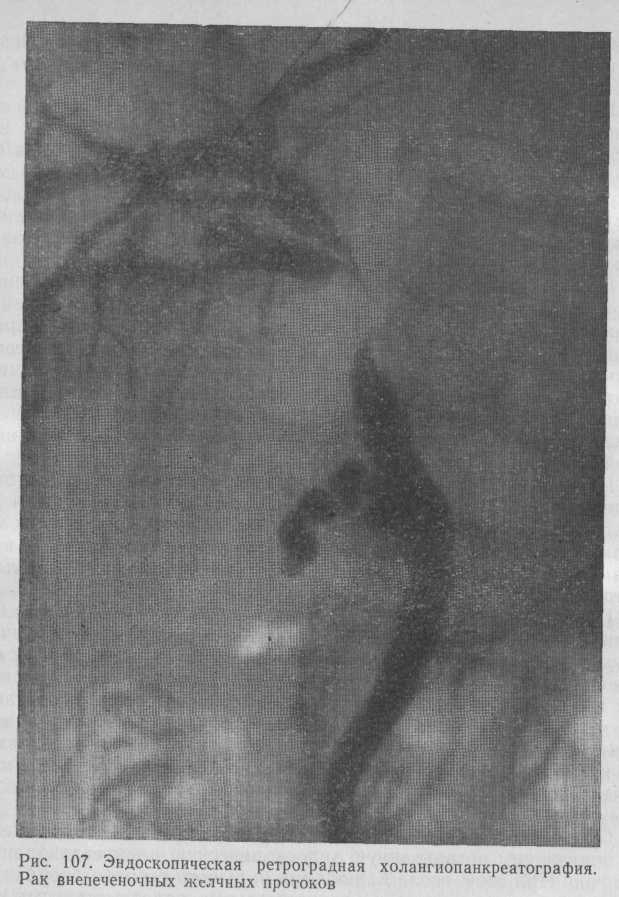
Для получения полной информации о состоянии проксимальных отделов желчевы-водящих путей в тот же день под контролем ультразвукового исследования производим чрескожную чреспеченочную холангиографию с контрастированием желчных протоков проксимальнее зоны поражения (рис. 108).
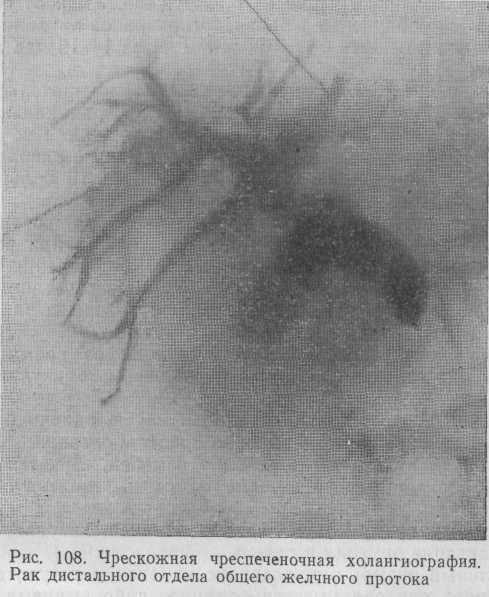
Сопоставляя полученные холангиограммы получаем информацию об уровне блока, его протяженности, а также о состоянии желчных протоков проксимальнее и дистальнее места обтурации, что позволяет заранее наметить объем предстоящей операции.
Методы лечения. Основной метод лечения рака желчного пузыря и желчных протоков — оперативный. Консервативные методы применяют лишь на подготовительном этапе. Интоксикация, явления печеночно-почечной недостаточности на фоне желтухи всегда требуют проведения интенсивной терапии, которую, как показал наш опыт, следует проводить не дольше 3 дней.
Лучевую и химиотерапию при раке желчного пузыря и желчных протоков проводят по показаниям и схемам, принятым для лечения рака поджелудочной железы.
Облучение в дозе 50—100 Гр дробными дозами через 4 нед после операции W. R. Chitwood и соавторы (1982) провели 17 больным раком желчных протоков. Средняя продолжительность жизни составила (9,3 ±2,6) мес. Авторы применили одновременно наружное облучение в дозе 50 Гр с введением по чреспеченочному дренажу в желчные протоки иридия-192 на срок от 21 до 100 ч. Глубина эффективного излучения от последнего источника составляет 10 мм. В сроки от 3 до 13 мес после облучения признаков опухоли при контрольной холангиографии не обнаружено. Умер от сепсиса через 4 мес после облучения 1 больной (признаков опухоли на аутопсии не выявлено). Пять больных живы через 1—12 мес после курса терапии.
Хирургическое лечение включает два вида вмешательств: 1) радикальные 2) паллиативные. Удельный вес радикальных операций в связи с поздней диагностикой очень низкий. Так, Preitner и соавторы (1984) удалось выполнить радикальные операции у 7 из 41 больного раком желчного пузыря и у 6 из 18 больных раком желчных протоков.
В целях дифференцированного анализа возможности применения различных видов оперативных вмешательств при раке желчного пузыря и желчных протоков, а также определения эффективности холецистэктомии (изолированной или в сочетании с удалением частей других органов) при различных формах рака желчного пузыря мы выделили следующие его формы.
1. Макроскопических признаков опухоли во время операции нет, изменения типичные, как при хроническом калькулезном холецистите.
2. Желчный пузырь опухолевидно изменен, однако патологический процесс не распространяется за пределы органа.
3. Желчный пузырь опухолевидно изменен, имеются увеличенные регионарные лимфатические узлы в гепатодуоденальной связке.
4. Желчный пузырь опухолевидно изменен, визуально выявляется прорастание опухоли в печень.
5. Желчный пузырь опухолевидно изменен, в результате блокады пузырного протока имеется водянка, либо эмпиема желчного пузыря, либо околопузырный абсцесс.
6. Желчный пузырь опухолевидно изменен, опухолевая инфильтрация распространяется на гепатодуоденальную связку и соседние органы (двенадцатиперстную кишку, желудок, толстую кишку и парааортальные лимфатические узлы).
Выбор адекватного объема операции определяется стадией процесса, общим состоянием больного, характером и тяжестью осложнений, уровнем непроходимости желчевыводящих путей. Все оперативные вмешательства по поводу рака желчного пузыря делят на 3 группы: 1) радикальные; 2) паллиативные; 3) пробные лапа-ротомии.
Характер выполненных нами операций по поводу рака желчного пузыря отражен в табл. 21.
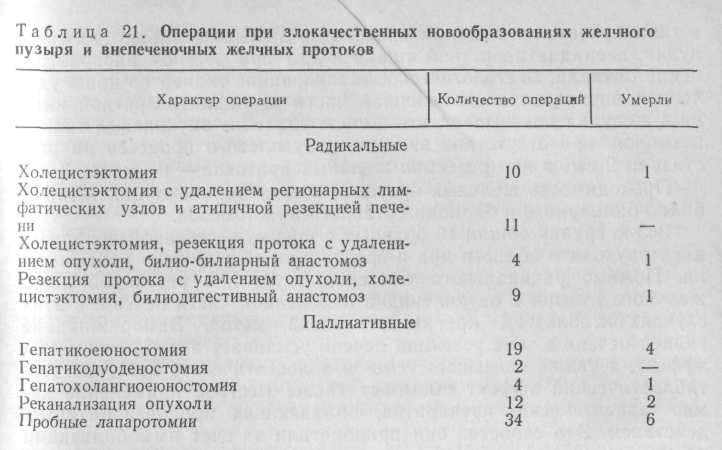
Различные виды радикальных операций произведены у 34 (32,4 %) больных. Причем в последние годы, благодаря широкому применению ультразвуковой эхотомографии и других инструментальных методов диагностики, удельный вес радикальных операций увеличился. Все больные раком желчного пузыря, которым выполнены радикальные операции, условно разделены на 3 группы.
В первую группу вошли 10 больных, оперированных по поводу холелитиаза, хронического калькулезного холецистита (6), острого деструктивного холецистита (3) и хронического «бескаменного» холецистита (1). Рак желчного пузыря выявлен при гистологическом исследовании удаленного препарата.
Ретроспективная оценка отдельных этапов операции у этих больных позволяет высказать некоторые соображения в отношении методики выполнения холецистэктомии у этой категории больных.
Во всех случаях при малейшем подозрении на рак (чрезмерная плотность отдельных участков желчного пузыря, чрезмерная инфильтрация окружающих желчный пузырь тканей и органов — двенадцатиперстной кишки, желудка, правой доли печени, правой почки) требуется обязательное срочное гистологическое исследование тканей желчного пузыря и прилежащих к нему органов.
2. Даже отрицательные результаты срочной операционной биопсии требуют выполнения холецистэктомии, удаления увеличенных лимфатических узлов гепатодуоденальной связки, ложа желчного пузыря с краевой резекцией печени в области ложа и криодест-рукцией тканей в этой зоне.
Вторую группу составили 14 больных, у которых опухоль преимущественно локализовалась в теле или шейке желчного пузыря. Радикальная операция в этих случаях предполагает, помимо удаления желчного пузыря, скелетизацию элементов гепатодуоденальной связки ввиду наиболее частого поражения регионарных узлов,
а также резекцию желчных протоков и других органов (части желудка, двенадцатиперстной кишки и др.) при местном распространении опухоли. Гистологическое исследование тканей по краю удаленной опухолевидно измененной части двенадцатиперстной кишки и желудка показывает, что полное удаление опухолевых тканей возможно при отсутствии видимого опухолевого процесса на расстоянии 2 см, а при резекции желчных протоков — не менее 3 см. Проходимость желчных протоков восстанавливают наложением билио-билиарного и билиодигестивного анастомозов.
В 3-ю группу вошли 10 больных с преимущественной локализацией опухоли в области дна и врастанием ее в правую долю печени. Помимо радикального удаления опухоли с резекцией ложа желчного пузыря и опухолевидно измененной части печени, в этих случаях используем криохирургический метод. Замораживание тканей печени в зоне резекции печени усиливает антибластический эффект, а также оказывает гемо- и холестатическое действие. Антибластический эффект вызывает также местное применение хи-миотерапевтических препаратов, обладающих пролонгированным действием. Это свойство они приобретали за счет иммобилизации на матрице из полиметилсилоксана (кремнийорганического полимера), обладающей двоякой функцией: она защищает иммобилизованный химиопрепарат от ускоренной биодеградации и проявляет местное детоксицирующее действие, адсорбируя кислые гидрофобные метаболиты, полипептиды, липополисахариды и др. По нашим данным, в результате применения иммобилизованного фторурацила, циклофосфана, цист-платины или адриабластина число местных рецидивов рака снизилось в 2 раза, практически не возникают послеоперационные осложнения.
Билиодигестивный анастомоз накладывают, если удается выделить участок расширенных желчных протоков выше опухоли. Обычно соустье накладывают непосредственно с общим печеночным протоком, а не с желчным пузырем (в последнем случае высока вероятность холангита, а в дальнейшем — обструкции пузырного протока вследствие роста опухоли). Учитывая возможность роста опухоли, желательно накладывать анастомоз с петлей тощей кишки, выключенной из пассажа пищи по Ру или Шалимову.
Техника гепатикоеюностомии не отличается от таковой при рубцовых стриктурах желчных протоков.
Паллиативная холедохоеюностомия выполнена нами у 19 больных, холедоходуоденостомия — у 2 больных с опухолями желчных протоков. Печеночная недостаточность, холангит, кровотечение из острых язв желудка и двенадцатиперстной кишки привели к 4 летальным исходам в ранний послеоперационный период.
Реканализация печеночных протоков с проведением дренажа через опухоль показана, если опухоль расположена на уровне развилки долевых печеночных протоков и удаление ее невозможно.
Техника реканализации желчных протоков заключается в следующем. Вскрывают просвет общего печеночного протока на 5— 7 мм ниже опухоли. В проток вводят металлический зонд с диаметром оливы 2—3 мм и с усилием продвигают в направлении одного из долевых протоков. Необходимо строго придерживаться хода протоков, а также соизмерять усилия с плотностью опухоли во избежание прорыва зондом стенки воротной вены и ее ветвей. Аналогичным методом реканализируют второй долевой печеночный проток. Затем, используя зонды с большим диаметром оливы, расширяют образованный канал до 5—7 мм в поперечнике. Для обеспечения постоянного оттока желчи через созданный канал проводят транспеченочный дренаж по Smith. Дистальный конец дренажа устанавливают таким образом, чтобы он был ниже места вскрытия стенки желчного протока. Последнюю зашивают наглухо.
Криодеструкцию опухоли при температуре —180°С в течение 10 мин в сочетании с реканализацией ее мы применили у 3 больных.
Необходимость одномоментной реканализации желчных протоков обеих долей печени до настоящего времени окончательно не доказана (J. L. Cameron и соавт., 1978). Считают, что двусторонняя реканализация обеспечивает лучший паллиативный эффект (Т. Tsuzuki, N. Uekusa, 1978). Наши наблюдения свидетельствуют о том, что реканализация протоков только правой доли печени, хотя и сопровождается значительным улучшением состояния больного и уменьшением уровня билирубина в крови, однако не избавляет больного полностью от желтухи. В связи с этим считаем допустимым отказ от двусторонней реканализации желчных протоков только в том случае, если рентгенологически установлено сообщение между протоками обеих долей, либо при массивном прорастании опухоли.
Гепатохолангиоеюностомию по Longmire или по аналогичным методикам производят, если реканализация опухоли не удалась, либо при отказе от попыток реканализации из-за значительных размеров опухоли. Модификация гепатохолангиоеюно-стомии, применяемая в клинике, заключается в следующем. Рукояткой скальпеля тупо разделяют печень по левому краю круглой связки на глубину до 2 см. Первым препятствием по ходу расслоения является облитерированная ветвь пупочной вены. Ее перевязывают с обеих сторон и пересекают. При дальнейшем углублении обнажаются желчный проток, артерия и вена III сегмента печени. Пункцией устанавливают желчный проток и вскрывают его продольным разрезом на длину, вдвое превышающую диаметр протока. В приводящий и отводящий концы вводят дренажные трубки, которые фиксируют обвязыванием протока на них. Петлю тощей кишки, выключенную из пассажа пищи, подводят к месту расслоения печени и подшивают отдельными серозно-капсульными швами ниже его. Иссекают серозный и мышечный слои стенки кишки на участке, соответствующем размерам углубления в печени. Вскрывают просвет кишки на небольшом участке. На расстоянии 10—15 см от десерозированной поверхности накладывают кисетный шов, внутри которого вскрывают просвет кишки. Через отверстия на десерозированном участке, а также внутри кисетного шва проводят дренажи желчных протоков, выводя их наружу. Слизистую оболочку кишки обвязывают кетгутовой нитью вокруг дренажных трубок и вводят внутрь углубления в печени. Отдельными серозно-капсульными швами поднимают кишку к печени вокруг передней и боковых стенок соустья, герметизируя его. К месту анастомоза подводят перчаточно-трубчатый дренаж. Дренажи желчных протоков выводят наружу по типу подвесной еюностомы.
Если по каким-либо причинам разделение печени по ходу круглой связки невозможно, используют подход к желчному протоку III сегмента через четырехугольник Краковского. Мы применили гепатохолангиоеюностомию у 4 больных.
Вшивание подкапсулярных желчных протоков в тощую кишку производят при неудалимых опухолях долевых печеночных протоков и их развилки в тех случаях, когда под-капсульные протоки значительно расширены и могут обеспечить эффективный отток желчи. Методика операции заключается в следующем (рис. 109).

После лапаротомии и принятия решения об объеме вмешательства петлю тощей кишки проводят через брыжейку поперечной ободочной кишки и подшивают к капсуле печени на 4—5 мм ниже расширенного протока. По ходу протока рассекают капсулу печени, проток выделяют и пересекают. Периферическую культю протока лигируют, а центральную продольно рассекают на протяжении до 5 мм. В петле тощей кишки делают отверстие, по размерам соответствующее диаметру протока. В кишку вставляют дренажную трубку, которую фиксируют одним швом к стенке кишки. Анастомозируют края протока и кишку, при этом дренажную трубку вторым концом вводят в просвет желчного протока. Рассеченные стенки протока прошивают П-образным швом, концы которого через отверстие в кишке вводят в просвет ее, а затем выкалывают наружу. Таким образом желчный проток инваги-нируется в просвет кишки. Дополнительными серозно-капсульными швами герметизируют соустье. Если имеется несколько расширенных подкапсульных желчных протоков, анастомозы по описанной методике накладывают с каждым из них. Петлю кишки, использованную для анастомозов, выключают из пассажа пищи по Шалимову или Ру. К месту анастомозов подводят перчаточно-трубчатый дренаж.
Вшивание подкапсулярных желчных протоков в желчный пузырь производят также при неудалимых опухолях долевых печеночных протоков и их развилки, если подкапсу-лярные протоки расположены вблизи желчного пузыря, а проходимость пузырного и общего желчного протоков хорошая (рис. 110).
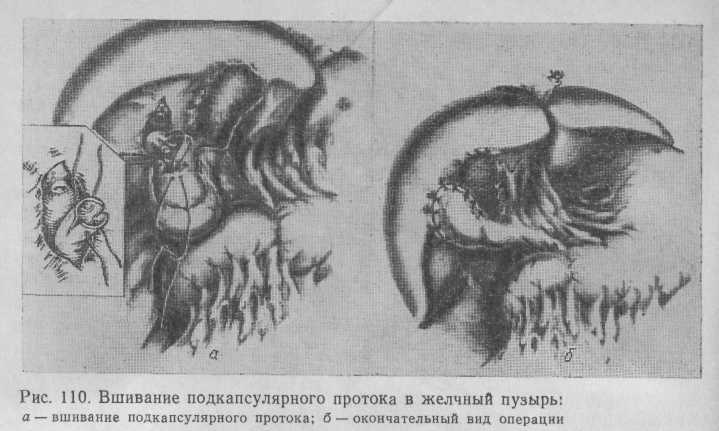
Г е п а т о х о л а н г ио г а стр ос то м и я по Dogliotti выполнена нами у 1 больного. Послеоперационный период сопровождался выраженным холангитом, изжогой, обусловленной поступлением большого количества желчи в желудок и рефлюксом пищи в желчные протоки. В дальнейшем от выполнения подобных операций мы отказались в пользу гепатохолангиоеюностомии по Longmire.
Из 37 больных, которым были произведены паллиативные операции по поводу опухолей развилки печеночных протоков, умерли в ближайший послеоперационный период 7. У 6 больных с печеночной недостаточностью II—III степени (по И. В. Ярема, 1980) прогрессирование ее после операции привело к летальному исходу, несмотря на то что отток желчи через дренаж восстановился в объеме до 300 мл в сутки у 3 из них. Эти наблюдения свидетельствуют о том, что попытки реканализации опухоли или гепатохо-лангиоеюностомии с паллиативной целью эффективны только при отсутствии или начальных признаках печеночной недостаточности в предоперационный период.
Средняя продолжительность жизни после восстановления оттока желчи у больных с неудалимыми опухолями развилки печеночных протоков составила (49,7±7) нед. Рецидив желтухи в последние 3—8 нед жизни наступил у 5 больных, что было обусловлено блокадой опухолью сегментарных и долевых печеночных протоков по данным чресдренажной холангиографии.
Наружный дренаж желчных протоков в качестве паллиативного метода лечения опухолевой непроходимости протоков выполняют в виде чрескожной чреспеченочной холангиостомии в тех случаях, когда по результатам предоперационного обследования установлена невозможность радикального хирургического вмешательства.
Чрескожная реканализация опухоли желчных протоков получила распространение в последнее время. Техника операции заключается в следующем (J. A. Oleaga и Е. J. Ring, 1981). Чрескожную чреспеченочную холангиографию выполняют тонкой иглой с надетым на нее полиэтиленовым катетером. После попадания иглы в желчный проток катетер придерживают, а иглу извлекают. По катетеру вводят металлический проводник, которым проходят через опухоль в нижележащие отделы желчных протоков. При неудачной попытке реканализации проводник удаляют, сохраняя наружную холангиостому. Повторная попытка реканализации через 24—48 ч, как правило, оказывается успешной. По проводнику вводят катетер, фиксируют его к коже отдельным швом и оставляют в желчных протоках. После этого наружный конец катетера закрывают, и отток желчи происходит естественным путем в двенадцатиперстную кишку. Смену катетера производят 1 раз в 3—4 мес.
Лапаротомией ограничивают объем оперативного вмешательства у тех больных, у которых не удается создать эффективный отток желчи — при наличии массивной опухоли в воротах печени и множественных метастазов в обеих долях ее, а также при раке желчного пузыря, не сопровождающемся желтухой. В наших наблюдениях из 34 больных после лапаротомии умерли 6 (17,3 %). Продолжительность жизни составила (9±3) нед.
Повторные операцииу больных раком желчных протоков и желчного пузыря производили Е. С. Футорян и Н. П. Забазный (1979). Интервал между первичной и повторной операцией составлял от 1 до 27 мес. Авторы указывают, что при поражении желчных протоков паллиативные вмешательства были эффективными у 11 больных, а у 2 больных удалось даже удалить опухоль. В то же время при раке желчного пузыря из-за местной распространенности опухоли пришлось ограничить объем повторной операции у 2 из 3 больных.
Дальнейший прогресс в лечении рака желчного пузыря и вне-печеночных желчных протоков связан в значительной мере с ранней диагностикой заболевания, а также разработкой эффективных методов комбинированной терапии. Профилактика заболевания связана со своевременным плановым хирургическим лечением хо-лелитиаза.
СПИСОК ЛИТЕРАТУРЫ
Альперович Б. И. Альвеококкоз и его лечение.— М.: Медицина, 1972.— 272 с. Альперович Б. И. Хирургия печени.— Томск: Изд-во Томск, ун-та, 1983.— 349 с. Арикьянц М. С, Тышко А. Г., Захараш М. П. Анаэробная инфекция в хирургии
печени и желчных путей.— К.: Наук, думка, 1991.— 112 с. Аскерханов Р. П. Хирургия эхинококкоза.— Махачкала: Даг. кн. изд-во, 1976.—
205 с.
Блохин Н. Н., Итин А. Б., Клименков А. А. Рак поджелудочной железы и внепече-
ночных желчных путей.— М.: Медицина, 1982.— 271 с. Боровков С. А. Операции на печени.— М.: Медицина, 1968.— 218 с. Брегадзе И. Л. Наружные желчные свищи // Наружные и внутренние свищи в
хирургической клинике.— М.: Медицина, 1982.— С. 89—124. Брегадзе И. Л., Константинов В. М. Альвеолярный эхинококкоз.— М.: Медгиз,
1963.—224 с.
Виноградов В. В., Мазаев П. Н., Гришкевич Э. В. Рентгеноманометрическое исследование желчных путей.— Л.: Медицина, 1966.— 164 с.
Виноградов В. В., Зима П. И., Кочиашкили В. И. Непроходимость желчных путей.—М.: Медицина, 1977.— 312 с.
Вишневский А. А., Ульманис Я. Л., Гришкевич Э. В. Желчеотводящие анастомозы.—М.: Медицина, 1972.—304 с.
Галкин В. А., Линденбратен Л. Д., Логинов А. С. Распознавание и лечение холецистита.— М.: Медицина, 1972.— 184 с.
Гальперин Э. И., Островская А. М. Контрастные исследования в хирургии желчных путей.— М.: Медицина, 1964.— 165 с.
Гальперин Э. И., Кузовлев Н. Ф., Карагюлян С. Р. Рубцовые стриктуры желчных протоков.— М.: Медицина, 1982.— 240 с.
Гальперин Э. И., Волкова В. Н. Заболевания желчных путей после холецистэкто-мии.—М.: Медицина, 1988.—272 с.
Гальперин Э. И., Дедерер Ю. М. Нестандартные ситуации при операциях на печени и желчных путях.— М.: Медицина, 1987.— 336 с.
Гранов А. М., Борисов А. Е.— Эндоваскулярная хирургия печени.— Л.: Медицина, 1986.—226 с.
Дедерер Ю. М., Крылова Н. П. Атлас операций на печени.— М.: Медицина, 1975.—200 с.
Дедерер Ю. М., Крылова Н. П., Устинов Г. Г. Желчнокаменная болезнь.— К.: Медицина, 1983.— 176 с.
Дейнека И. Я. Эхинококкоз человека.— М.: Медицина, 1968.— 376 с.
Земское В. С, Радзиховский А. П., Панченко С. Н. Хирургия печени.— К.: Наук, думка, 1985.— 150 с.
Ищенко И. Н. Операции на желчных путях и печени.— К.: Здоров'я, 1966.— 473 с.
Королев Б. А., Гагушин В. А. Хирургия цирроза печени.— М.: Медицина, 1973.— 160 с.
Королев Б. А., Пиковский Д. Л. Осложненный холецистит.— М.: Медицина, 1971.—239 с.
Кочиашвили В. И. Атлас хирургических вмешательств на желчных путях.— М.з Медицина, 1971.—208 с.
Линденбратен Л. Д. Рентгенология печени и желчных путей.— М.: Медицина,
1980.—518 с.
Милонов О. Б., Смирнов В. А. Внутренние желчные свищи. Наружные и внутренние свищи в хирургической клинике.— М.: Медицина, 1982.—С. 125—151. Милонов О. Б., Грязное С. Н. Двойное внутреннее дренирование общего желчного
протока.— М.: Медицина, 1986.— 157 с. Милонов О. Б., Тоскин К. Д., Жебровский В. В. Послеоперационные осложнения
и опасности в абдоминальной хирургии.— М.: Медицина, 1990.— 559 с. Напалков П. И., Артемьева Н. Н., Качурин В. С. Пластика терминального отдела
желчного и панкреатического протоков.— Л.: Медицина, 1980.— 184 с. Петров Б. А., Гальперин Э. И. Хирургия внепеченочных желчных протоков.— М.:
Медицина, 1971.—200 с.
Петровский Б. В. Хирургическая гепатология.— М.: Медицина, 1972.— 352 с. Реконструктивная хирургия при поражениях внепеченочных желчных протоков// Петровский Б. В., Милонов О. Б., Смирнов В. А., Мовчун А. А.— М.: Медицина, 1982.—304 с. Родионов В. В., Филимонов М. И., Могучее В. М. Калькулезный холецистит.—
М.: Медицина, 1991.—320 с. Савельев В. С, Буянов В. М., Огиев Ю. В. Острый панкреатит.— М.: Медицина,
1983.—239 с. Смирнов В. А. Смешанные и сложные желчные свищи // Наружные и внутренние
свищи в хирургической клинике.— М.: Медицина, 1982.— С. 152—154. Соколов В. И. Свищи поджелудочной железы // Наружные и внутренние свищи в
хирургической клинике.— М.: Медицина, 1982.— С. 72—87. Тальман И. М. Хирургия желчного пузыря и желчных протоков.— М.: Медгнз,
1963.—432 с.
Хирургия печени и желчных протоков / Шалимов А. А., Доманский Б. В., Клименко Г. А., Шалимов С. А.— К.: Здоров'я, 1975.— 408 с. Шалимов А. А., Шапошников В. И., Пинчук М. П. Острый перитонит.— К.: Наук.
думка.— 284 с.
Шалимов С. А. Диагностика и лечение заболеваний большого дуоденального соска.— К.: Здоров'я, 1985.— 146 с.
Шапкин В. С. Резекция печени.— М.: Медицина, 1967.— 300 с. Шапкин В. С, Гриненко Ж. А. Закрытые и открытые повреждения печени.—
М.: Медицина, 1970.—392 с.
Balasegaram M., Joishy S. К. Hepatic resection: the logical approach to surgical management of major trauma to the liver//Amer. J. Surg.— 1981.— Vol. 142.— P. 580—593. Calne R. Y. Liver transplantation for liver cancer// Wld. J. Surg.— 1982.—Vol. 6.—
P. 76—80. Cameron J. S., Maddrey W. C. Mesoatrial shunt: a new treatment for the Budd —
Chiari syndrome//Ann. Surg.— 1978.—Vol. 187.—P. 402—406. Cauinaud С Controlled hepatectomies and exposure of the intrahepatic bile
ducts.—Paris, 1981.— 112 p.
Deitsch E. A. In vivo measurements of the internal and external diameters of the common bile duct in man//Surg. Gynecol. Obstet.— 1981.— Vol. 152.— P. 642—644. Enneker C, Berens J. P. Schwerste Leberruptur mit Lebervcnenabriss und massiver
Bilhamie // Chirurg.— 1978.— Bd. 49.— S. 311—314.
Harbin W. P., Mueller P. R., Ferrucci J. T. Transhepatic chalangiography: complications and use patterns of the fineneedle technique//Radiology.— 1980.— Vol. 135, N 4.—P. 15—22.
Huguet C, Hakami F.. Block P. L'intubation Trans-Tumorale des Obstructions Neoplasiques du Hile du Foie//Ann. Chir.—1981.—Vol. 35, N 5.—P. 342— 347.
Madding G. F., Lim R. C, Kennedy P. A. Hepatic and vena caval injuries//Surg. Clin. N. Amer.— 1977.—Vol. 57, N 2.—P. 275—289.
Mallet-Guy P. Sur 1272 operations pour lithiase de la voie biliaire principale.
Choledocoduodenostomies primaires//Lyon Chir.— 1975.— Vol. 71, N 3.—
P. 155—165. Manegold В. С Moglichkeiten und Grenzen der diagnostischen une therapeutischen
ERCP beim Verschlussikterus//Chirurg.—1981.—Bd. 52, H. 7.—S. 423—432. Martin E. C, Karlson К. В., Cooperman A. Percutaneous drainage in the management of hepatic abscesses//Surg. Clin. N. Amer.— 1981.— Vol. 61, N 1.—
P. 157—167. Orloff M. J., Johansen К. Н. Treatment of Budd-Chiari syndrome by side-to-side
portacaval shunt: Experimental and clinical results//Ann. Surg.— 1978.—
Vol. 188.—P. 494—512. Safrany L. Transduodenal endoscopic sphincterotomy and extraction of bile duct
stones //Wld. J. Surg.— 1978.—Vol. 2, N 4.—P. 457—464. Thompson J. E., Tompkins R. K-, Longmire W. P. Factors in management of acute
cholangitis //Ann. Surg.— 1982—Vol. 195, N 2.—P. 137—145. Way L. W.. Bernhoft R. A., Thoams J. M. Biliary stricture//Surg. Clin. N. Amer.—
1981.—Vol. 61, N 4.—P. 963—972. Williams L. F., Schoetz D. J. Primary sclerosing cholangitis//Ibid.—P. 951—961.
Date: 2015-09-18; view: 528; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |