
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретические пояснения
Калориметрические измерения: определение водяного числа калориметра и удельной интегральной теплоты растворения соли
Цель: ознакомление с калориметрическим методом определения тепловых эффектов физико-химических процессов, определение водяного числа калориметра (суммарной теплоемкости калориметрической системы) и удельной интегральной теплоты растворения соли.
Оборудование и реактивы: калориметрическая система (рисунок 1), секундомер, мерный цилиндр, ртутный термометр, соли: KCl; Na2SO4 или другие по указанию преподавателя.
Теоретические пояснения
Калори́метр (от латинского calor — тепло) — прибор для измерения количества теплоты, выделяющейся или поглощающейся в каком-либо физическом, химическом или биологическом процессе.
Путем калориметрических измерений можно получить экспериментальные данные по теплоемкостям веществ и тепловым эффектам различных процессов. Величина и знак теплового эффекта ΔН определяется по изменению температуры калориметра.
Можно выделить два основных типа калориметров: приборы с постоянной и переменной температурой. В наших опытах используется второй тип. В ходе опыта температура системы изменяется, причем не только за счет протекания изучаемого процесса, но и частично за счет теплообмена с окружающей средой. Теплообмен в студенческих опытах стараются минимизировать, однако полностью устранить его не удается.
Теплообмен искажает истинные результаты опыта, поэтому он должен быть учтен. В настоящей работе это предлагается сделать графическим методом, который рассматривается в разделе, касающемся обработки результатов опыта.
В основе определения тепловых эффектов калориметрическим методом лежит уравнение (1).
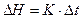 , (1)
, (1)
где 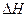 - общий тепловой эффект проводимого в калориметре процесса в изобарных условиях (энтальпия процесса);
- общий тепловой эффект проводимого в калориметре процесса в изобарных условиях (энтальпия процесса);
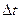 - изменение температуры в результате процесса;
- изменение температуры в результате процесса;
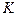 - суммарная теплоемкость калориметрической системы (водяное число).
- суммарная теплоемкость калориметрической системы (водяное число).
Водяное число, называемое также постоянной калориметра, соответствует тому количеству теплоты, которое необходимо для изменения температуры системы на 1 градус.
Удельный тепловой эффект процесса, отнесенный к 1 г вещества, измеряется в Дж/г и рассчитывается по формуле
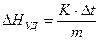 (2)
(2)
Водяное число можно рассчитать по формуле:
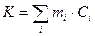 , (3)
, (3)
где mi – массы веществ, калориметра и вспомогательных устройств (мешалка, термометр, пробирка);
Сi – их удельные теплоемкости.
При обычных температурах для большинства твердых веществ истинные теплоемкости мало зависят от температуры, а удельные теплоемкости разбавленных водных растворов неорганических солей практически одинаковы (4,1 Дж/г·град).
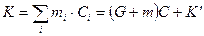 ,
,
где G – масса воды;
m – масса соли;
С – удельная теплоемкость раствора;
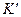 - теплоемкость калориметра и вспомогательных устройств.
- теплоемкость калориметра и вспомогательных устройств.
Если для серии опытов масса воды и массы солей остаются неизменными, то можно считать, что водяное число К будет величиной постоянной.
Для определения водяного числа в калориметре проводят такой процесс, тепловой эффект которого точно известен, например, растворение KCl в воде.
Зависимость удельной теплоты растворения KCl, выраженной в Дж/г, от температуры в интервале от 100С до 300С имеет следующий вид:
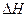 t=334,3–3,866·t, (4)
t=334,3–3,866·t, (4)
где t – средняя температура опыта, 0С.
t=0,5(t1+t2), (5)
где t1 и t2 – температуры начала и окончания растворения.
Водяное число калориметра рассчитывают по формуле:
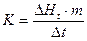 (6)
(6)
Зная величину водяного числа калориметра, можно определить удельную интегральную теплоту растворения любой неорганической соли по формуле (2).
Date: 2015-09-18; view: 501; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |