
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт №2. Зависимость буферной емкости ацетатных буферных смесей от буферного соотношения
К пяти ацетатным буферным системам с различными соотношениями соли и кислоты добавляют одинаковое количество сильного основания или сильной кислоты, измеряют pH и вычисляют их буферную ёмкость.
В пять стаканчиков налить 20 мл приготовленных буферных смесей с буферным соотношением: 100; 10; 1; 0,1; 0,01.
Измерить pH исходных буферных систем при помощи pH-метра (после каждого измерения pH электроды должны быть тщательно вымыты). Измеренное значение pH исходных смесей несколько отличается от рассчитанного, так как в этих системах  aH+
aH+ 
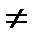 cH+.
cH+.
Во все буферные смеси добавить по 2 мл 0,1M NaOH, тщательно перемешать и снова измерить pH.
Налить в стаканчики такое же количество буферных систем и при перемешивании добавить в каждый по 2 мл 0,1M HCl. Измерить pH систем после добавления кислоты.
Рассчитать в каждом отдельном случае буферную ёмкость по кислоте и основанию:
Bk= 
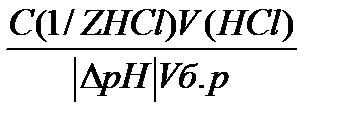 :
:
Bщ= 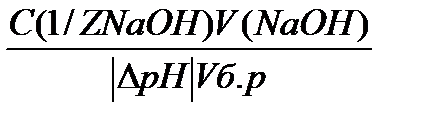
Полученные данные занести в таблицу 1 по образцу:
Таблица №1
| Буферное соотношение | Исходное значение pH | pH после добавления NaOH |  pH pH
| Bщ. | pH после добавления HCl |  pH pH
| Вк. |
| 0,1 | |||||||
| 0,01 |
Построить на основании полученных данных график зависимости буферной ёмкости по кислоте и основанию от соотношения количества соли и кислоты в буферной смеси. На ось абсцисс нанести логарифм соотношения соль/кислота, а на ось ординат –B. Ось ординат удобно проводить в пересечении с точкой абсциссы, где lg 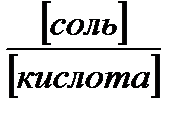 =0 и pH=pK.
=0 и pH=pK.
Кривые, относящиеся к буферной ёмкости по кислоте и основанию, начертить в цвете.
В отчете объяснить ход кривых зависимости буферной ёмкости по кислоте и основанию от соотношения количества соли и кислоты в системе и объяснить, почему ход кривых различный.
РАБОТА №3. ОПРЕДЕЛЕНИЕ БУФЕРНОЙ ЁМКОСТИ.
Опыт №1. Определение буферной ёмкости объемным методом.
В одну колбочку наливают 10 мл ацетатного буферного раствора с pH равным 5, в другую 10 мл 0,00001M раствора HCl, pH которого равен 5, и прибавляют по 3 капли индикатора метилового красного. Затем растворы осторожно титруют 0,1 М раствором NaOH (или KOH) до момента появления лимонно-желтой окраски(pH=6,3), и вычисляют буферную ёмкость по известной нам формуле (см. выше).
Date: 2015-09-17; view: 758; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |