
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Диаграммы плавкости
Диаграммы состояния 2-х компонентных систем с твердыми фазами получают экспериментально методами термического анализа и называют диаграммами плавкости.
Термический анализ – частный случай физико-химического анализа, разработанного Н.С.Курнаковым. В основе термического анализа лежит наблюдение за скоростью охлаждения (нагревания) расплавленных чистых веществ и расплавов различного состава, а также построение кривых охлаждения (нагревания) в координатах температура-время.
Для 2-х компонентной системы правило фаз Гиббса запишется:
С=2–Ф+2=4–Ф, т.е. максимальное число фаз, которое может находиться в равновесии равно 4.
Часто состояние 2-х компонентных систем изучают при Т или P=const. В этом случае правило фаз С=2–Ф+1=3–Ф, а диаграмма, построенная в координатах t-состав или давление-состав, будет плоской.
Рассмотрим простейшие виды диаграмм плавкости с неограниченной растворимостью в жидком состоянии.
Диаграмма плавкости систем с полной нерастворимостью компонентов в твердом состоянии эвтектического типа (рис.3).
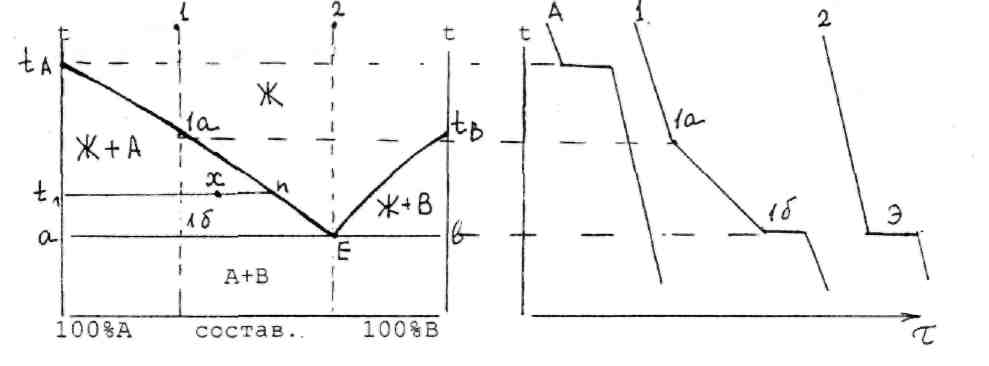
Рис. 3 Рис. 4
Кривые taE и tвE (рис.3) – образуют линию ликвидус (с лат. жидкость). Выше этих кривых сплавы находятся в жидком состоянии. Точка Е – эвтектическая точка. Линия ав соответствует эвтектической температуре, ее называют солидус (лат. - твердый), ниже этой линии сплавы находятся в твердом состоянии.
Линии ликвидуса и солидуса делят диаграмму на несколько полей:
(Ж) - ненасыщенный расплав компонентов А и В;
(Ж+А) - расплав компонентов А и В и кристаллы А;
(Ж+В) - расплав компонентов А и В и кристаллы В;
(А+В) - кристаллы А и В;
Определим вариантность системы на каждом участке диаграммы:
(Ж): С = 2-1+1 = 2, система бивариантна, т.е. можно изменять температуру и состав без изменения числа и вида фаз.
(Ж+А) и (Ж+В): С = 2-2+1 = 1, система моновариантна, т.е. каждой температуре соответствует определенный состав ненасыщенного расплава.
(А+В): С = 2-2+1 = 1,также каждой температуре соответствует определенный состав системы.
В точке Е в равновесии находятся 3 фазы.
Ж(Е) <=> А + В (эвтектическое равновесие).
С = 2-3+1 = 0, система нонвариантна (безвариантна), т.е. расплав, находящийся в равновесии с кристаллами обоих компонентов имеет строго определенный состав и температуру.
Диаграммы плавкости строят по кривым охлаждения (нагревания) (рис.4). Кривые охлаждения чистых компонентов А и В имеют горизонтальные участки при температурах их кристаллизации. На кривых охлаждения остальных сплавов, кроме эвтектического, наблюдается излом при температурах выпадения первых кристалов соответствующего компонента, а затем, при эвтектической температуре - горизонтальный участок.
Соотношение масс равновесных фаз можно определить, используя правило рычага: отношение масс равновесных фаз обратно пропорционально отношению отрезков, отсекаемых на изотерме точкой, характеризующей общий состав смеси.
Например точка х (рис.3) разбивает изотерму t1n на отрезки t1x и хn, поэтому:
масса расплава/масса кристаллов = xn/xt1
Date: 2015-09-17; view: 1619; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |