
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

А. Изобарный процесс
1. По определению процесса
p=const (6.10)
Используя уравнение Клапейрона 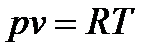 , уравнение процесса можно еще представить в виде
, уравнение процесса можно еще представить в виде 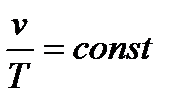 .
.
2. На основании последнего выражения  .
.
3. Пользуясь уравнением процесса p=const, по формуле 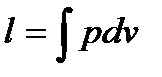 получаем:
получаем:
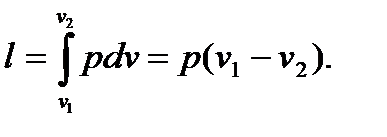 (6.11)
(6.11)
Это выражение можно преобразовать на основе уравнения Клапейрона 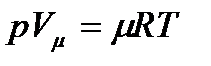 к виду
к виду 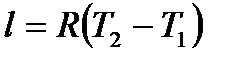 . Отсюда вытекает механическая трактовка газовой постоянной: она численно равна удельной работе изменения объема при изобарном нагревании газа на 1 град.
. Отсюда вытекает механическая трактовка газовой постоянной: она численно равна удельной работе изменения объема при изобарном нагревании газа на 1 град.
Из (6.10) следует dp=0, так что техническая работа изобарного процесса, 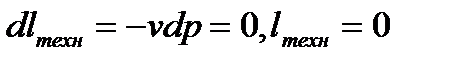 . Выясним смысл этого обстоятельства. При изобарном процессе изменение потенциальной энергии давления внешней среды равно
. Выясним смысл этого обстоятельства. При изобарном процессе изменение потенциальной энергии давления внешней среды равно
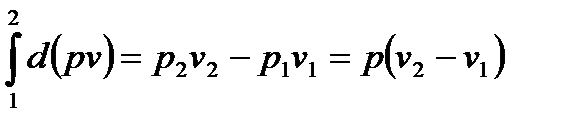 , т.к. p2=p1=p.
, т.к. p2=p1=p.
Как видим, работа изменения объема в точности равна работе проталкивания, поэтому в данном процессе никакой полезной работы не совершается.
4. Теплоемкость изобарного процесса обычно определяется по справочным данным. Формулы для количества теплоты процесса являются следствием формул 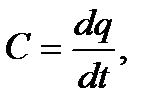 (6.1) и
(6.1) и  (6.2):
(6.2):
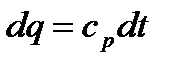 ;
; 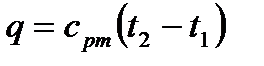 (6.12)
(6.12)
Из уравнения 1-го закона термодинамики в форме 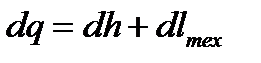 при
при 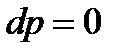 вытекает:
вытекает:
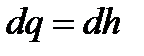 ;
; 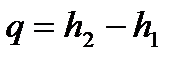 . (6.13)
. (6.13)
Формула (6.13) справедлива не только для идеального газа, но и для любых других веществ, так как она получена из общего выражения первого закона.
5. Используя определение дифференциала энтропии 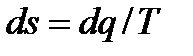 и подставляя вместо dq первое из выражений (6.11), получим
и подставляя вместо dq первое из выражений (6.11), получим  . Чтобы найти изменение энтропии в конечном изобарном процессе, нужно проинтегрировать последнее уравнение. При этом, если истинная изобарная теплоемкость не зависит от температуры (cp=const), то получится
. Чтобы найти изменение энтропии в конечном изобарном процессе, нужно проинтегрировать последнее уравнение. При этом, если истинная изобарная теплоемкость не зависит от температуры (cp=const), то получится
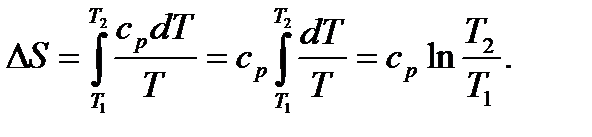
В большинстве случаев зависимость cp от температуры должна учитываться, поэтому формула для изменения энтропии будет иметь вид
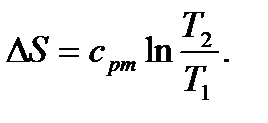 (6.14)
(6.14)
6. Из самого определения процесса p=const следует, что в pv - диаграмме изобарный процесс представляет собой отрезок горизонтальной прямой (рис. 6.1). Вид процесса в Ts -диаграмме легко установить на основе формулы (6.14). Перепишем эту формулу, полагая T1 и S1 фиксированными, а T2 и S2 - переменными: 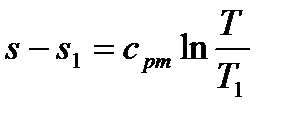 .
.
Отсюда видно, что изобара в Ts - диаграмме представляет собой логарифмическую кривую (см. рис. 6.1). Установим соответствие между направлениями процесса в обеих диаграммах. По закону Гей-Люссака, увеличению объема при изобарном процессе соответствует увеличение температуры. Следовательно, направлению изобары в pv - диаграмме вправо соответствует направление в Ts - диаграмме также вправо. На рис. 6.1 соответствующие точки в диаграммах обозначены одинаковыми цифрами. Из Ts -диаграммы следует, что при dq>0 dT>0, так что теплоемкость изобарного процесса есть величина положительная.

Рис. 6.1. Изображение изобарного процесса.
7. Изобарные процессы с газами чрезвычайно широко распространены в технике. Так, процесс нагревания или охлаждения протекающего газа в любом теплообменном аппарате является изобарным. Примерами таких теплообменных аппаратов являются воздухоподогреватели доменных и мартеновских печей, котельные установки, калориферы и т.д. Изобарный процесс также является составной частью цикла ДВС Дизеля.
Date: 2015-09-18; view: 952; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |