
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Форми відображення результатів хімічних аналізів
Хімічний склад підземних вод установлюється за даними хімічних аналізів. Раніше результати усіх аналізів виражалися в окисно-ангідридній і сольовій формах. У першому випадку компоненти, які містяться у воді, виражаються таким чином: метали в окисній формі (Nа2O, K2О, CaО, MgО та ін.), а металоїди – в ангідридній (SO2, CO2, N2O5, N2O3 – ангідриди відповідних кисневих кислот). Сольова форма передбачала вираження результатів аналізу води у вигляді молекул солей, одержаних при комбінуванні катіонів та аніонів (Na2SO4, MgCl2, CaCO3 та ін.).
Головною формою існування більшості компонентів в підземних водах є іони, тому й перейшли до іонної форми виразу результатів хімічних аналізів.
При цьому вміст того або іншого іона виражають в прісних або слабомінералізованих водах у міліграмах на дециметр куб. (мг/дм3) або грамах на дециметр куб. (г/дм). Для мінеральних і високомінералізованих підземних вод, питома вага котрих набагато більша одиниці, - в міліграмах або грамах на один кг води. Іонна форма виразу аналізу відповідає дійсному стану речовини у водних розчинах і відповідає дійсній можливості аналітично визначати саме іони, а не солі або окисли і ангідриди.
Проте лише перелік вмісту у воді іонів та їх вагової кількості ще не дають ясного уявлення про взаємозв'язок окремих іонів між собою. Відомо, що іони реагують один з одним у суворе визначених еквівалентних кількостях. Тому результати аналізу можна надавати і в еквівалентній формі, що дає можливість установити співвідношення між іонами. Для цього вагову іонну форму перераховують у еквівалентну. Цей перерахунок здійснюється шляхом ділення вагового вмісту іона в одному дециметрі куб. води на його еквівалентну вагу. Еквівалентна вага — це атомна вага елемента, поділена на його валентність. Атомна вага головних макрокомпонентів така: кальцій - 40,08; магній - 24,32; натрій - 22,997; хлор - 35,457; сірка - 32,066; кисень - 16,0.
Наприклад, 460 мг/дм3 натрію відповідає 460/(23:1) = 20 мг·екв.
Можна також вирахувати кількість іона у міліграмах - еквівалентах, помноживши його вагу в міліграмах на дм3 на коефіцієнт, протилежний еквівалентній вазі, тобто у даному прикладі будемо мати
460-(1:23) = 460-0,0435 = 20 мг·екв.
Для скорішого переходу до міліграмів-еквівалентів існують "Таблиці та номограми для рахування результатів гідрохімічних аналізів".
Тільки за вмістом будь-яких іонів (наприклад гідрокарбонату і кальцію), вираженому в міліграмах на дм3 (наприклад відповідно 554 і 181), не можна судити про те, який з них знаходиться у надлишку з точки зору утворення солі. Для цього треба перерахувати міліграми на дм в міліграм-еквіваленти. У даному прикладі 554 мг/дм3 гідрокарбонату відповідає 9,05 мг·екв (554:61 = 9,05) і 181 мг/дм" кальцію також дорівнює 9,05 мг·екв (181:20.04 = 9,05). Таким чином, іони гідрокарбонату і кальцію знаходяться у розчині в еквівалентних кількостях.
Для висновку про хімічний склад води і для порівняння води різної мінералізації, крім переліку іонів і виразу їх у ваговій і еквівалентній формах, необхідно мати уявлення про долю участі кожного з них у загальній кількості розчинених у воді речовин. З цією метою аналізи перераховуються у відсотково-еквівалентну (%-екв) форму. Тобто установлюють відносний вміст іонів, виражений у відсотках-еквівалентах від загальної суми іонів у даній воді.
Відомо, що б кожному водному розчині кількість еквівалентів катіонів дорівнює кількості еквівалентів аніонів, так як електроліти дисоціюють у водних розчинах на еквівалентну кількість тих і інших. Розчин при цьому є електронейтральним. Звичайно суму еквівалентів аніонів і суму еквівалентів катіонів приймають відповідно за сто відсотків і кількість знаходжуваного іона визначається із пропорції
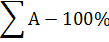
Ашук. – х% (1.1.1)
х = 
Для знаходжуваного катіона будемо мати
х =  (1.1.2)
(1.1.2)
Еквівалентна форма виразу даних хімічного аналізу дозволяє вирішити цілий ряд практичних завдань.
1. Користуючись даними аналізу, вираженими в еквівалентній формі, можна визначити вміст недостатнього у цьому аналізі іона. Так, розрахунковим шляхом часто знаходять такі надто працемісткі для визначення компоненти, як натрій і калій.
Припустимо, що досліджувана вода має хімічний склад, наведений у таблиці.
У цьому випадку натрій і калій можна визначити за різницею сум еквівалентів аніонів і відшуканих катіонів, тобто кількість міліграм-еквівалентів натрію і калію буде рівнятися 9,76 – (4,42+2,01) = 3,33. Потім їх можна перерахувати в міліграмах на дм3 і відсотках-еквівалентах, що й зроблено при заповненні таблиці.
2. Еквівалентна форма вираження результатів аналізу має особливо важливе значення з точки зору його контролю. Сума міліграмів-еквівалентів аніонів повинна дорівнювати сумі міліграмів-еквівалентів катіонів. Якщо цього немає, то очевидно, що при аналізі не визначені якісь іони або припущені помилки в кількісному їх визначені.
Таблиця 1.1.1 – Хімічний склад підземних вод
| Іони | Вміст іонів | ||
| мг/дм'3 | мг·екв | %-екв | |
| Катіони | |||
| №+ + К+ Mg2+ Ca2+ | 76,6 24,4 88,6 | 3,33 2,01 4,42 | 34,1 20,6 45,3 |
| Разом | 9,76 | ||
| Аніони | |||
| Cl- SO42- HCO3- | 124,5 83,0 276,3 | 3,51 1,73 4,52 | 36,0 17,7 46,3 |
| Разом | 673,4 | 9,76 |
3. За допомогою еквівалентної форми виразу аналізу, перерахованої у відсотково-еквівалентну, класифікують підземні води, тобто визначають їх хімічний тип. При цьому назву воді дають за компонентами, які містяться у розчині у кількості більше 25%-екв.
Назву води починають з аніонів у завершують катіонами. Існують два способи назв хімічного типу води: старий та новий.
Date: 2015-09-02; view: 530; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |