
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Построение карт рестрикции
Ферменты рестрикции стали эффективным инструментом исследования. Они позволяют превращать молекулы ДНК очень большого размера в набор фрагментов длиной от нескольких сотен до нескольких тысяч оснований. С помощью метода электрофореза в агарозном геле (см. раздел 1) фрагменты ДНК, различающиеся по размеру, можно легко разделить, а затем исследовать каждый фрагмент отдельно.
Короткие фрагменты мигрируют намного быстрее, чем длинные. При сравнительно высокой концентрации агарозы большие фрагменты вообще не могут проникнуть в гель. В процессе миграции рестрикционные фрагменты не деградируют, их можно элюировать (вымывать) в виде биологически активных двуцепочечных молекул. При окрашивании гелей красителями, связывающимися с ДНК, выявляется набор полос, каждая из которых отвечает рестрикционному фрагменту, молекулярную массу которого можно определить, проведя калибровку с помощью ДНК с известными молекулярными массами.
Сравнение размеров фрагментов ДНК, полученных после обработки определенного участка генома набором рестрицирующих нуклеаз позволяет построить рестрикционную карту, на которой указано положение каждого сайта рестрикции относительно других участков.
Молекулу ДНК длиной 5000 пар нуклеотидов (п. н.). обрабатывают отдельно рестриктазами А и В. Фрагменты разделяют электрофорезом. Фермент А разрезал ДНК на 4 фрагмента размером 2100, 1400, 1000 и 500 п. н. Обработка рестриктазой В дала 3 фрагмента: 2500, 1300 и 1200 п. н. (рис. 37). Для определения расположения сайтов рестрикции этих ферментов на следующем этапе применяют процедуру двойного расщепления – обрабатывают ДНК двумя эндонуклеазами. Обработка изучаемого фрагмента одновременно двумя рестриктазами дала 6 фрагментов: 1900, 1000, 800, 600, 500, 200 п. н.
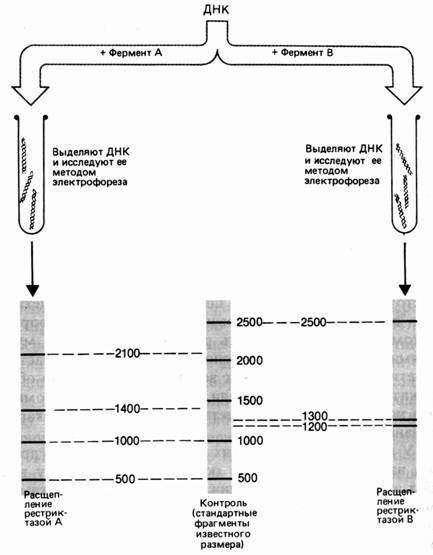
Рис. 37. Результаты электрофореза после обработки фрагмента ДНК разными рестриктазами
Наиболее полный вариант – элюировать каждый фрагмент, образующийся в результате расщепления одной рестриктазой, а затем обработать его второй. Смесь фрагментов, полученных после такой обработки, также анализируют с помощью электрофореза. В нашем примере были получены следующие результаты:
Обработка каждого из 4-х А-фрагментов рестриктазой В
2100 - 1900 и 200,
1400 - 800 и 600,
1000 - 1000 (изменений нет)
500 - 500 (изменений нет)
Обработка каждого из 3-х В-фрагментов рестриктазой А
2500 - 1900 и 600
1300 - 800 и 500
1200 - 1000 и 200
Анализ полученных результатов показывает, что каждый из ферментов, полученный при расщеплении А-фрагментов рестриктазой В можно обнаружить в образцах, полученных при расщеплении В-фрагментов рестриктазой А. Ключом к рестрикционному картированию являются перекрывающиеся фрагменты. Такими в рассматриваемом примере являются В-фрагмент 2100 и А-фрагмент 2500. При обработке другой рестриктазой они дают фрагмент 1900.
Из данных о расщеплении этих фрагментов мы предполагаем, что с одной стороны на расстоянии 200 п. н. от фрагмента 1900 находится следующий А-сайт, а с другого конца, на расстоянии 600 п. н. – следующий В-сайт (рис. 38). При обработке двумя эндонуклеазами фрагмент 200 п. н. образуется 1 раз, при обработке рестриктазой А из В-фрагмента 1200, т. е. фрагмент 1200 лежит слева. Остается определить, как продолжается карта вправо. Очевидно, это А-фрагмент 1400, так как он рассечен рестриктазой В на фрагменты 600 и 800. Вправо от фрагмента 2500 следует отложить, очевидно, фрагмент 1300. Тогда логично наличие А-фрагмента 500 и деления В-фрагмента 1300 рестриктазой А на 800 и 500.
При построении рестрикционных карт обычно используют несколько рестриктаз, поэтому приходится анализировать сложные соотношения между фрагментами, полученными при действии разных ферментов. Для упрощения процедуры картирования можно применять неполное расщепление. В определенных условиях рестриктаза узнает и расщепляет не все сайты в молекуле ДНК. Например, при частичном расщеплении ДНК ферментом А могут образовываться фрагменты 3100 п. н., 1400 п. н. и 500 п. н. Сопоставив их с данными полного расщепления (2100, 1400, 1000 и 500), можно сразу поставить рядом 2100 и 1000 (фрагмент 3100). А получив фрагмент 3500 – расположить рядом 2100 п. н. и 1400 п. н.

Рис. 38. Анализ фрагментов рестрикции и карта фрагмента ДНК
Другой прием – введение радиоактивной концевой метки. Концевые фрагменты определяются в этом случае по включению метки. Можно также сопоставить фрагменты путем гибридизации нуклеиновых кислот. Перекрывающиеся фрагменты (в данном случае 2100 и 2500) будут гибридизоваться.
Первая карта была получена для вируса SV40 (обезьяний вирус, вызывающий злокачественную трансформацию), содержащего 5423 пары оснований. Использовали рестриктазу Hind-II, расщепляющую кольцевую ДНК вируса на 11 фрагментов. Порядок их расположения в ДНК был установлен путем исследования наборов фрагментов, образующихся по мере того, как расщепление доходит до конца. Первый разрыв превращал кольцевую молекулу в линейную, которая затем расщеплялась на все меньшие и меньшие фрагменты. Исследовали вначале наборы перекрывающихся фрагментов, а затем продукты полного расщепления. Таким образом была получена рестрикционная карта кольцевой вирусной ДНК, на которую были нанесены сайты расщепления рестриктазой. Повторив подобные эксперименты с другой рестриктазой можно получить более подробную карту, где отмечено много сайтов рестрикции.
Располагая такой информацией, можно идентифицировать на ДНК биологически важные участки. Поскольку рестрикционная карта отражает расположение определенной последовательности нуклеотидов в данном участке, сравнение таких карт для двух или более родственных генов позволяет оценить гомологию между ними. Анализируя рестрикционные карты, можно сравнивать определенные участки ДНК разных видов животных без определения их нуклеотидной последовательности. Таким образом, например, было установлено, что хромосомные участки, кодирующие цепи гемоглобина у человека, орангутанга и шимпанзе сохранились в практически неизменном виде в течение последних 5 - 10 млн. лет (с тех пор как виды дивергировали).
Метод рестрикционного картирования позволяет увидеть крупные генетические изменения, такие как делеции или инсерции. При этом происходит уменьшение или увеличение рестрикционных фрагментов, а также исчезновение или возникновение сайтов рестрикции.
Один из приемов картирования – фингерпринт («метод отпечатков пальцев» или DNA-fingerprint). Он подразумевает использование неупорядоченных и неполных наборов фрагментов, которые являются характеристикой генома, хотя описывает его не полностью.
48. Клонирование нуклеотидных
последовательностей.
Размер, сложность организации и изменчивость генома человека затрудняют анализ индивидуальных признаков и генов. Возможности такого анализа сильно возросли с развитием методов рекомбинации ДНК, позволяющих выделять небольшие фрагменты ДНК и синтезировать их в неограниченном количестве. Уже клонированы сотни генов, например гены, мутации которых вызывают муковисцидоз, синдром Марфана, аденоматозный полипоз толстой кишки,нейрофиброматоз, атрофическую миотонию, синдром ломкой Х-хромосомы, болезнь Гентингтона, семейный рак молочной железы типа 1, синдром Линча и многие другие.
Клонированные гены и кодируемые ими белки используют для изучения структуры и функции гена в норме и при патологии, как с исследовательскими целями, так и для диагностики, лечения и консультирования.
Клонирование заключается в выделении фрагментов ДНК, встраивании их в нуклеиновую кислоту из другого организма (так называемый вектор), что позволяет получить множество копий каждого фрагмента. В вектор можно встроить фрагмент ДНК размером от десятков до сотен тысяч нуклеотидов. Методы клонирования ДНК описаны в работе Watson J.D. et al., 1992. (см." Генетика и болезни: литература ").
С помощью обратной транскриптазы на матрице мРНК можно синтезировать кДНК, пригодную для клонирования и анализа. Клоны кДНК (в отличие от клонов геномной ДНК) не содержат последовательностей, соответствующих интронам. Клоны геномной ДНК и кДНК выделены для сотен генов и для тысяч их фрагментов, а также для так называемых анонимных областей генома человека. Выполняющие неизвестную функцию анонимные области - это уникальные участки генома, часто содержащие полиморфные генетические маркеры. На основании полного или частичного определения нуклеотидной последовательности клонированной кДНК определяют аминокислотную последовательность белка и сравнивают с аминокислотными последовательностями известных белков.
В любой клонированный фрагмент можно ввести метку (радиоактивный изотоп, биотин и др.) и использовать его как специфический молекулярный зонд. Радиоактивные зонды выявляют с помощью радиоавтографии, а биотинилированные - с помощью меченого авидина.
Клонирование позволило получить зонды для анализа ДНК, для выявления мутаций, вызывающих заболевания, а также установить последовательность нуклеотидов в ДНК, зная которую можно определить аминокислотную последовательность в белке и приготовить праймеры дляамплификации ДНК с помощью ПЦР.
54. Молекулярные методы идентификации
Личности
Типирование ДНК – это молекулярно-генетическое исследование, основанное на изучении полиморфных локусов генома человека (микросателлитная и минисателлитная ДНК). У каждого человека совокупность таких полиморфных геномных локусов имеет свои характерные особенности, что позволяет применять этот метод для идентификации личности и установления родства.
Для подтверждения отцовства (материнства, родства) необходимо исследование как минимум 10-15 независимых локусов ДНК, с возрастанием числа исследуемых локусов ДНК увеличивается вероятность подтверждения отцовства. Максимальная вероятность подтверждения отцовства составляет 99, 99%.
Для исключения отцовства достаточно провести исследование 4-6 локусов ДНК, вероятность исключения составляет 100%.
Одним из важных применений метода исследования полиморфных локусов ДНК является отслеживание приживления стволовых кроветворных клеток донора у больного (реципиента) при трансплантации костного мозга. Явление сосуществования в организме реципиента собственных кроветворных клеток и кроветворных клеток донора носит называется химеризм. Перед трансплантацией у реципиента и донора проводится исследование 10-12 локусов ДНК и определяются такие локусы, по которым ДНК реципиента и донора различается, так называемые «метки». После трансплантации по таким геномным меткам можно отследить приживление костного мозга донора, при полном успешном приживлении костного мозга у реципиента исчезают его собственные характерные маркеры ДНК и остаются только характерные маркеры донора. Исследование химеризма проводится в течение 5 лет после трансплантации. Появление у реципиента через какой-то промежуток времени его собственных маркеров ДНК свидетельствует о возникновении рецидива заболевания. Таким молекулярно-генетическим методом рецидив можно выявить на ранней стадии, что позволит принять своевременные врачебные меры для предотвращения развития болезни.
56. Репарация повреждений ДНК
Репарация — особая функция клеток, заключающаяся в способности исправлять химические повреждения и разрывы в молекулахДНК, повреждённой при нормальном биосинтезе ДНК в клетке или в результате воздействия физических или химических агентов. Осуществляется специальными ферментными системами клетки. Ряд наследственных болезней (напр., пигментная ксеродерма) связан с нарушениями систем репарации.
Date: 2015-09-02; view: 925; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |