
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт. Получение и собирание кислорода. Доказательство наличия кислорода в сосуде
Задача. Вычисление массовой доли вещества, находящегося в растворе.
Рассчитайте массовую долю растворенного вещества, если при выпаривании 16 г воды было получено 4 г соли.
Для растворенного вещества формула расчета массовой доли будет иметь следующий вид:
ω = m растворенного вещества / m раствора, где ω — массовая доля,
m раствора = m растворенного вещества + m растворителя
Решение:
m растворенного вещества = 4г
m раствора = 16г (воды)+ 4г (соли)= 20 г
ω = 4г/20г = 0,2д.е. или 20%
Ответ: 0,2д.е. или 20%.
Билет № 3
Задача. Вычисление количества вещества одного из продуктов реакции, если известна масса исходного вещества.
Какое количество вещества водорода выделится при взаимодействии цинка с соляной кислотой массой 146 г? Решение:
Записываем уравнение реакции: Zn + 2HCl = ZnCl2 + H2↑
Находим молярную массу соляной кислоты: M (HCl) = 1 + 35,5 = 36,5 (г/моль)
Находим количество вещества соляной кислоты: ʋ(HCl) = m/M = 146 г / 36,5 г/моль = 4 моль
Записываем над уравнением реакции имеющиеся данные, а под уравнением — число моль согласно уравнению (равно коэффициенту перед веществом):
4 моль x моль
Zn + 2HCl = ZnCl2 + H2↑
2 моль 1 моль
Составляем пропорцию: 4 моль — x моль
2 моль — 1 моль
Находим искомое: x = 4 моль • 1 моль / 2 моль = 2 моль Ответ: 2 моль.
Билет № 4
Опыт. Получение и собирание кислорода. Доказательство наличия кислорода в сосуде.
Оборудование: лабораторный штатив с лапкой, штатив для пробирок, 2 пробирки, Г-образная газоотводная трубка, химический стакан, спиртовка, спички, лучинка, комочек ваты.
Реактивы: KMnO4 кристаллический, Н2О2(раствор), МnO2 .
Kислород – газ без цвета и запаха,поддерживает горение и дыхание. В лаборатории кислород получают разложением пероксида водорода в присутствии КАТАЛИЗАТОРА оксида марганца (IV): 2H2O2 = 2H2O + O2↑
или разложением перманганата калия при нагревании: 2 KMnO4 = K2MnO4 + MnO2 + O2↑
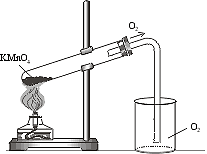 Чтобы собрать газ, в пробирку насыпают 1 см KMnO4. Сосуд закрывают пробкой с газоотводной трубкой, конец которой опускают в стакан, служащий для сбора газа.
Чтобы собрать газ, в пробирку насыпают 1 см KMnO4. Сосуд закрывают пробкой с газоотводной трубкой, конец которой опускают в стакан, служащий для сбора газа.
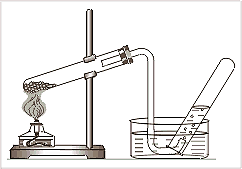 Кислород тяжелее воздуха, поэтому его собирают в сосуд, поставленный на дно.
Кислород тяжелее воздуха, поэтому его собирают в сосуд, поставленный на дно.
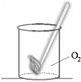 Kислород мало растворим в воде, поэтому его можно собирать и методом вытеснения воды из сосуда.
Kислород мало растворим в воде, поэтому его можно собирать и методом вытеснения воды из сосуда.
Чтобы доказать наличие кислорода в сосуде, вносят в него тлеющую лучинку —
она ярко вспыхивает. Кислород поддерживает горение.
В воздухе около 21% кислорода, поэтому лучинка только тлеет, а в чистом кислороде горит ярким пламенем.
Билет № 5
Date: 2015-08-24; view: 2641; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |