
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт 2. Окислительно-восстановительная
Двойственность нитрита калия
В две пробирки налью по 2-3 мл раствора нитрита калия KNO2. Добавлю в каждую из них по 1-2 мл разбавленной серной кислоты. Затем в одну из них прилью раствор дихромата калия K2Cr2O7, в другую – раствор иодида калия KI. Что наблюдается?
1.
· Уравнения реакций (I)
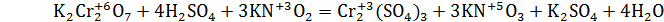
окислитель среда восстановитель
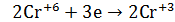 1 - окислитель
1 - окислитель
N+3 – 2e → N+5 3 - восстановитель
· Уравнения реакций (II)
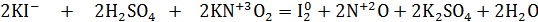
восстановитель среда окислитель
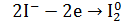 1 - восстановитель
1 - восстановитель
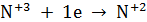 2 - окислитель
2 - окислитель
2. Вывод об окислительно-восстановительных функциях KNO2
Нитрит калия KNO2 содержит азот в степени окисления +3
· Реакция (I): N+3 → N+5 ⇒ KNO2 – восстановитель
· Реакция (II): 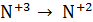 ⇒ KNO2 – окислитель
⇒ KNO2 – окислитель
3. Общий вывод: Вещества, которые содержат элемент в промежуточной степени окисления, в зависимости от условий проведения реакции может быть и окислителем, и восстановителем (в присутствии сильных окислителей проявляют восстановительные свойства, а при взаимодействии с активными восстановителями являются окислителями). Эти вещества могут проявлять окислительно-восстановительную двойственность.
Date: 2015-08-15; view: 7367; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |