
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры решения типовых задач
ПРИМЕР 1 Для реакции
2KBr + PbO2 + 4HNO3 = Pb(NO3)2 + Br2 + 2KNO3 + 2H2O
установить направление возможного протекания ее при стандартных условиях.
РЕШЕНИЕ. Запишем уравнение реакции в ионно-молекулярной форме:
2Br- + PbO2 + 4H+ = Pb2+ + Br2 + 2H2O.
Затем представим его в виде полуреакций, с указанием табличных значений ОВ-потенциалов:
2Br- - 2ē = Br2 E 0(Br2/Br-) = 1,065 В,
восстановитель
PbO2 + 4H+ + 2ē = Pb2+ + 4H2O E 0(Pb2+/PbO2) = 1,449 В
Окислитель
Потенциал окислителя Е 0ок больше, чем потенциал восстановителя Е 0восс, следовательно, приведенная реакция будет самопроизвольно протекать слева направо.
ПРИМЕР 2. Могут ли в стандартных условиях одновременно находиться в растворе хлориды двухвалентного олова и трехвалентного железа?
РЕШЕНИЕ. Представим данную систему в виде реакции
SnCl2 + FeCl3 = SnCl4 + FeCl2
Определим по таблице значения стандартных электродных потенциалов полуреакций.
Sn2+ - 2 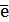 = Sn4+ Е 0восс = +0,151 В
= Sn4+ Е 0восс = +0,151 В
2 Fe3+ + 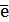 = Fe2+ Е 0ок = +0,771 В
= Fe2+ Е 0ок = +0,771 В
Sn2+ +2Fe3+ = Sn4+ + 2Fe2+
В данном примере Е ок > E восс, т.е. реакция в стандартных условиях будет протекать самопроизвольно в прямом направлении и, следовательно, указанные хлориды будут реагировать между собой, поэтому одновременное нахождение их в растворе невозможно.
ПРИМЕР 3. Рассчитать константу равновесия окислительно-восстановительной системы при стандартных условиях:
10Br- + 2MnO4- + 16H+ = 5Br2 + 2Mn2+ + 8H2O,
если E 0(Br2/Br-) = 1,065В; E 0(MnO4-/Mn2+) = 1,507В.
РЕШЕНИЕ. Представим данную реакцию в виде полурекций окисления и восстановления:
2Br- -2ē = 5Br2 Е 0восс = 1,065 В,
MnO4- + 8H+ + 5ē = Mn2+ + 4H2O, E 0ок = 1,507В
Константа равновесия К окислительно-восстановительной реакции с окислительно-восстановительными потенциалами связана следующим соотношением:
lg К = 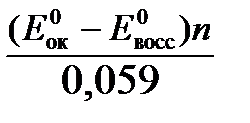 .
.
Окислителем в данной реакции является MnO4-, а восстановителем – Br-. В окислительно-восстановительном процессе участвуют 10 электронов. Отсюда:
lg K = 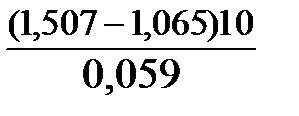 = 76,27,
= 76,27,
K = 1,86.1076.
ПРИМЕР 4. Рассчитайте равновесный потенциал электрода, на котором протекает реакция PbO2+ 4 H+ + 2ē ↔ Pb2+ + 2H2О, если 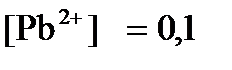 моль/л, а рН=5.
моль/л, а рН=5.
РЕШЕНИЕ. Потенциал окислительно-восстановительного электрода определяем по уравнению:
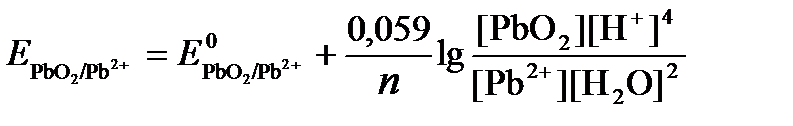 .
.
Концентрация 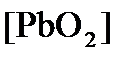 (как твердого вещества) и
(как твердого вещества) и 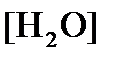 принимаются постоянными и включены в
принимаются постоянными и включены в 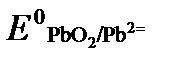 =+1,449 В, n =2 –число электронов. С учетом этого,
=+1,449 В, n =2 –число электронов. С учетом этого,
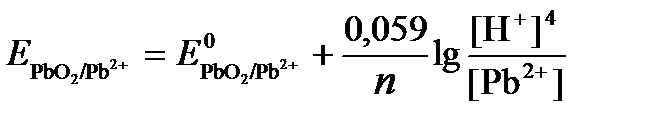
Исходя из того, что рН =-lg[H+] или [H+]= 10-рН, данное уравнение принимает вид:
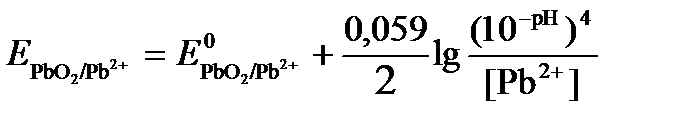
Подставляя значения Е 0 и концентраций ионов, получаем
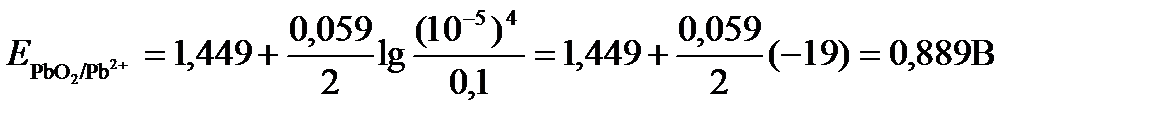
ПРИМЕР 5. Рассчитайте ЭДС окислительно-восстановительной системы
3Fe2+ + NO3- + 4H+ = NO + 3Fe3+ + 2H2O,
если [Fe2+]=10-3 моль/л, [Fe3+]=10-2 моль/л, [NO3-]=10-1 моль/л, а рН=3.
РЕШЕНИЕ. Выразим данную ОВ-систему в виде окислительно-восстановительных полурекций с указанием стандартных ОВ-потенциалов:
а) Fe2+ - ē →Fe3+ 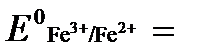 +0,771 В,
+0,771 В,
б) NO3- + 4H+ + 3ē → NO + 2H2O 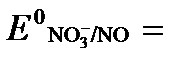 +0,960 В.
+0,960 В.
Для реакции (а) определим ОВ-потенциал по уравнению (3):
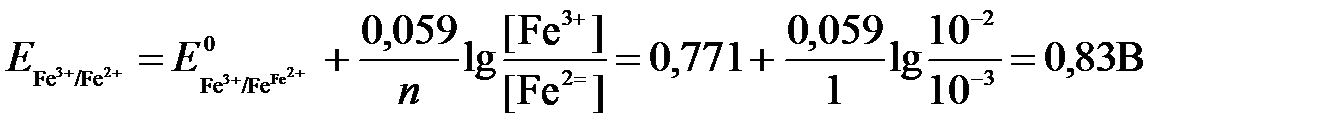
Для реакции (б) используем уравнение Нернста с учетом рН-среды:
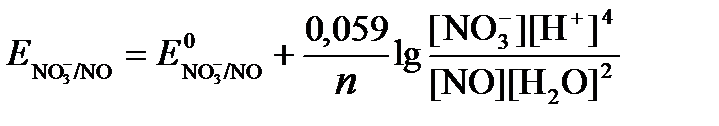 .
.
Имея ввиду, что активности [NO] и [H2O] являются постоянными и включены в значение Е 0, а [H+]=10-рН, рассчитаем ОВ-потенциал реакции (б) по уравнению:
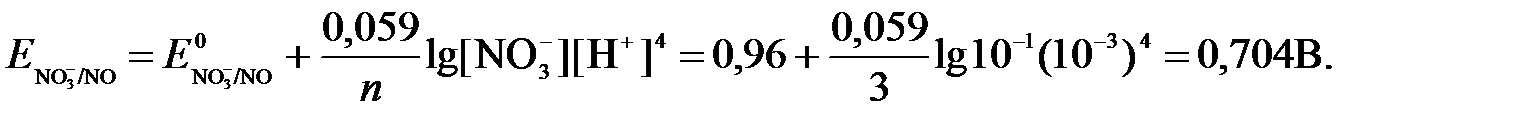
Затем рассчитаем ЭДС приведенной окислительно-восстановительной системы:
ЭДС= Δ Е = Е окс – Е восст= 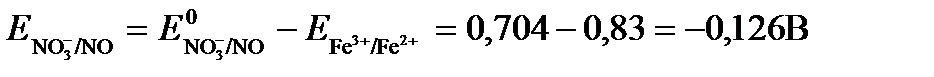
Так как Δ Е < 0, следовательно, реакция в прямом направлении протекать не может.
ПРИМЕР 6. Могут ли в стандартных условиях KClO3 и КBr одновременно находиться в щелочном растворе? Если нет, то укажите возможные продукты окисления и восстановления.
РЕШЕНИЕ. В бромиде калия КBr бром имеет низшую степень окисления -1 (Br-1), следовательно, он может проявлять только восстановительные свойства. В щелочной среде возможны следующие реакции окисления Br-1:
а) Br-1 + 6ОН- - 6ē = BrО3-1 + 3Н2О Е 0 = +0,61В
б) Br-1 + 2ОН- - 2ē = BrО-1 + Н2О Е 0 = +0,76В.
В ионе ClO3- хлор находится в промежуточной степени окисления +5. В случае совместного нахождения в растворе с восстановителем (КBr), KClO3 будет проявлять только окислительные свойства.
В щелочном растворе возможно восстановления ClO3- по реакции:
ClO3- + 3Н2О +6е = Cl- + 6ОН- Е 0 = +0,63В.
Сравнивая потенциалы окислителя и восстановителя, можно сделать вывод, что реакция окисления Br-1 по реакции (б) не может протекать, потому что Е ок < E восс. Окисление же Br-1 в присутствии KClO3 по реакция (а) возможно:
Br-1 + 6ОН- - 6ē = BrО3-1 + 3Н2О
+
ClO3- + 3Н2О +6ē = Cl- + 6ОН-
Br-1 + 6ОН- + ClO3- + 3Н2О = BrО3-1 + 3Н2О + Cl- + 6ОН-
KClO3 + КBr = КBrО3+ КCl
Таким образом, KClO3 и КBr одновременно находиться в щелочном растворе не могут, а вероятные продукты реакции - KCl и К BrО3.
ПРИМЕР 7. Может ли пероксид водорода H2O2 проявлять окислительные и восстановительные свойства? На основании стандартных электродных потенциалов привести примеры возможных реакций.
РЕШЕНИЕ. Пероксид водорода H2O2 имеет в своем составе кислород в промежуточной степени окисления (-1), поэтому он может проявлять как окислительные, так и восстановительные свойства.
Например, в кислой среде восстановление H2O2 протекает по реакции:
H2O2 + 2H+ + 2ē = 2H2O E 0 =1,776 B.
Окисление H2O2 протекает по реакции:
H2O2 -2ē = О2 + 2Н+ E 0 =0,682 B.
Чтобы в ОВ-реакции H2O2 проявлял окислительные свойства, надо по окислительно-восстановительным потенциалам выбрать восстановитель, у которого потенциал был меньше 1,776 В. Например, ион I- для которого:
2 I-1 - 2ē = I2 Е 0 = +0,536В.
Таким образом:
H2O2 + 2H+ + 2ē = 2H2O
2 I-1 - 2ē = I2
H2O2 + 2H+ + 2 I-1 = I2 + 2H2O.
Чтобы в ОВ-реакции H2O2 проявлял восстановительные свойства, надо по окислительно-восстановительным потенциалам выбрать окислитель, у которого потенциал был больше 0,682 В. Например, ион ClO3- для которого:
2ClO3- + 12H+ + 10е = Cl2 + 6 H2O Е 0 = +1,47В.
Таким образом:
H2O2 -2ē = О2 + 2Н+ 5
2ClO3- + 12H+ + 10ē = Cl2 + 6 H2O
5H2O2 -2ClO3- + 12H+ = 5О2 + 10Н+ + Cl2 + 6 H2O.
Сократив в правой части ионы водорода (Н+), получаем:
5H2O2 -2ClO3- + 2H+ = 5О2 + Cl2 + 6 H2O.
ПРИМЕР 8. Какой из металлов никель или кадмий легче взаимодействует с разбавленной HCl?
РЕШЕНИЕ. Запишим уравнения реакции взаимодействия этих металлов с HCl:
а) Ni + 2 HCl → NiCl2 + H2
Ni – 2ē = Ni2+ E 0 = -0,25 B
2Н+ + 2ē =Н2 Е 0 = 0,0В
б) Cd + 2 HCl → CdCl2 + H2
Cd – 2ē = Cd 2+ E 0 = -0,403 B
2Н+ + 2ē =Н2 Е 0 = 0,0В
Рассчитаем для обеих реакций изменение свободной энергии Гиббса по формуле
Δ G х.р. 0 = -nF (Е 0окс – Е 0восст).
Для реакции (а) Δ G х.р. = -2.96500.(0,0 + 0,25)= -48250 Дж.
Для реакции (б) Δ G х.р. = -2.96500.(0,0 + 0,403)= -77779 Дж.
Так как в реакции (б) убыль свободной энергии Гиббса больше, чем в реакции (а), следовательно, кадмий легче взаимодействует с HCl.
ПРИМЕР 9. На основании окислительно-восстановительных потенциалов реакций восстановления иона ClО3- определите, в какой среде, нейтральной или кислой, ClО3- проявляет более сильные окислительные свойства.
РЕШЕНИЕ. Представим возможные реакции восстановления иона ClО3- в нейтральной и кислой средах:
C1О3- + 3H2O + 6ē = Cl- + 6ОH- E 0 =0,63 B
2C1О3- + 12H+ +10ē = Cl2 + 6Н2О E 0 =1,47 B
Процесс протекает тем глубже, чем отрицательнее Δ Gхр. Из соотношения Δ G 0х.р = -nF (Е 0ок – E 0восс ) следует: чем выше потенциал окислителя, тем меньше Δ G 0 хр. В кислой среде ОВ-потенциал иона ClО3- больше, значит, в кислой среде он проявляет более сильные окислительные свойства.
Date: 2015-07-27; view: 462; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |