
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Пример 1. Стандартный электродный потенциал никеля больше, чем кобальта (табл
Стандартный электродный потенциал никеля больше, чем кобальта (табл. 8). Изменится ли это соотношение, если измерить потенциал никеля в растворе его ионов с концентрацией 0,001 моль/л, а потенциал кобальта — в растворе с концентрацией 0,1 моль/л?
Решение. Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Е = Е° + 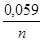 lg C
lg C
где Е° — стандартный электродный потенциал; n — число электронов, принимающих участие в процессе; С — концентрация (при точных вычислениях — активность) гидратированных ионов металла в растворе, моль/л; Е° для никеля и кобальта соответственно равны —0,25 и —0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях:
ENi2+/ Ni = 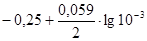 =-0,339 В,
=-0,339 В,
ECo2+/ Co =  =-0,307 В,
=-0,307 В,
Таким образом, при изменившейся концентрации потенциал кобальта стал больше потенциала никеля.
Таблица 7
Стандартные электродные потенциалы (Eo), некоторых металлов (ряд напряжений)
| Электрод | Eo, В | Электрод | Eo, В | |
| Li+/Li | -3,045 | Cd2+/Cd | -0,403 | |
| Rb+/Rb | -2,925 | Co2+/Co | -0,277 | |
| K+/K | -2,924 | Ni2+/Ni | -0,25 | |
| Cs+/Cs | -2,923 | Sn2+/Sn | -0,136 | |
| Ba2+/Ba | -2,90 | Pb2+/Pb | -0,127 | |
| Ca2+/Ca | -2,87 | Fe3+/Fe | -0,037 | |
| Na+/Na | -2,714 | 2H+/H2 | -0,000 | |
| Mg2+/Mg | -2,37 | Sb3+/Sb | +0,20 | |
| Al3+/Al | -1,70 | Bi3+/Bi | +0,215 | |
| Ti2+/Ti | -1,603 | Cu2+/Cu | +0,34 | |
| Zr4+/Zr | -1,58 | Cu+/Cu | +0,52 | |
| Mn2+/Mn | -1,18 | Hg22+/2Hg | +0,79 | |
| V2+/V | -1,18 | Ag+/Ag | +0,80 | |
| Cr2+/Cr | -0,913 | Hg2+/Hg | +0,85 | |
| Zn2+/Zn | -0,763 | Pt2+/Pt | +1,19 | |
| Cr+3/Cr | -0,74 | Au3+/Au | +1,50 | |
| Fe2+/Fe | -0,44 | Au+/Au | +1,70 |
Date: 2015-07-25; view: 4174; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |