
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Гемоглобин взрослых (гемоглобин А)
Представляет основную массу гемоглобина взрослых людей. С помощью электрофореза на крахмале установлено наличие нескольких фракций гемоглобина А:
- гемоглобин A1 (основная фракция, на долю которой приходится 96 - 98 % всей массы гемоглобина).
- гемоглобин A2 (2 - 5 %).
- гемоглобин A3 (содержание менее 1 %).Содержание гемоглобина F в крови взрослого человека составляет 1 - 2 %. Повышение этих величин возможно в условиях патологии.
Аномальные гемоглобины Гемоглобин S. В капиллярах при отдаче кислорода гемоглобин S выпадает в осадок в форме веретенообразных кристаллоидов, которые растягивают оболочку и ведут к распаду эритроцитов. Гетерозиготная форма аномалии протекает бессимптомно или сопровождается легкой гемолитической анемией. У гомозиготных особей уже с первых месяцев жизни развивается тяжелая форма серповидноклеточной анемии. Гемоглобин F Характерный для крови плода фетальный гемоглобин может быть обнаружен в повышенных количествах в эритроцитах крови недоношенных детей, при коклюше, серповидноклеточной анемии, талассемии, врожденной микроцитарной анемии, пернициозной анемии, острых и хронических лейкозах, миеломной болезни Гемоглобин С Наличие гена С в гомозиготном состоянии ведет к развитию выраженной спленомегалии, умеренной микроцитарной анемии с наличием эритроцитов мишеневидной формы. Гемоглобин У гомозиготов наблюдается микроцитоз, слабый анизо- и пойкилоцитоз и мишеневидность эритроцитов. Гемоглобин Е У гомозиготов ЕЕ наблюдается микроцитоз, компенсируемый развитием эритроцитоза. Миоглоби́н — кислород-связывающий белок скелетных мышц и мышцы сердца.Миоглобин отвечает за транспорт кислорода в скелетных мышцах и в мышце сердца.
5. Классификация сложных белков. Нуклеопротеины, структура, виды, биологическая роль. Строение мононуклеотидов, входящих в состав нуклеопротеинов.
Классификация сложных белков по строению простетической группы.
1. Гликопротеины. Простетические группы представлены углеводами и их производными связанными с белковой частью ковалентно-гликозидной связью через ОН-группы (серин, треонин) или NH-группу (лизин, аспарагин, глутамин).
Состав простетической группы гликопротеинов: моносахариды,олигосахариды;полисахариды (гомополисахариды, гетерополисахариды).
Функции гликопротеинов:рецепторы клеточных мембран;интерфероны; белки плазмы крови (кроме альбуминов);- иммуноглобулины;- групповые вещества крови;- фибриноген, протромбин;- гаптоглобин, трансферин;- церулоплазмин;- мембранные ферменты;
- гормоны (гонадотропин, кортикотропин).
2. Липопротеины — содержат липиды нескольких классов в качестве простетической группы, связаны с липидами и холестерином за счет различных нековалентнвых сил.
3. Фосфопротеины — сложные белки. Простетическая группа представлена фосфорной кислотой. Остатки фосфата соединяются с белковой частью молекулы сложноэфирными связями через гидрокси-группы аминокислот серина и треонина. Включают казеины — белки молока, вителлины — белки яичного желтка, овальбумин — белок куриного яйца..
4. Хромопротеины (ХП) — сложные белки, простетическая группа которых придает им окраску. Гемопротеины — простетическая группа, имеет геминовую структуру. Флавопротеины — простетическая группа — ФАД или ФМН.
5. Металлопротеины — содержат ионы одного или нескольких металлов, соединенных координационными связями с функциональными группами белка. Часто являются ферментами.Содержание металла в металлопротеинах: ферритин, трансферрин — Fe;
Нуклеопротеины – это сложные белки, содержащие в качестве небольшой части нуклеиновые кислоты состоят из 2-х частей: белковой (содержит гистоны и протамины, которые являясь основными белками, придают основные свойства) и простетической, представленной НК, сообщающими кислотные свойства. Взаимодействие между этими частями по ион-ионному механизму.
Все НП по составу НК можно разделить на 2 группы: рибонуклеопротеины (РНП) и дезоксирибонуклеопротеины (ДНП).
Состав НК:
НК – высокомолекулярные органические вещества, полинуклеотиды. Мономерами являются мононуклеотиды. Каждый мононуклеотид состоит из: углевода, азотистого основания и фосфорной кислоты. Так, РНК содержит (рибозу),(А, Г, Ц или У) и остаток фосфорной кислоты. ДНК содержит(дезоксирибозу), одно (А, Г, Ц или Т) и остаток фосфорной кислоты.
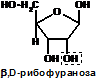
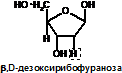
Строение азотистых оснований:
К группе пуриновых относятся аденин и гуанин К группе пиримидиновых – урацил тимин и цитозин


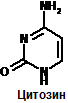
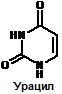
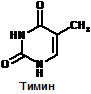
Структура нуклеиновых кислот:
1. первичная структура. РНК и ДНК построены однотипно – представлены полинуклеотидной цепью, состоящей из отдельных мононуклеотодов, соединённых между собой 3’→5’-фосфодиэфирными связями. Эта связь образуется между фосфорным остатком одного мононуклеотида и 3’-ОН-группой пентозного остатка другого мононуклеотида.
2. вторичная структура представляет собой двойную спираль, состоящую из 2 полинуклеотидных цепей, закрученных вокруг одной общей оси. Эти цепи антипараллельны, т.е. одна идет в направлении 5’→3’, а другая 3’→5’. Пуриновому основанию одной цепи соответствует пиримидиновое основание другой цепи – эти основания комплиментарны друг другу. Между А и Т две водородные связи (А=Т), а между Г и Ц – 3 (ГºЦ).
Молекула спирализована на всем протяжении, гидрофобные участки внутри спирали, их плоскости перпендикулярны основаниям и параллельны друг другу. В вертикальном направлении возникают гидрофобные взаимодействия. Вторичная структура стабилизируется водородными связями и гидрофобными взаимодействиями.
Вторичная структура РНК более простая, представляет собой одну полинуклеотидную цепь, в которой спирализованы лишь некоторые участки. Вторичная структура РНК представлена в виде клеверного листа. Для тРНК известна третичная структура в форме буквы Г
Биологическая роль НК:
ДНК – основная часть её локализуется в ядре в виде ДНк в составе хроматина или хромосом делящихся клеток. Главная роль – хранение генетической информации, участие в процессе транскрипции в качестве матрицы для построения молекулы РНК.
Все РНК по функции делятся на:
- рРНК (рибосомальные), Играют роль каркаса для объединения рибосом белков;
- мРНК (иРНК) – образуется в ядре (ядрышке). Переносит информацию из ядра в цитоплазму, является матрицей в процессе трансляции белка.последний кодон иРНК соответствует последней АК в белке;
- тРНК активирует аминокислоты и транспортирует их к месту биосинтеза белков, также участвует в трансляции. Имеет антикодоновый триплет – место, с помощью которого тРНК связывается с комплиментарным кодоном мРНК.
Date: 2015-07-22; view: 742; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |