
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Обмен жидкостью между сосудом и тканью определяется гидродинамическим давлением в сосуде и коллоидно-осмотическим давлением крови
В физиологических условиях в артериальном колене капилляра гидродинамическое давление превышает коллоидно-осмотическое давление крови и жидкость переходит в ткань. В венозном колене капилляра гидродинамическое давление становится ниже коллоидно-осмотического давления крови, и жидкость из ткани поступает в сосуд.
На участке воспаления гидродинамическое давление в сосудах возрастает, а коллоидно-осмотическое давление крови снижается вследствие увеличения проницаемости сосудистой стенки и выхода белков плазмы в ткань, а также воздействия ряда других факторов. В итоге в артериальном колене капилляра выход жидкости из сосуда в ткань резко возрастает, но и в венозном колене вместо резорбции наблюдается поступление жидкости из сосуда в ткань.
Существуют два пути прохождения веществ через стенку сосуда, которые сочетаются, дополняя друг друга.
Первый путь — межэндотелиальный: в норме, а особенно при воспалении, компоненты крови, в том числе ее форменные элементы, выходят из сосуда в ткань через межэндотелиальные щели. Этому предшествует сокращение эндотелиальных клеток, вследствие чего межклеточные щели расширяются, обнажая базальную мембрану.
Второй путь прохождения— трансэндотелиальный: в норме, а особенно при воспалении, в эндотелиальных клетках образуются направленные внутрь выпячивания плазмолеммы, в которых находится плазма. Таким образом образуются везикулы, которые передвигаются на противоположную сторону клетки. Здесь они раскрываются, освобождая содержимое. Пузырьки с той и другой стороны клетки могут сливаться, образуя каналы, по которым проходят различные вещества (микровезикулярный транспорт).
Возможна комбинация двух способов прохождения веществ через стенку сосуда. В зависимости от характера повреждающего агента, свойств макромолекул или частиц, а также особенностей сосуда может преобладать первый либо второй способ транспорта.
Наибольшее значение в повышении проницаемости стенок микрососудов в воспалительном очаге имеют медиаторы воспаления.
Характер веществ, выходящих из просвета сосуда во внесосудистую среду, зависит от степени повышения проницаемости стенок. Умеренное увеличение проницаемости приводит к выходу мелкодисперсных фракций белков, прежде всего альбуминов. При значительном увеличении проницаемости происходит выход глобулинов, а при еще более выраженном — фибриногена, который во внесосудистом русле образует сгустки фибрина. Тяжелые повреждения стенок микрососудов в виде фибриноидного некроза сопровождаются диапедезом эритроцитов и возникновением кровоизлияний. Часто наблюдается избирательная повышенная проницаемость для определенных веществ или клеток. В связи с этим выделяют различные формы экссудата и виды воспаления.
Из механизмов экссудации осмотический, онкотический и гидродинамический факторы воспалительного отека.
В ткани очага воспаления повышается осмотическое давление (гиперосмия), при этом осмотическое давление крови обычно не изменяется. Возникающий градиент осмотического давления крови и ткани является важным фактором усиления экссудации и развития отека. Гиперосмия тканей возникает в результате повышения в них концентрации осмоактивных частиц, ацидоза тканей.
В ткани очага воспаления повышается также и онкотическое давление (гиперонкия). Это происходит вследствие возрастания концентрации, дисперсности и гидрофильности белковых продуктов. В крови онкотическое давление, как правило, снижается (гипоонкия) в связи с нарушением функции печени и уменьшением образования альбуминов гепатоцитами, увеличением синтеза менее онкоактивных глобулинов.
Градиент онкотического давления ткани и плазмы крови — важный фактор усиления экссудации и развития отека.
В динамике развития острого воспаления мехамизмы экссудации и формирования воспалительного отека включаются не сразу, а в определенной последовательности:
1. Повышение проницаемости стенок микрососудов.
2. Усиление выхода жидкости с умеренным содержаниембелка (онкотическое и осмотическое давление ткани в очаге воспаления временно сохраняется неизменным).
3. В период тяжелых расстройств микроциркуляции и возникновения гипоксии развивается гиперосмия и гиперонкия ткани.
При различных формах воспаления в зависимости от характера и интенсивности действия повреждающего фактора, а также от локализации воспалительного процесса отмечаются особенности изменения проницаемости стенок сосудов. Выделяют немедленное — мимолетное, немедленное — продолжительное и отсроченное — пролонгированное увеличение проницаемости стенок микрососудов при воспалении.
Немедленное — мимолетноеувеличение проницаемости стенок микрососудов при воспалении обнаруживают при сравнительно слабом повреждении. В этом случае повышение проницаемости возникает практически сразу, достигает максимума в течение 5—10 мин и исчезает через 15—30 мин. Оно связано с высвобождением гистамина, серотонина и брадикинина. Немедленное — продолжительное увеличение проницаемости стенок микрососудов при воспалении обнаруживают при глубоком повреждении микрососудов. Резкое повышение проницаемости стенок микрососудов при этом возникает сразу после повреждения, нарастает в течение 1—5 ч и сохраняется 1—5сут. В результате патогенного воздействия гибнут эндотелиальные клетки сосудов всех уровней микроциркуляции, включая венулы, артериолы и капилляры. Процесс завершается либо репарацией сосудов, либо тяжелым тромбозом.. При этом происходит прямое повреждение микроциркуляторных сосудов фактором, вызывающим воспаление, с последующей плазмореей.
Отсроченное — пролонгированное увеличение проницаемости стенок микрососудов при воспалении характеризуется сравнительно продолжительным латентным периодом после повреждения с последующим быстрым увеличением проницаемости, продолжающимся несколько часов или дней. Такой тип ответа сосудов наиболее часто встречается в патологии: при легком и среднем по тяжести термическом повреждении, ионизирующем и ультрафиолетовом облучении, действии бактериальных токсинов, аллергии замедленного типа и др. В этих случаях характерного сокращения и округления эндотелиальных клеток не происходит, а нарушаются межэндотелиальные сцепления в капиллярах и венулах. Увеличение проницаемости при этом обусловлено прямым действием патогенных факторов.
В динамике воспаления не исключено также сочетание различных типов изменения проницаемости стенок сосудов.
Усиленная экссудация вызывает отек, боль — вследствие сдавления нервных окончаний и проводников, нарушения функции — в результате увеличения диффузионного расстояния от капилляров до паренхиматозных клеток, а также их сдавления. Она может усугублять расстройства микроциркуляции, вызывая чрезмернуюгемоконцентрацию, сладжирование эритроцитов и способствуя образованию тромбов. Вместе с тем увеличенная экссудация является, вероятно, одним из наиболее древних механизмов ослабления действия на организм агентов, вызывающих воспаление.
2.3. Эмиграция лейкоцитов.
Сосудистые изменения в очаге воспаления связаны с транформацией тока жидкой части крови и поведения ее форменных элементов. В воспалительном очаге обнаруживают шесть фаз изменения микроциркуляции и поведения клеток крови.
I. В начале развития пассивной гиперемии в венулах наблюдается расширение осевого цилиндра, но клетки крови временно сохраняют свое положение в центре сосуда.
II. Далее по мере замедления кровотока форменные элементы в осевом цилиндре перераспределяются, лейкоциты выходят на границу осевого цилиндра и плазматического слоя, а в дальнейшем подходят к стенке сосуда и начинают прикрепляться к ней.
III. При еще большем замедлении кровотока адгезия лейкоцитов нарастает и клетки образуют муфты вдоль стенок сосудов, нарушая ламинарность кровотока.
IV. Постепенно лейкоциты начинают проходить через стенку сосуда и эмигрировать в ткань.
V. Одновременно происходит выраженное набухание эндотелия, еще более нарушается ток крови в микрососудах, с помощью того же механизма эмиграции форменных элементов из сосудов выходят эритроциты, что свидетельствует о грубых нарушениях проницаемости стенок венул.
VI. По мере развития процесса на фоне толчкообразного движения крови или стаза разобщаются эндотелиальные клетки, нарушается целость стенок посткапилляров и венул, возникают тяжелые биохимические изменения крови и появляются микрокровоизлияния.
|
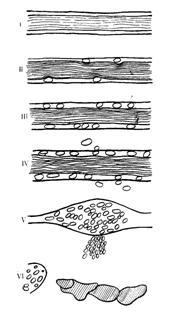
В период краевого стояния происходит два основных явления — выход лейкоцитов из осевого цилиндра к его краю и приклеивание (адгезия) их к стенке сосуда. Частицы с низким удельным весом, какими являются лейкоциты, в случае замедления тока жидкости относятся к стенке сосуда, а частицы с более высоким удельным весом (эритроциты) продолжают движение в центре сосуда. В застойном кровотоке эритроциты объединяются в «монетные столбики», которые занимают всю осевую часть сосуда, и лейкоциты оказываются в плазматическом слое.Для осуществления краевого стояния необходимы два условия: повышение адгезивных свойств эндотелиальных клеток и активированное состояние лейкоцита, направляющегося в определенное место стенки сосуда. Важное значение имеет устранение отрицательного заряда эндотелиальной клетки и лейкоцита, в нормальных условиях предупреждающего адгезию. Инициируют адгезию лейкоцитов к стенке сосуда также естественные факторы защиты (комплемент, фибронектин, иммуноглобулины) и медиаторы воспаления (гистамин, лейкотриены).
Комплемент обладает мощными хемоаттрактантными и адгезивными свойствами в отношении лейкоцитов в очаге воспаления. Связывание его с соответствующими рецепторами на мембране грануло- и агранулоцнтов определяет активацию комплемента и направленную хемоаттракцию к эндотелиальным клеткам сосудов.
Фибронектин имеет ряд активных центров (доменов), каждый из которых связывается с соответствующим лигандом - коллагеном, фибрином, некоторыми микроорганизмами, со специализированными рецепторами лейкоцитов. Фибронектин находится не только в плазме, но и на коллагеновых волокнах, и на мембране эндотелиальных клеток, осуществляя направленную аттракцию ПЯЛ и мононуклеаров крови.
Фагоциты, обладающие чувствительностью, воспринимают сигналы из окружающей среды и реагируют на них изменением своего состояния и движением в направлении этих сигналов.
В большинстве случаев острого воспаления первыми эмигрируют неитрофилы, доминирующее положение в эмиграции они занимают в первые 6—24 ч. Через 24—48 ч наибольшее значение в эмиграции приобретают моноциты. Одновременно или несколько позднее эмигрируют лимфоциты. Считают, что одним из наиболее важных механизмов, определяющих такую последовательность эмиграции, является высвобождение специфических для каждого вида лейкоцитов хемотаксических факторов. В частности, нейтрофилы в процессе активизации высвобождают хемотаксические факторы для моноцитов. Порядок эмиграции весьма вариабелен.
♦ Фагоцитоз.
Одним из важнейших факторов воспалительной реакции является фагоцитоз.
Фагоцитоз - это процесс поглощения и переваривания клеткой различных корпускулярных агентов (частиц), которые являются или становятся инородными для всего организма или для отдельных его частей.
ü При фагоцитозе происходит процесс поглощения и переваривания не только частиц, изначально являющихся чужеродными для организма но и тех, которые могут стать таковыми при определенных условиях. Например, микроорганизмы, составляющие нормальную микрофлору кишечника, при их попадании в ткани парэнтерально становятся объектами фагоцитоза.
ü Какой-то объект может не быть чужеродным для одной части организма и стать чужеродным для другой. Например, эритроциты в кровеносном русле для организма не чужеродны, но если, они попадут в ткани при кровоизлиянии, то становятся чужеродными и могут стать объектами фагоцитоза.
Внутриклеточному захвату и перевариванию могут подвергаться не только корпускулярные агенты, но и жидкие. Захват клетками капель жидкости и использование этих жидкостей в процессах внутриклеточного пищеварения - пиноцитоз.
Явление фагоцитоза было открыто в конце декабря 1882 г. И.И. Мечниковым, и в дальнейшем, в результате его работ на протяжении четверти века, было доказано, что фагоцитоз - это один из основных механизмов воспалительной реакции, поскольку он направлен на уничтожение се причинного фактора.
В фагоцитозе могут принимать участие разнообразные элементы ретикуло-эндотелиальной системы. В воспалительной реакции в качестве основной фагоцитирующей клетки выступают нейтрофильныеполиморфноядерные лейкоциты крови.
Строение лейкоцита.
Лейкоциты имеют клеточный скелет, в состав которого входят микротрубочки, актиновые, миозиновые и промежуточные филаменты - опорно-двигательный аппарат, элементы которого связаны с рецепторами, расположенными на поверхности мембраны, в связи с чем цитоскелет лейкоцита в значительной степени определяет и особенности реакции последнего на различные воздействующие на него раздражители. Клеточный скелет не представляет собой чего-то постоянного как структурно, так и функционально. Его элементы могут перегруппировываться в зависимости от конкретных условий процесса и требований, которые предъявляются лейкоциту этими условиями. Элементы цитоскелета могут менять свое физико-химическое состояние: основной принцип функционирования этого структурного комплекса - процесс обратимой деполимеризации входящих в него белков, регулируемый ионами кальция, кальцийсвязывающим белком-кальмодулином, а также внутриклеточным соотношением цАМФ и цГМФ. Этим определяются важнейшие функции лейкоцита: передвижение, захват чужеродных частиц, внутриклеточное переваривание. Дефекты клеточного скелета лейкоцитов делают их неполноценными, не способными эффективно участвовать в защите организма от факторов, вызывающих воспалительную реакцию.
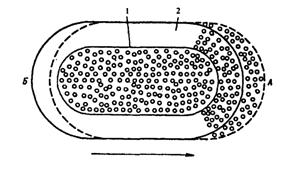
Рис. 6. Первый способ передвижения лейкоцита:
А — передний полюс лейкоцита; Б — задний полюс лейкоцита; 1 — центральная часть лейкоцита (золь); 2 — наружная часть лейкоцита (кортикальный гель). Стрелкой обозначено направление движения лейкоцита.
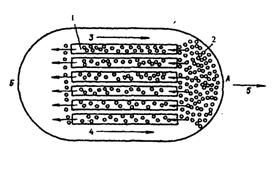
Рис. 7. Второй способ передвижения лейкоцита:
А — передний полюс лейкоцита; Б — задний полюс лейкоцита; 1 — микротрубочки цитоскелета; 2— разжиженная часть кортикального геля;
3, 4 — направление движения микротрубочек;
5 — направление движения лейкоцита.
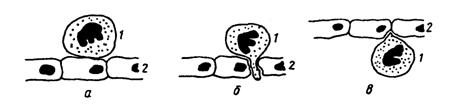
Рис. 8. Выход лейкоцита из сосудистого русла:
а — адгезия лейкоцита к сосудистому эндотелию; б — образование лейкоцитом псевдоподии, проходящей в межэндотелиальную щель; в — лейкоцит, вышедший за пределы сосуда; 1 — лейкоцит; 2— эндотелий.
Процесс фагоцитоза включает в себя пять стадий.
Первая стадия - адгезия, то есть прилипание лейкоцита к эндотелиальной клетке и прохождение его через стенку сосуда. На мембране лейкоцита располагаются высокомолекулярные протеины, которые при воспалении меняют свои свойства, благодаря чему лейкоцит может прилипнуть к сосудистому эндотелию. Затем у лейкоцита образуются псевдоподии, как у амебы. Такая псевдоподия проникает между эндотелиальными клетками и в нее переливается протоплазма лейкоцита, который таким образом оказывается по другую сторону эндотелиальной выстилки сосуда (рис. 8). Базальная мембрана сосуда лизируетсяколлагеназой лейкоцита, и он выходит из просвета сосуда в ткань. Часть лейкоцитов попадает затем в лимфатические сосуды и возвращается обратно в кровь, вновь выходит из кровеносного сосуда и вновь в него возвращается. Другая же часть лейкоцитов, выйдя из кровеносного сосуда, устремляется к очагу воспаления.
Вторая стадия - передвижение фагоцита к объекту фагоцитоза. Это передвижение начинается и поддерживается благодаря тому, что в очаге воспаления образуются вещества, к которым лейкоцит обладает положительным хемотаксисом, то есть при наличии этих веществ лейкоцит начинает двигаться в их сторону. Вещества, к которым лейкоцит проявляет положительный хемотаксис, воздействуют на рецепторы его оболочки, в результате чего возникает сенсорный эффект - лейкоцит начинает «чувствовать», «ощущать» эти вещества.
Лейкоциты обладают положительным хемотаксисом по отношению к целому ряду веществ, в частности, к различным полипептидам. Особо важное значение в контроле за хемотаксическим процессом имеют циклические нуклеотиды.цГМФ повышает чувствительность лейкоцитов к хемотаксическому фактору и усиливает их движение. Противоположным действием обладает цАМФ.
Вещества, к которым у лейкоцитов имеется положительный хемотаксис, меняют физико-химическое состояние их протоплазмы, переводя ее из состояния геля в состояние золя и обратно. Таким образом, какая-то часть протоплазмы лейкоцита становится жидкой и в нее постепенно переливается вся клетка.
Перемещение фагоцита в пространстве осуществляется следующим образом:
Протоплазма фагоцита состоит из центрального жидкого слоя (золя) и более плотного наружного - кортикального геля. Под влиянием веществ, к которым лейкоцит обладает положительным хемотаксисом, на переднем полюсе лейкоцита кортикальный гель превращается в золь, то есть становится более жидким. В эту «разжиженную» часть лейкоцита переливается золь его центральной части, в результате чего лейкоцит укорачивается сзади и удлиняется спереди (Рис. 6).
Существует и другой способ движения фагоцита (рис. 7). Микротрубочки цитоскелета в тот период, когда лейкоцит находится в спокойном состоянии, не имеют четкой ориентации, расположены хаотически и выполняют в основном опорную функцию. Когда же лейкоцит начинает двигаться, эти трубочки меняют свое расположение в цитоплазме и ориентируются точно по направлению движения. Разжиженная часть кортикального геля с переднего полюса лейкоцита засасывается в эти трубочки и с силой выбрасывается из них назад. Возникает реактивная тяга: сами трубочки начинают двигаться в противоположном направлении и толкают лейкоцит вперед (лейкоцит передвигается как ракета). Исходя из наличия в лейкоците актин-миозиновой системы, можно предположить, что в нем происходят процессы, аналогичные мышечному сокращению, благодаря чему он и передвигается. Скорость движения лейкоцитов может быть довольно большой. За сутки лейкоцит может пройти 5-6 см. Передвижение лейкоцитов является энергозависимым процессом, то есть идет с потреблением энергии, причем эту энергию лейкоцит получает от гликолитических реакций. Блокада процессов окислительного фосфорилирова-ния соединениями синильной кислоты не останавливает движения фагоцитов, в то время как монойодацетат, угнетая гликолиз, тормозит этот процесс.
Третья стадия - прилипание фагоцита к фагоцитируемому агенту (рис. 10). В механизмах этой стадии важную роль играют электрические заряды фагоцита и объекта, а также интенсивность процессов хемотаксиса.
Четвертая стадия - погружение объекта в фагоцит, которая может осуществляться двумя путями. Во-первых, фагоцит, подобно амебе, способен выпускать псевдоподии, которые смыкаются над объектом фагоцитоза, и он оказывается внутри фагоцита (рис. 9а). Во-вторых, это погружение может происходить путем инвагинации клеточной оболочки фагоцита (рис. 9б), в нем образуется все увеличивающаяся впадина, в которую и погружается объект. Затем края впадины смыкаются над объектом, и он оказывается внутри фагоцитирующей клетки. Если же объект по своим размерам очень большой, то он окружается несколькими фагоцитами, которые внедряют в него сливающиеся друг с другом цитоплазматические отростки, и таким путем осуществляется совместный фагоцитоз несколькими фагоцитами одного объекта.
В процессе погружения объекта в фагоцит важную роль играют электрические заряды объекта и фагоцита, интенсивность хемотаксиса и величина поверхностного натяжения в месте соприкосновения фагоцита и фагоцитируемого объекта. Чем ниже последний показатель, тем интенсивнее идет погружение. Такие антитела как опсонины и бактериотропины, снижающие поверхностное натяжение, способствуют интенсификации фагоцитирования микроорганизмов.
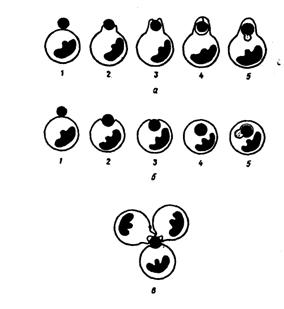
Рис. 9 Варианты погружения объекта в фагоцит:
а - образование фагоцитом псевдоподий, охватывающих объект и погружающих его внутрь клетки;
б - погружение объекта в фагоцит путем инвагинации мембраны последнего;
1, 2, 3, 4— отдельные моменты погружения;
5 - слияние объекта с пищеварительной вакуолью;
в - поглощение одного объекта тремя фагоцитами.
Рис. 10
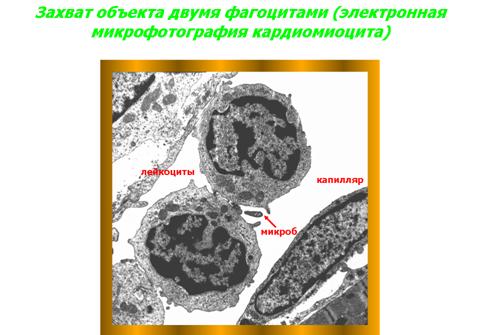
Пятая стадия – переваривание (рис. 11). Вначале живой объект, попавший в фагоцит и находящийся в его пищеварительной вакуоли, должен быть убит. Живые объекты фагоцит не переваривает. Основную роль в гибели живых объектов, попавших в фагоцит, играет резкий сдвиг рН протоплазмы фагоцита в кислую сторону. После того, как объект убит, пищеварительная вакуоль, в которой он находится, сливается с одной или несколькими лизосомами фагоцита, и лизосомные ферменты осуществляют процесс пищеварения в этой полости.
Рис. 11
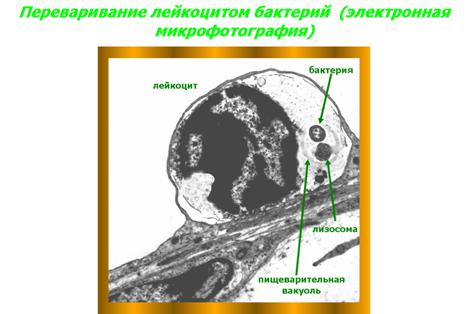
Живой объект может быть фагоцитирован и иным путем: в гранулах лейкоцита содержатся бактерицидные вещества, которые выбрасываются в окружающую среду, и, таким образом, лейкоцит убивает микроорганизм. Затем осуществляется процесс его погружения и переваривания.
Таковы процессы, лежащие в основе так называемого завершенного фагоцитоза. Однако фагоцитоз протекает по-иному, если микроорганизмы - объекты фагоцитоза, либо обладают мощной полисахаридной капсулой, защищающей их от кислой реакции среды, либо выделяют вещества, которые препятствуют слиянию лизосом с пищеварительной вакуолью, в результате чего процесс внутриклеточного пищеварения не может быть осуществлен. В этом случае имеет место так называемый незавершенный фагоцитоз. Он заканчивается тем, что через некоторое время либо живые микроорганизмы выбрасываются из фагоцита, либо фагоцит гибнет. Аналогичная ситуация может возникать при некоторых генетически обусловленных дефектах фагоцитарной системы.
2.4. Морфофункциональная характеристика клеток, появляющихся в очаге воспаления.

Date: 2015-07-22; view: 749; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |