
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Порядок реакции
l Если реакция сложная, то происходит ряд промежуточных превращений и порядок реакции равен порядку реакции лимитирующей стадии.
l В сложных реакциях порядок реакции не совпадает с ее молекулярностью.
l Молекулярность - это число одновременно сталкивающихся молекул.
Константа скорости реакции (удельная скорость реакции) — коэффициент пропорциональности в кинетическом уравнении.
Физический смысл константы скорости реакции k следует из уравнения закона действующих масс: k численно равна скорости реакции при концентрации каждого из реагирующих веществ равной 1 моль/л.
Константа скорости реакции зависит от температуры, от природы реагирующих веществ, но не зависит от их концентрации.
Конста́нта равнове́сия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия (в соответствии с законом действующих масс).
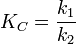
где k1 — константа скорости прямой реакции, а k2 — обратной. Это важное соотношение даёт одну из «точек соприкосновения» химической кинетики и химической термодинамики.
Простая или элементарная реакция протекает в одну стадию, без образования промежуточных веществ.
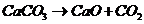 Мономолекулярная реакция – в элементарном акте участвует одна молекула (разложение)
Мономолекулярная реакция – в элементарном акте участвует одна молекула (разложение)
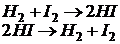 Бимолекулярная реакция -в элементарном акте участвуют 2 молекулы (столкновение двух молекул)
Бимолекулярная реакция -в элементарном акте участвуют 2 молекулы (столкновение двух молекул)
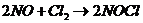 Трехмолекулярная реакция -в элементарном акте участвуют три молекулы, вероятность их столкновения мала
Трехмолекулярная реакция -в элементарном акте участвуют три молекулы, вероятность их столкновения мала
Сложные реакции протекают в несколько стадий с образованием промежуточных продуктов.
Date: 2015-07-22; view: 322; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |