
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Молекули і атоми
Розрізняємо атом і молекулу
З попереднього курсу «Природознавство» ви вже знаєте, що всі речовини складаються з дрібних частинок — молекул та атомів. Ви також знаєте, що первинні складові речовини — атоми — мають спеціальні назви та символи для позначення кожного з видів атомів. Наприклад: Гідроген (Н), Меркурій (Нg), Оксиген (О), Карбон (С). Атоми різних видів відрізняються один від одного своїми хімічними властивостями та масою. З фізичною величиною під назвою «маса» ви вже познайомилися в нашому курсі. Що таке «хімічні властивості», ви дізнаєтеся з курсу хімії.
Станом на 2005 рік науці відомі тільки 116 різних видів атомів. «Не може бути,— заперечите ви.— Як це, тільки 116? Кожний із нас із легкістю перелічить 200—300, а може, і більше різних речовин». Так, дійсно, у світі існують мільйони різних речовин. Як же поєднати існування тільки 116 видів атомів з мільйонами різних речовин? Річ у тім, що речовини здебільшого складаються з молекул.
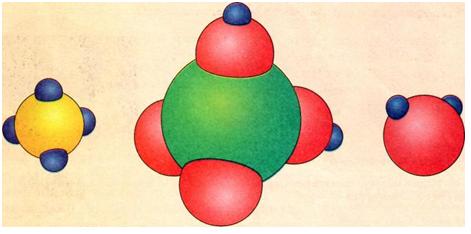
Рис. 2.11. Моделі молекул деяких речовин: а — метану (СН4); б — сірчаної кислоти (Н4S04); в — води (Н20). (Сині кульки — атоми Гідрогену, червоні — Оксигену, зелені — Сульфуру, жовті — Карбону.)
Молекулою називається найменша частинка речовини, що має її основні хімічні властивості та складається з атомів.
Ситуація з різними речовинами дуже подібна до складання тисяч різних слів із «тільки» 33-х літер абетки. У цьому порівнянні кожна літера — це, так би мовити, окремий атом, а кожне слово відповідає певній молекулі, тобто певній речовині.
На рис. 2.11, а ви бачите схематичне зображення молекули метану, яка складається з п'яти атомів: чотирьох атомів Гідрогену та одного атома Карбону. Користуючись нашою аналогією — це слово з п'яти літер. На рис. 2.11, б наведено схему більш складної молекули сірчаної кислоти, яка складається з семи атомів. Аналог цієї молекули — слово з семи літер. З наведених прикладів зрозуміло, що кожна нова молекула (нова комбінація атомів) відповідає новій речовині.
2. Знайомимося з простими та складними речовинами
Продовжимо нашу аналогію речовин зі словами. Ви знаєте, що поряд зі словами, які складаються з декількох різних літер, ми іноді вимовляємо і слова з використанням тільки однієї літери (наприклад, «я», «аа...», «ууу...»). Так само і з речовинами. Декілька з них складаються тільки з одного виду атомів (одного хімічного елемента) і тому називаються простими (див. рис. 2.12). Прикладами таких речовин є вуглець, залізо та ін.
Z12.jpg
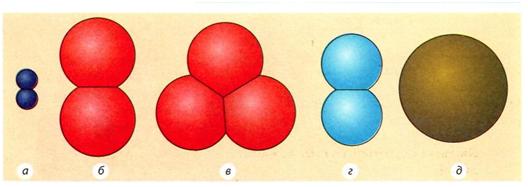
Рис. 2.12. Моделі молекул простих речовин: а — водню (Н2); б— кисню (02); в — озону (03); г — азоту (N2); д — заліза (Fе)
Цілком очевидно, що слів, які складаються з декількох літер, набагато більше, ніж слів з однієї літери. Так само і з речовинами. Найчастіше в повсякденному житті ми маємо справу з речовинами, які складаються з атомів декількох різних сортів. Ці речовини так і називаються — складні (див. рис. 2.11).
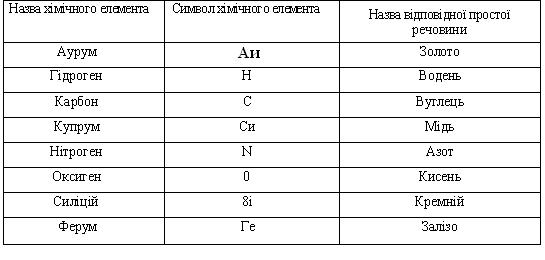
Нагадаємо, що в науковій літературі, щоб уникнути плутанини, застосовують різні назви для простих речовин і для хімічних елементів, із яких ці речовини складаються. Приклади назв простих речовин та відповідних хімічних елементів наведено в таблиці.
3. Переконуємося в наявності проміжків між молекулами
Після того як ми познайомилися з найменшими частинками речовини, пригадаймо деякі відомості про будову речовини. У результаті досліджень учені з'ясували, що між молекулами (атомами) існують проміжки. Цей висновок учених можна легко підтвердити досить простим дослідом. Якщо змішати 100 мл води і 100 мл спирту, то об'єм суміші буде меншим, ніж 200 мл. Після змішування двох рідин молекули води потрапляють у проміжки між молекулами спирту. Наведений дослід можна змоделювати, наприклад, за допомогою пшона і гороху (рис. 2.13). Наповніть склянку до половини пшоном, а потім додайте стільки ж гороху. Ви одержите двошарову композицію та до краю заповнену склянку. Акуратно перемішайте цю композицію, і ви побачите, що об'єм суміші буде меншим, ніж вихідний,— частина пшона розмістилась у порожнинах між горохом.

Рис. 2.13.Моделювання явища зменшення об'єму в результаті змішування різних рідин. Якщо взяти горох і пшоно (a) і ретельно перемішати їх, побачимо, що об'єм суміші менший за суму об'ємів її компонентів (б). Це можна пояснити тим, що крупинки пшона потрапили в проміжки між горошинами
4. Намагаємось уявити собі розміри атомів
Атоми є дуже малими. З'ясовано, що розміри атомів приблизно дорівнюють 10-10м (0,0000000001 м). Щоб уявити, наскільки малим є це значення, наведемо таке порівняння: діаметр молекули в стільки ж разів менший за діаметр яблука, у скільки разів діаметр яблука менший, ніж діаметр Землі.
Про розміри атомів також можна судити з прикладу. Якби всі люди нашої планети проводили все життя, займаючись тільки лічбою, усі разом ми змогли б полічити атоми тільки в головці однієї малої шпильки.
5. Пригадуємо будову атома
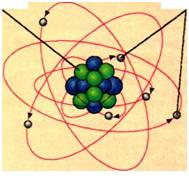
Досліди показали, що атом має складну структуру. Він являє собою позитивно заряджене ядро, оточене хмарою легких частинок — електронів, які мають негатив ний заряд (рис. 2.14). Маса ядра незначно відрізняється від маси атома. Маса ж електронів порівняно з ядром дуже мала.
Звичайно, наведені в цьому параграфі дані — це тільки незначна частина сучасних відомостей про атоми й молекули. З деякими іншими їхніми властивостями ви познайомитесь у наступних параграфах, про дещо довідаєтесь у старших класах.
Ядро(+) Електрони (-) Електрони (-)
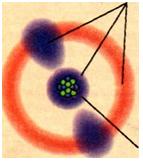
Ядро (+)
Рис. 2.14. Моделі атома: а — планетарна модель: у центрі атома — ядро, навколо ядра оберта-ються електрони; б — сучасна: електрони нібито «розмазані» по орбіталях — частинах простору, що оточують ядро. Для наочності на рисунку відстань від ядра до електронів показано у 2—3 рази більшою, ніж діаметр ядра. Насправді ця відстань перевищує розмір ядра в 100 000 разів
ПІДБИВАЄМО ПІДСУМКИ
Усі речовини складаються з дрібних частинок — молекул або атомів. Між молекулами (атомами) існують проміжки.
Молекулою називається найменша частинка речовини, що має її основні хімічні властивості та складається з атомів. Атом має складну структуру і являє собою позитивно заряджене ядро, оточене хмарою легких частинок — електронів, які мають негативний заряд.
РОЗТАШУВАННЯ МОЛЕКУЛ У ТВЕРДИХ ТІЛАХ РІДИНАХ ТА ГАЗАХ ДИФУЗІЯ
Взаємодія атомів і молекул. Дифузія
Дифузія – взаємне проникнення дотичних речовин одна в одну внаслідок безперервного руху молекул.
Найшвидше дифузія відбувається в газах, повільніше за все – у твердих тілах. Це пов’язано з особливостями розташування молекул газів, рідин та твердих тіл. Швидкість дифузії також залежить від температури тіла: чим вища температура, тим швидкість дифузії більша.
Дифузія дуже важлива для людей та інших живих організмів. Дифузією пояснюється проникнення кисню в кров через тонкі тканини легенів, вуглекислого газу з повітря у листя рослин, повітря у воду водоймищ. Морська тварина кальмар при нападі на неї викидає у воду чорнильну рідину. Це їй дозволяє заховатися від небезпеки. Але з часом вода у морі знову стає прозорою.
Також дифузія забезпечує нам безпеку. Природній газ, яким люди користуються на кухні, не має ні кольору, ні запаху. Але на розподільних станціях газ змішують з особливою речовиною, що має неприємний різкий запах, який легко відчуває людина навіть при невеликій концентрації.
Чому тіла не розпадаються на окремі частинки, хоча молекули розділені проміжками та безперервно рухаються? Справа в тому, що між молекулами існує взаємне притягання. Кожна молекула притягує до себе сусідню і сама притягується до неї. Це притягання помітно виявляється лише на відстанях, які можна порівняти з розмірами самих молекул. Тоді чому між молекулами існують проміжки? Відповідь проста: між молекулами існує взаємне відштовхування. Притягання і відштовхування діють одночасно, але в разі зближення молекул збільшується відштовхування, а в разі віддалення – притягання.
Досліди довели, що атом також має складну будову: в середині атома знаходиться позитивно заряджене ядро, навколо якого обертаються електрони.
Таку модель атома запропонував Резерфорд і назвав її планетарною моделлю атома. Порівняння з Сонячною системою не випадкове: діаметр Сонця майже в стільки ж разів менший за розміри Сонячної системи, у скільки розмір ядер менший від діаметра атома.
ВЛАСТИВОСТІ ТВЕРДИХ ТІЛ РІДИН І ГАЗІВ
Усе, що нас оточує у навколишньому світі, називається матерією. Матерія існує в двох видах — речовина і поле. Речовина це те, з чого складаються усі тіла. Поля бувають різні. Це, наприклад, гравітаційне поле, або поле тяжіння внаслідок дії якого всі тіла притягуються до’ Землі Електричне поле спричинює електричний струм. Під дією магнітного поля залізні предмети притягуються до магніту. Світло і радіохвилі також є польовим видом матери.
Речовина може перебувати в трьох станах твердому, рідкому й газоподібному. Відповідно у Природі існують тверді тіла, рідини і гази. Наприклад, олівець і зошит, стіл і стільці, під лога і стіни, будинок школи є твердими тілами. Вода, молоко, сік, олія, бензин, ртуть за звичайних умов є рідинами. Повітря, кисень, вуглекислий газ, природний газ (метан), якии використовують у побуті, є газами.
Ми практично безпомилково розрізняємо тверді, рідкі і газоподібні тіла за їхніми певними ознаками ми властивостями. Наприклад, легко відрі інмгмо воду від льоду, хоча за хімічними іиііктиностими це одна й та сама речовина; чітко роїмежовуємо гази і рідини, хоча всі газоподібні тіла за певних умов можуть стати рідкими Так, зокрема, газ для запальничок перебуває в балончиках у зрідженому стані; скраплений азот використовують
у наукових дослідженнях. …
З’ясуємо, за якими ознаками ті чи інші тіла
називають твердими, рідкими чи газоподібними?
Тверді тіла. Візьмемо кілька предметів – дерев’яний брусок, металеву кульку, скляну пластину, шматок пластиліну, ластик (мал. 2.1) 
За зовнішніми ознаками—кольором, прозорістю.,розміром, формою—вони відрізняються одне від одного. Проте вони мають і спільну властивість, за якою їх називають твердими тілами: вони зберігають свою форму. Легко помітити, що кожне з цих тіл має власну поверхню, яка обмежує його і визначає форму.
Тверді тіла можуть бути крихкими (скло, дорцеляна, лід) або пластичними (гума, пластилін, віск). Одні тіла відновлюють свою форму. виявляючи пружні властивості, інші залишаються у зміненому стані після припинення дії на них. Існують тіла, у яких можна легко змінити форму (пластилін, віск, свинець), для інших це вимагатиме значних зусиль (дуб, сталь, алмаз).
Очевидно, що ці тіла мають різну твердість. Наприклад, якщо стальним різаком провести по мідній пластині, на ній залишиться подряпина. Це вказує на те, що сталь твердіша за мідь; мід-на ж пластина ніколи не залишить подряпини на сталі, оскільки мідь м’якша за сталь.
Цю властивість твердих тіл, зокрема, використовують у технології обробки матеріалів. Так, за допомогою інструмента, виготовленого із загартованої сталі, обробляють різні металеві та дерев’яні вироби, алмазним різаком ріжуть скло, стальними ножицями кроять тканини і метал.
З життєвого досвіду нам відомо, що внаслідок нагрівання до певної температури тверді тіла плавляться і стають рідинами. Так, лід плавиться при температурі 0 °С, мідь—при 1085 °С, залізо—при 1535 °С, алмаз—вищій за 3500 °С.
Тверді тіла різняться й іншими фізичними властивостями, наприклад, здатністю передавати теплоту або проводити електричний:трум. З такими їхніми властивостями ознайомимося далі. Проте вже на підставі наведених вище прикладів можна помітити загальну ознаку, за якою тверді тіла відрізняються від рідин і газів: здатність упродовж тривалого часу зберігати надану їм форму.Адже треба докласти певних зусиль, інколи значних, для того, щоб змінити форму твердого тіла. При цьому можна дізнатися — крихке, пластичне чи пружне воно.
Рідини. Наповнимо рідинами кілька посудин різної форми (мал. 2.2). Як бачимо, усі рідини
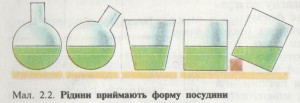
приймають форму посудини, яку заповнюють. На межі з повітрям рідина утворює власну вільну поверхню. Під дією тяжіння ця поверхня завжди горизонтальна, як би ми не нахиляли посудину. Якщо рідину перелити в іншу посудину, то вона набуде іншої форми, повторивши форму цієї посудини.
Зазвичай ми говоримо: «тече вода», «ллється молоко», «витікає пальне». Не раз ми помічали, що розлита на підлогу рідина розтікається тонким шаром по її поверхні. Усі ці приклади ілюструють властивість рідин, яку називають текучістю. Вона використовується, наприклад, під час транспортування рідин. Так, вода по трубах надходить у будівлі, басейни і фонтани, нафта і рідке паливо тече у нафтопроводах, розплавлений метал металурги виливають у форми.
Під час охолодження рідин до певної температури вони тверднуть, кристалізуються. Встановлено, що відбувається це за тієї самої температури, за якої дана речовина плавиться. Так, за природних умов вода стає льодом при 0 °С, але й лід тане також при 0 °С. Усе залежить від того, як відбувається цей процес —тіло дістає чи втрачає теплоту. Якщо, наприклад, в озері плаває лід, то він танутиме, коли температура повітря вища за 0 °С, тобто навколишнє середовище віддаватиме теплоту, і навпаки, при «мінусовій» температурі утворюватимуться нові брили льоду.
Відомо, ЩО рідини можуть випаровуватися, тобто переходити у газоподібний стан. Легко переконатися, що чим вища їхня температу-па тим інтенсивніше відбувається цей про цес. Так, улітку калюжі висихають швидше,
ніж навесні чи восени.
За певної температури рідини починають
інтенсивно випаровуватися не лише з поверхні але й усередині, з утворенням бульбашок.
Це явище називається кипінням. За них умов вода кипить при плюс 100 С, аце ТОн—при плюс 56,5 °С, зріджене повітря
при мінус 195 °С.
Отже, на підставі узагальнення нашого досвіду можна зробити такий висновок: на відміну від твердих тіл рідини не мають власної форми і тому під дією сили тяжіння повторюють форму тієї посудини, яку заповнюють; рідини текучі і тому легко змінюють свою форму; на межі з повітрям вони утворюють вільну горизонтальну поверхню; під час охолодження за певної температури вони кристалізуються і тверднуть; рідини переходять у газоподібний стан через випаровування.
Гази. Візьмемо м’яч, дитячу повітряну кульку і циліндр з поршнем або насос. Коли за допомогою насоса «накачати» повітрям, наприклад, футбольний м’яч чи кульку, вони набудуть округлої форми, яку задають їм оболонки (мал. 2.3)

Очевидно, що всередині них повітря розподілилося по всьому об єму. І ази леткі і заповнюють увесь наданий їм об єм. Вони не мають власної вільної поверхні, як
тверді тіла і рідини.
Гази легко стискуються і так само легко розширюються, що можна продемонструвати за допомогою насоса (мал. 2.4).
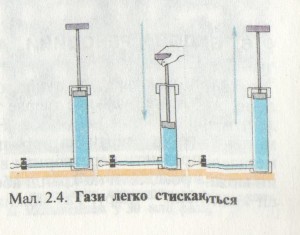
Натиснемо на поршень насоса—він переміститься майже до кінця свого ходу. Якщо тепер відпустити його, то він повернеться у своє початкове положення.,
Досліди показали, що з охолодженням газів
до певної температури вони починають скраплюватися і стають рідинами. Встановлено, що це відбувається при тій самій температурі, при якій відповідна рідина кипить. Тобто, як і у випадку переходу води в лід, усе залежить від конкретних фізичних умов: якщо теплота надається рідині, то вона кипить і переходить у газоподібний стан; якщо газ віддає теплоту, то він скраплюється, тобто конденсується. Наприклад, аміак кипить (отже, і скраплюється) при температурі мінус 33,4 °С, рідкий кисень кипить при мінус 183 °С, зріджене повітря — при мінус 195 °С. Найнижчу температуру кипіння має гелій — мінус 270 °С.
Отже, гази леткі і тому заповнюють увесь наданий їм простір; вони легко стискуються і легко розширюються; вони не мають власної форми і легко її змінюють, але на відміну від рідин гази не утворюють вільної поверхні; під час охолодження до певної температури гази скраплюються і стають рідинами.
Як підсумок, можна сказати, що тверді тіла, рідини і гази —це не особливі види речовини, а її стани, в яких вона перебуває за певних фізичних умов. Зокрема, це залежить від температури. У фізиці ці стани називають агрегатними станами речовини.
Висновки:Речовина і поле – два види матерії.Лід, вода і пара —це три стани однієї речовини.За різних фізичних умов одна й та сама речовина може перебувати у твердому, рідкому або газоподібному стані.Тверді тіла відрізняються своїми механічними властивостями — твердістю, пластичністю, пружністю тощо.За певної температури тверді тіла плавляться.Рідини мають власну вільну поверхню.Усі рідини проявляють текучість.За певної температури рідини тверднуть.Рідини можуть випаровуватися.За певної температури (рідини киплять).Вода кипить при 100 °С.Гази заповнюють увесь об’єм посудини, в якій містяться.За певних умов гази можуї бути зрідженими.Гази леткі і не утворюють вільної поверхні. Вони легко стискуються.Речовина перебуває у тому чи іншому агрегатному стані з певних фізичних умов, зокрема при певній температурі.
РІЗНОМАНІТНІСТЬ РЕЧОВИН І МАТЕРІАЛІВ ТА ЇХ ВИКОРИСТАННЯ ЛЮДИНОЮ
Поняття про енергію
Що є поняттям «енергія», яке ми так часто використовуємо? «Енергія» (грецьк. ενεργια – дія, діяльність) – загальна кількісна міра різних форм руху матерії. За великим рахунком поняття енергії, ідея енергії штучні й створені спеціально для того, щоб бути результатом наших роздумів про навколишній світ. На відміну від матерії, про яку ми можемо сказати, що вона існує, енергія – це плід людської думки, її «винахід», побудований так, щоб була можливість описати різні зміни в навколишньому світі й водночас говорити про сталість, збереження чогось, що було назване енергією. Для цієї фізичної величини довгий час вживався термін «жива сила», введений І. Ньютоном. Вперше в історії в поняття «жива сила» сенс «енергія», не вимовляючи ще цього слова, вкладає Роберт Майєр у статті «Зауваження про сили неживої природи», опублікованій у 1842 році. Спеціальний термін «енергія» був введений у 1807 р. англійським фізиком Томасом Юнгом і позначав величину, пропорційну масі та квадрату швидкості тіла,що рухається. У науку термін «енергія» у сучасному його розумінні ввів Уїльям Томсон (лорд Кельвін) у 1860 році.
Енергія проявляється у різних формах руху матерії, що заповнює весь світовий простір. Властивістю, притаманною всім видам енергії і об'єднуючою їх, є здатність кожного виду енергії переходити за певних умов у будь-який інший її вид у суворо визначеному кількісному співвідношенні. Сама назва цієї властивості – «закон збереження і перетворення енергії» – була введена у науковий обіг Ф. Энгельсом, що дозволило всі види енергії вимірювати в одних одиницях. За таку одиницю було прийнято джоуль (1 Дж =1 H · м =1 кг · м2/с2). У той же час для вимірювання кількості теплоти використовують «стару» одиницю – 1 кал (калорія), для вимірювання механічної енергії – величину 1 кГм = 9,8 Дж, електричної енергії – 1 кВт · ч = 3,6 МДж, при цьому 1 Дж = 1 Вт · с.
Майже всі види енергії, що розглядаються у технічній термодинаміці, за винятком теплової, являють собою енергію направленого руху. Так, механічна енергія проявляється у безпосередньо спостережуваному русі тіл, що має певний напрям у просторі (рух газу по трубі, політ снаряда, обертання валу і т.ін.). Електрична енергія проявляється в прихованому русі електронів провідником (електричний струм). Теплова енергія виражається в молекулярному і внутрішньомолекулярному хаотичному русі, будучи енергією хаотичного руху атомів і молекул речовини. Теплова енергія газів проявляється в коливальному, обертальному і поступальному русі молекул, які постійно змінюють свою швидкість за величиною і напрямом. При цьому кожна молекула може безладно переміщуватися у всьому обсязі газу. У твердих тілах теплова енергія проявляється в коливаннях молекул і атомів стосовно положень, які визначаються кристалічною структурою речовини, в рідинах – у коливанні та переміщенні молекул або їх комплексів. Отже, корінною відмінністю теплової енергії від інших видів енергії є те, що вона є енергією не направленого, а хаотичного руху. У результаті цього перетворення теплової енергії на будь-який вид енергії направленого руху має свої особливості, вивчення яких і є одним з головних завдань технічної термодинаміки.
Кожне тіло в будь-якому його стані може володіти одночасно різними видами енергії, зокрема тепловою, механічною, електричною, хімічною, внутрішньоядерною, а також потенційною енергією різних фізичних полів (гравітаційного, магнітного, електричного). Сума всіх видів енергії, якими володіє тіло, є повною його енергією.
Теплова, хімічна і внутрішньоядерна енергії входять до складу внутрішньої енергії тіла. Всі інші види енергії, пов'язані з переміщенням тіла, а також потенційна енергія зовнішніх фізичних полів відносяться до його зовнішньої енергії. Наприклад, зовнішньою енергією снаряду, що летить, в зоні дії сил земного тяжіння буде сума його кінетичної Е к і потенційної енергії гравітаційного поля. Якщо газ або рідина рухаються безперервним потоком у трубі, то в їх зовнішню енергію додатково входить енергія проштовхування, яку іноді називають енергією тиску Е пр.
Зовнішня енергія, отже, є сумою
Ез=Ек+ΣЕпi+Епр,,
де Епi – потенційна енергія i-го поля (магнітного, електростатичного і т. д.).
Внутрішня енергія тіла U може бути представлена такою, що нібито складається з двох частин: внутрішньої теплової енергії U Т і U 0 – внутрішньої нульової енергії тіла, умовно охолодженого до абсолютного нуля температури:
U=U0+UТ.
Внутрішньою тепловою енергією є та частина повної внутрішньої енергії тіла, яка пов'язана з тепловим хаотичним рухом молекул і атомів й може бути виражена через температуру тіла та інші його параметри. Оскільки температура реального тіла тільки частково відображає його внутрішню теплову енергію, зміна останньої може мати місце і при постійній температурі тіла. Прикладами цього є процеси випаровування, плавлення, сублімації, в яких відбувається фазове перетворення і змінюється ступінь хаотичності молекулярного руху. Таким чином, повна енергія тіла в загальному випадку може бути представлена у вигляді суми внутрішньої нульової U 0, внутрішньої теплової U Т, зовнішньої кінетичної Е к енергій, сукупних зовнішніх потенційних? Е п i енергій і енергії проштовхування Е пр:
Е = U 0+ U Т +Е к+Σ Е п i + Е пр.
Кожна з цих складових повної енергії може за певних умов перетворюватися одна в одну. Наприклад, у хімічних реакціях має місце взаємне перетворення U0 в UТ. Якщо реакція екзотермічна, то частина нульової енергії перетворюється на теплову. Нульова енергія отриманих речовин виявляється меншою, ніж вихідних, – відбувається «виділення тепла». У ендотермічних реакціях спостерігається зворотне явище: нульова енергія збільшується за рахунок зменшення теплової енергії – відбувається «поглинання тепла». У процесах, не пов'язаних зі зміною хімічного складу речовини, нульова енергія не змінюється і залишається постійною. За цих умов змінюється тільки внутрішня теплова енергія. Це дозволяє в різних розрахункових рівняннях враховувати зміну лише внутрішньої теплової енергії, яку надалі називатимемо просто внутрішньою енергією U.
Якщо однорідне тіло масою m має внутрішню енергію U, то внутрішня енергія 1 кг цього тіла
u=U/m.
Величину u називають питомою внутрішньою енергією і вимірюють в Дж/кг.
Зовнішня кінетична енергія (Дж) є енергією поступального руху тіла як цілого і виражається формулою
E к= mw 2/2,
де m – маса тіла, кг; w – швидкість руху, м/с.
Зовнішня потенційна енергія як енергія направленої дії статичних полів може бути виражена через можливі роботи кожного поля від заданого положення до якихось нульових. Так, потенційна енергія гравітаційного поля виражається як добуток сили тяжіння mg цього тіла на його висоту H над яким-небудь нулем відліку:
E = mgH.
Тут висота H є відповідною координатою. Енергія проштовхування Епр є додатковою енергією речовини, що виникає в системі за рахунок впливу на неї інших частин системи, які прагнуть виштовхнути цю речовину із займаної посудини. Так, при перетіканні газу (або пари) трубою або яким-небудь каналом в умовах суцільного потоку кожен кілограм цього газу, окрім внутрішньої і зовнішньої кінетичної і потенційних енергій, володіє ще додатковою, переношуваною на собі енергією проштовхування:
E пр.= p υ,
де p – питомий тиск; υ – питомий об'єм (об'єм 1 кг маси речовини).
Для газів, пари і рідин, що знаходяться у потоці, величина pυ (або pV для m кг речовини) визначає невід'ємну частину їх енергії. Тому для речовин, що знаходяться в суцільному потоці, визначальним параметром буде вже не внутрішня енергія U, а сума U + pV = I, звана ентальпією. Для 1 кг речовини
i = u + pυ,
де i – в Дж/кг.
Такою ж енергією i володіє й 1 кг газу, що знаходиться в циліндрі, при витісненні його поршнем.
Повна енергія даної системи, що складається з 1 кг газу і діючого на нього поршня, дорівнюватиме сумі внутрішньої енергії u газу та енергії pυ його виштовхування, тобто буде дорівнювати його ентальпії. На цій підставі ентальпію часто називають енергією розширеної системи.
СОНЯЧНА ЕНЕРГІЯ ТА ЇЇПЕРЕТВОРЕННЯ В ІНШІ ВИДИ ЕНЕРГІЇ
Сонце – це найпотужніше джерело енергії для нашої планети. Без сонячного тепла і світла будь-яке життя на Землі було б неможливе. Всі наші повсякденні справи включають використання енергії. Вона необхідна для пересування транспорту і приготування їжі, для роботи і відпочинку, для обігріву і охолоджування приміщень. І навіть для того, щоб провести один вигляд енергії, доводиться витрачати інший.
Енергія Сонця може використовуватися для безлічі завдань. Одна з них – це перетворення сонячної енергії в електричну, в так звану сонячну електрику. Переваги використання сонячної енергії є такими, що далеко йдуть. Хоча сонячна енергія є порівняно новим джерелом енергії, він легко може стати найважливішим джерелом енергії в майбутньому. Це відбувається тому, що з багатьох переваг використання сонячної енергії:
• сонячна енергія, є поновлюваним ресурсом. Це означає, що ми не в страху виснаження її запасів. Хоча вона може зникнути за хмарами на мить, і недоступна в нічний час, але як правило потім повертається в повній силі.
• сонячна енергія не забруднює довкілля. На відміну від нафти, використання сонячної енергії не виділяє яких-небудь парникових газів, а також при виробленні її немає шкоди екології шляхом розливу або днопоглиблювальних робіт. Це, мабуть, одній з основних переваг використання сонячної енергії.
• електрика і тепло від Сонця є абсолютно безкоштовними. Після того, як сонячні батареїабо сонячні теплові колектори встановлюються, немає електричних витрат, необхідних для їх живлення.
• Сонячні батареї вимагають дуже малого обслуговування, в значній мірі тому немає рухомих частин, які мають бути збережені.
• Сонячні батареї можуть експлуатуватися все життя.
• Вживання сонячної енергії неймовірне різностороннє. Починаючи від простих калькуляторів і продовжуючи автомобілями, водонагрівачами, фонтанами, будівлями, а також електростанціями і супутниками.
• У віддалених районах, сонячна енергія може бути реалістичнішим варіантом енергії, ніж прокладення великих кількостей електричних дротів для підключення до енергомережі.
В цілому, складається враження, що сонячна енергія є просто гармонійнішим енергетичним ресурсом. Для здобуття інших джерел енергії, є необхідність видобутку викопних видів палива, тваринних джерел, або рослинного походження джерела. Тим часом, сонячне світло постійно падає на землю і у величезних об’ємах, незалежно від того, використовується він як енергетичний ресурс, чи ні. Людство не витрачає часу і зусиль для видобутку сонячного ресурсу, таким чином, економлячи засоби і довкілля.
І що найцікавіше, то лише завдяки тому, що у нас є Сонце ми і маємо практично всі джерела енергії. Виключенням можна назвати енергію приливів і відливів, за яку відповідальний Місяць, і радіоактивні елементи, які використовуються на атомних станціях. Енергія вітру повністю залежить від Сонця і різниці температур ним же і створюваною. Енергія вугілля, нафти і природного газу також у владі хімічних процесів, які відбуваються в надрах Землі під дією сонячних променів. Все б добре, але є «маленька» проблемка. Людство з такою швидкістю витрачає викопні джерела енергії, що відновлюватися вони ніяк не встигають. Саме час задуматися про заміну «викопній енергії».
Поряд з перевагами використання сонячної енергії, варто відзначити недоліки. До них відносяться сонячне світло не доступний ресурс в деяких регіонах планети. Крім того, сонячні батареї все ще не дешеві. Звичайно, технічний процес здобуття сонячної енергії буде вдосконалюватися, і вона продовжуватиме здешевлюватися, тоді як витрати на інші види енергії збільшаться.
ВИЧЕРПНІ І НЕВИЧЕРПНІ ДЖЕРЕЛА ЕНЕРГІЇ
Природні ресурси класифікуються за принципом вичерпності і відновлюваних.
Вичерпні природні ресурси — ресурси, кількість яких обмежено і абсолютно, і відносно. Вичерпні ресурси, у свою чергу, підрозділяються на невідновлювані та відновлювані. Невідновлювані природні ресурси абсолютно не відновлюються (кам’яне вугілля, нафту і більшість інших корисних копалин) або відновлюються значно повільніше, ніж йде їх використання (торф’яники, багато осадові породи). Використання цих ресурсів неминуче веде до їх виснаження. Охорона невідновлюваних природних ресурсів зводиться до раціонального, економного використання, боротьбі з втратами при добуванні, перевезенні, обробці та застосуванні, пошуку замінників. Відновлювані природні ресурси у міру використання постійно відновлюються (тваринний світ, рослинність, грунт). Процеси відновлення протікають з різною швидкістю для різних ресурсів: для відновлення тварин потрібно кілька років, лісу — 60-80 років, грунту — кілька тисячоліть.
Невичерпні природні ресурси — ресурси, кількість яких необмежено, але не абсолютно, а відносно наших потреб і термінів існування. Невичерпні природні ресурси включають ресурси водні (води Світового океану, прісні води) і космічні (сонячна радіація, енергія морських припливів). Однак якщо кількість невичерпних природних ресурсів щодо необмежено, то їх якість може обмежити можливість їх використання людиною (наприклад, кількість води не обмежена, але обмежена кількість питної води).
Основним і єдиним постачальником харчових ресурсів людства є біосфера. Харчові ресурси формуються і виробляються як в агроекосистемах, так і в первинній природі, включаючи Світовий океан. За даними фахівців, на даний момент 9-12% поверхні суші розорано, а 22-25% складають повністю або частково окультурені пасовища.
Найбільша частина харчових ресурсів зосереджена в Світовому океані та первинної природі суші. Причому продуктивність цих частин біосфери вище, ніж штучних агроекосистем. Тому протягом останніх десятиліть вченими планети приймаються великі зусилля по збільшенню харчових ресурсів в аграрному секторі. Зокрема, шляхом гібридизації, відбору були створені багаторічна пшениця, зернокормовая гібриди.
У тваринництві вченими світу також виведені високопродуктивні породи худоби з використанням досягнень генної інженерії. Швидку віддачу харчової продукції дає птахівництво. Харчові ресурси Світового океану зосереджені в основному в прибережних районах і на мілководді, причому ці місця найбільше схильні до негативного антропогенного впливу. Тому рішення багатьох екологічних глобальних і локальних проблем необхідно з метою збереження харчових ресурсів. В даний час в багатьох країнах світу, і в першу чергу в Африці, продовольча проблема загострилася.
СКЛАД ТА ВЛАСТИВОСТІ ГРУНТУ ВИДИ ГРУНТІВ
Грунт - це поверхневий шар земної кори, який утворюється і розвивається в результаті взаємодій, живих мікроорганізмів, гірських порід і є самостійною екосистемою.
Найважливішим властивістю грунту є родючість грунту, тобто здатність забезпечити ріст і розвиток рослин. Це властивість становить виняткову цінність для життя людини та інших організмів. Грунт є складовою частиною біосфери і енергії в природі і підтримує газовий склад атмосфери.
Date: 2015-07-22; view: 1492; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |