
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Рак почки
Рак почки (РП) называют опухолью терапевтов. Многообразие клинических проявлений этого заболевания приводит к тому, что большинство больных длительное время лечатся у врачей различных специальностей по поводу предполагаемых неопухолевых заболеваний.
ЭПИДЕМИОЛОГИЯ
В структуре онкологической заболеваемости РП занимает восьмое место, однако частота его в последнее десятилетие выросла более чем в 2 раза. В 1998 г. заболеваемость РП в РБ составила 11,9 случаев на 100 тысяч населения. У мужчин рак почки (РП) встречается в 2 раза чаще, заболевают преимущественно лица в возрасте 40–60 лет. Правая и левая почки поражаются с одинаковой частотой, двусторонние опухоли наблюдаются редко (0,5–1,5 %).
ЭТИОПАТОГЕНЕЗ
В возникновении опухолей почки доказана роль гормональных нарушений (экспериментальная индукция ОП путем введения самцам эстрогенов; терапевтический эффект прогестинов); ионизирующей радиации; химических канцерогенов (ароматические углеводороды, нитрозамины – достоверно повышает риск развития РП курение табака). В развитии ОП у детей несомненна роль врожденных пороков развития органа. В развитии рака почечной лоханки значительную роль играет предшествующий пиелонефрит.
МОРФОЛОГИЯ ОПУХОЛЕЙ ПОЧЕК.
Морфология новообразований почек характеризуется значительным разнообразием. Большинство опухолей почек – злокачественные, на доброкачественные приходится лишь около 6 %. Различают опухоли паренхимы почки (встречаются наиболее часто – в 75–95 % случаев), и почечной лоханки (встречаются редко – исключение составляют зоны эндемического нефрита – балканские страны). Термин "рак почки" относится именно к раку почечной паренхимы.
Опухоли почечной лоханки характеризуются выраженной спецификой клинического течения, являются самостоятельной нозологической формой и будут рассмотрены отдельно. Опухоли паренхимы почки у взрослых в подавляющем большинстве случаев – эпителиальные, у детей – нефробластические (из эмбриональных тканевых зачатков).
Среди опухолей почечной паренхимы у взрослых выделяют доброкачественные (аденома, составляет менее 6 %, крайне редко – неэпителиальные – фиброма, гемангиома), и злокачественные – рак (90 %), редко – саркомы (3,3 %). РП возникает из эпителия различных отделов нефрона и собирательных трубочек.
Основную массу, 90–94 % случаев РП, составляет почечно-клеточный рак; устаревшее его название – "гипернефроидный" рак, или гипернефрома – опухоль на разрезе пестрого серо-коричнево-желтого цвета, по внешнему виду напоминает ткань надпочечника. Консистенция опухоли мягкая, хотя при пальпации через брюшную стенку или интраоперационно, из-за покрывающего ее фасфиального футляра, она определяется как плотное образование. Почечно-клеточный рак часто имеет псевдокапсулу, характеризуется длительным, относительно доброкачественным течением, нередко достигает больших размеров (20–30 см. в диаметре). Гистологически почечно-клеточный рак чаще всего представлен светлоклеточным, или альвеолярным вариантом. Клетки опухоли полигональные, светлые, резко очерченные. Строма разделяет опухолевые элементы на отчетливые альвеолы. Характерны обширные очаги спонтанного некроза и гиалиноза, отложения извести, свежие и старые кровоизлияния. Другие формы РП встречаются редко. “Негипернефроидные” раки характеризуются выраженной злокачественностью течения, инфильтративным ростом и ранним метастазированием. Среди вторичных опухолей почки чаще других встречаются метастазы рака легкого.
КЛИНИЧЕСКАЯ АНАТОМИЯ.
Почка – это парный орган, осуществляющий экскрецию мочи. Почка имеет бобовидную форму, длина ее у взрослого человека 10–12 см., ширина 5–6 см., и толщина 4 см. Масса колеблется от 120 до 200 г. Почка имеет переднюю (более выпуклую) и заднюю поверхность, верхний и нижний полюсы, выпуклый латеральный и вогнутый медиальный край. В среднем отделе медиального края имеются почечные ворота. В них входят почечная артерия, нервы, и выходят мочеточник, почечная вена, лимфатические сосуды. Перечисленные структуры составляют "почечную ножку". Почечные ворота переходят в обширное углубление – так называемую почечную пазуху (sinus renalis), в которой расположены собирающие мочу малые и большие почечные чашечки и почечная лоханка. Вещество почки представлено корковым слоем толщиной 4–7 мм. (содержащим почечные тельца, проксимальные и дистальные отделы извитых почечных клубочков) и мозговым, имеющим форму пирамид, толщиной 2–2,5 см. Локализующиеся в мозговом веществе прямые канальцы и собирательные почечные трубочки сливаются в сосочковые протоки.
Расположены почки в поясничной области, по обе стороны от позвоночного столба, на передней поверхности задней брюшной стенки, забрюшинно. Почки лежат несимметрично: левая – несколько выше (верхний ее полюс располагается на уровне середины XI грудного позвонка, нижний – на уровне верхнего края III поясничного позвонка), чем правая (верхний полюс располагается на уровне нижнего края XI грудного позвонка, нижний – на уровне середины III поясничного позвонка). Легко запоминаемый ориентир: на рентгенограмме XII ребро пересекает левую почку посередине, правую – в верхней части. Нередко отмечается опущение почек, у 11 % женщин нижние полюса почек касаются гребня подвздошных костей. Нефроптоз может быть поясничным и даже тазовым – при этом почка пальпируется в виде гладкого, плотно-эластической консистенции, легко смещаемого образования ("блуждающая почка"). В отличие от нефроптоза, при дистопии – врожденной аномалии, когда почечная артерия отходит ниже своего обычного места, почка почти несмещаема. При тазовой дистопии почечная артерия отходит от одной из подвздошных артерий, почка фиксирована в тазу и может симулировать опухоль гениталий или неорганную забрюшинную опухоль.
Часто встречающаяся повышенная подвижность почки определяется строением ее оболочек, являющихся фиксирующим аппаратом. Почка покрыта тонкой фиброзной капсулой. Кнаружи от нее располагается значительной толщины жировая капсула, более выраженная сзади – паранефральная клетчатка. Почка вместе с надпочечником, прилежащим к верхне-медиальной поверхности ее верхнего полюса и жировой капсулой охватывается в виде мешка, открытого книзу, почечной фасцией (фасцией Герота), состоящей из двух листков – предпочечного и позадипочечного. Почечная фасция соединяется с фиброзной капсулой почки посредством волокнистых тяжей, пронизывающих жировую капсулу. Когда последняя при быстром похудании уменьшается, почка может стать подвижной. При нефроптозе традиционно, еще в прошлом веке рекомендовали усиленное питание. Спереди предпочечный листок фасции Герота покрыт брюшиной.
Кровоснабжение почек осуществляется отходящими от брюшной аорты почечными артериями, которые в воротах почки делятся на переднюю и заднюю ветви. Нередко имеются добавочные артерии, не обязательно вступающие в ворота, а часто идущие непосредственно к полюсам. Их травма во время операции угрожает интенсивным кровотечением – почка кровоснабжается очень обильно – за сутки через нее проходит более полутора тонн (1500–1800 л.) крови. Объемная скорость кровотока составляет 1000–1200 мл/мин. Отток крови происходит по почечным венам, впадающим в нижнюю полую вену. Лимфатические сосуды почки сопровождают кровеносные сосуды. Выходя из ворот почки, они впадают в лимфоузлы ворот почки, парааортальные и паракавальные лимфоузлы. Далее лимфа оттекает в грудной лимфатический проток и впадает в левый венозный угол.
РОСТ И РАСПРОСТРАНЕНИЕ РП.
Распространение РП происходит в результате инвазивного роста первичной опухоли, лимфогенного и гематогенного метастазирования.
При распространении за пределы капсулы почки опухоль врастает в паранефральную клетчатку, опухоли в/полюса – в надпочечник. Часто, в 15 –20 % случаев, РП в виде языков распространяется в просвет почечной и нижней полой вены. При этом опухолевая масса, покрытая эндотелиальной выстилкой (опухолевый тромб) может полностью обтурировать просвет вены либо располагаться пристеночно, частично сохраняя отток крови. Иногда опухолевый тромб распространяется выше диафрагмы, достигая в некоторых случаях правого предсердия. Прорастание первичной опухоли за пределы фасции Герота происходит редко.
Частота метастазирования РП не имеет строгой зависимости от размеров первичной опухоли. У значительной части больных первые проявления РП обусловлены отдаленными метастазами. Иногда первичная опухоль при этом настолько мала, что обнаруживается только на секции.
Основные пути метастазирования РП – лимфогенный и гематогенный. Отдаленные метастазы на момент установления диагноза имеются у 20 % больных. Лимфогенно наиболее часто поражаются регионарные лимфоузлы (у 13–14 % больных): ворот почек, парааортальные и паракавальные; реже – другие группы: медиастинальные, надключичные, подчелюстные лимфоузлы и др. Гематогенные метастазы, выявленные при установлении диагноза, поражают, в порядке убывания частоты (%): легкие (64,2), кости (47,1), печень (14,2), головной мозг и контралатеральную почку (по 4,2,%). У большинства больных метастазы были множественными. Иногда метастазы РП поражают кавернозные тела полового члена (характерно развитие приапизма), миокард (обычно клинически не проявляются), кожу и др. ткани. Редко (в 1–1,5 % случаев) происходит имплантация мигрирующих с током мочи клеток почечно-клеточного рака в слизистую мочеточника и мочевого пузыря (не доказано – возможно, лимфогенное распространение). Провоцирует метастазирование любая травма опухоли: при грубой пальпации, при выполнении восходящей пиелографии (противопоказана при РП), при мобилизации во время операции (перевязка сосудов должна быть выполнена возможно раньше).
КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ.
В настоящее время для стадирования РП наиболее широко применяется международная классификация по системе ТNМ (5я редакция, 1997 г.)
Классификация применима только для рака из почечного эпителия. Должно быть гистологическое подтверждение диагноза.
Т – первичная опухоль
Тх – недостаточно данных для оценки первичной опухоли.
Т0 – первичная опухоль не определяется.
Т1 – опухоль до 2,5 см. в наибольшем измерении, ограниченная почкой.
Т2 – опухоль более 2,5 см. в наибольшем измерении, ограниченная почкой.
Т3 – опухоль распространяется на крупные вены или надпочечник, или околопочечные ткани, но в пределах фасции Герота.
Т3А – опухоль распространяется на надпочечник или околопочечные ткани, но в пределах фасции Герота.
Т3В – массивное распространение опухоли на почечную или нижнюю полую вены ниже диафрагмы.
Т3С – массивное распространение опухоли в полую вену выше диафрагмы.
Т4 – опухоль распространяется за пределы фасции Герота.
N – регионарные лимфатические узлы
Регионарными лимфатическими узлами являются лимфоузлы ворот почки, парааортальные и паракавальные (ниже диафрагмы).
Nх – недостаточно данных для оценки регионарных лимфоузлов.
N0 – нет признаков метастатического поражения регионарных лимфоузлов.
N1 – имеются метастазы в одном лимфоузле до 2 см. в наибольшем измерении.
N2 – имеются метастазы в одном или нескольких лимфоузлах до 5 см. в наибольшем измерении.
N3 – имеются метастазы в лимфоузлах более 5 см в наибольшем измерении.
М – отдалённые метастазы
Мх – недостаточно данных для определения отдалённых метастазов.
М0 – нет признаков отдалённых метастазов.
М1 – имеются отдалённые метастазы.
Группировка по стадиям:
| Стадия I | Т1 | N0 | М0 |
| Стадия II | Т2 | N0 | М0 |
| Стадия III | Т1 | N1 | М0 |
| Т2 | N1 | М0 | |
| Т3А | N0, N1 | М0 | |
| Т3В | N0, N1 | М0 | |
| Стадия IV | Т4 | Любая N | М0 |
| Любая Т | N2, N3 | М0 | |
| Любая Т | Любая N | М1 |
КЛИНИКА.
Клиническое течение новообразований почек многообразно. "Классическая" триада симптомов – гематурия, опухоль, боль, встречается только у 14–15 % больных. У 50 % больных с описанной триадой уже имеются отдаленные метастазы. Чаще встречается один или два из этих симптомов.
Наиболее часто (у 60–88 % больных РП) встречается тотальная гематурия (термин "тотальная" характеризует не интенсивность, а характер гематурии, которая может быть также инициальной – когда примесь крови имеет место в первой порции мочи – при поражениях передней уретры, и терминальной – кровь в последней порции – при локализации патологического процесса в шейке мочевого пузыря). Гематурия при РП в большинстве случаев обусловлена деструкцией прорастающей в полостную систему опухоли, обычно не сопровождается болями. Появляется она внезапно, часто среди полного здоровья, и нередко имеет профузный характер. Характерны червеобразные сгустки крови в моче – "слепки" мочеточника. При интенсивном кровотечении крупные сгустки могут образовываться непосредственно в мочевом пузыре и вызывать задержку мочи (тампонада мочевого пузыря). Иногда вслед за гематурией развивается типичный приступ почечной колики, обусловленный закупоркой мочеточника кровяными сгустками (при мочекаменной болезни гематурия, наоборот, появляется после болевого приступа). Гематурия носит интермиттирующий характер – продолжается несколько минут или дней, затем неожиданно прекращается; возобновиться она может через несколько дней, месяцев или даже лет.
Следующий по частоте симптом – пальпируемая опухоль встречается у 50–75 % больных. При локализации в нижнем полюсе почки пальпируется само новообразование, а при поражении верхних отделов органа – оттесненная опухолью вниз почка. Из-за жирового и фасциального "футляра" опухоль обычно выглядит как гладкое, плотной консистенции, образование, при пальпации "выскальзывающее" из рук (симптом баллотирования свидетельствует о забрюшинной локализации образования, наблюдается и при редко встречающихся неорганных забрюшинных опухолях). Более точные данные можно получить при бимануальной пальпации в положении пациента на здоровом боку, иногда стоя (с легким наклоном туловища вперед для расслабления мышц брюшной стенки).
Боль в поясничной области на момент установления диагноза отмечается у 50 % больных. Тупая боль является следствием растяжения богатой нервными окончаниями фиброзной капсулы почки растущим опухолевым узлом, давлением последнего на окружающие ткани или смещением почки и натяжением почечной ножки. Интенсивная боль "радикулярного" характера возникает при прорастании опухолью нервных стволов или корешков спинномозговых нервов и является прогностически неблагоприятной. Коликообразная боль, нередко с иррадиацией в паховую область, возникает из-за резкого повышения внутрипочечного давления вследствие закупорки мочевыводящих путей кровяными сгустками.
Варикоцеле встречается у 3–14 % больных с новообразованиями почек. Слева варикозное расширение вен семенного канатика может быть идиопатическим и наблюдается у 20 % мужчин. Появление варикоцеле справа являются грозным симптомом, заставляющим заподозрить ОП. Правая внутренняя семенная вена впадает в нижнюю полую вену под острым углом, и в месте впадения ее всегда имеется клапан, из-за чего идиопатическое варикоцеле справа не встречается. При РП варикоцеле может быть обусловлено сдавлением или прорастанием опухолью внутренней семенной, левой почечной или нижней полой вен, опухолевым тромбозом их, а также повышением давления в почечной вене вследствие повышенного сброса в нее артериальной крови через патологические артериовенозные шунты. Это поздний, прогностически неблагоприятный признак. Опухолевая инвазия нижней полой вены встречается при РП в 6–10 % случаев и может проявиться такими симптомами, как расширение подкожных вен брюшной стенки ("голова медузы"), отеки нижних конечностей, половых органов.
Нередко встречаются общие, паранеопластические симптомы.
Стойкое повышение температуры тела, не реагирующее на антибактериальную терапию. Лихорадка наблюдается у 20–30 % больных, прогностически неблагоприятна, чаще встречается при высокозлокачественных "негипернефроидных" раках, исчезает после радикальной операции и возобновляется при появлении рецидива.
ü Похудание (у 20–30 %),
ü общая слабость, недомогание (у 20–40 %),
ü анорексия, тошнота, рвота (у 10–15 %),
ü нейропатии, миозиты (у 4–6 %) и др.
Эти проявления иногда предшествуют классическим признакам в течение нескольких месяцев и даже лет; в связи с чем около 30 % больных РП поступают в стационары с диагнозом неопухолевой патологии.
Своеобразными проявлениями опухолей почек являются встречающаяся у 0,4 % больных ренальная полицитемия (вторичный эритроцитоз), и артериальная гипертензия, исчезающая после нефрэктомии – у 2,5 % пациентов, которые могут быть обусловлены повышенным выделением, соответственно, эритропоэтина и ренина опухолью или почечной паренхимой, ишемизированной вследствие сдавления и функционирования артериовенозных шунтов.
Повышение СОЭ обычно сочетается с гиперпирексией и др. симптомами, в качестве единственного проявления РП наблюдается у 1.5 % больных. В ряде случаев при лабораторном исследовании выявляется также анемия, гипопротеинемия, повышение активности щелочной фосфатазы, трансаминаз и другие неспецифические изменения. Характерны эритроцитурия, протеинурия, лейкоцитурия, часто обусловленные паранеопластической нефропатией (функция контралатеральной почки часто улучшается после нефрэктомии).
У 3,6 % больных первые клинические проявления заболевания связаны с отдаленными метастазами. Костные метастазы, как правило, локализуются в диафизах трубчатых костей и плоских костях, и проявляются болью тупого характера, подчас очень интенсивной, особенно при поражении позвоночника, припухлостью и болезненностью в области поражения, иногда – патологическими переломами. Занимая по частоте 2е место после легочных, костные метастазы в качестве первого проявления РП наблюдаются чаще (соответственно – 31 и 58 % случаев). Метастазы в легких обычно являются случайной находкой при рентгенологическом исследовании (характерно выявление множественных округлых теней с четкими контурами, разных размеров), реже проявляются кашлем, кровохарканьем, одышкой, гиперпирексией. Редко причиной первых клинических проявлений РП служат метастазы в головной мозг, шейные лимфоузлы. Казуистическим является манифестирование заболевания метастазами в миокард, молочную железу, щитовидную железу, кожу, желудок.
ДИАГНОСТИКА.
С момента обращения к врачу до установления диагноза у 44 % больных проходит более 3 мес., и у 18 % – более года. Вследствие скрытого течения ранних форм заболевания и частого отсутствия патогномоничных симптомов более чем у половины больных РП выявляется в III–IV стадии. По данным Белорусского канцер-регистра, в 1998 г. в I–II стадии было выявлено 31,6 % случаев РП, в III стадии – 37,6 % и в IV стадии – 23.9 % (у 6,9 % больных стадия не была установлена).
До внедрения эхоскопии в широкую клиническую практику основным в диагностике РП являлось рентгеноурологическое обследование. Обзорная урография позволяет оценить контуры и положение почек, иногда обнаруживаются характерные для РП очаги кальцификации ячеистой структуры. Более четкая визуализация контуров достигается при томографии в условиях пневморетроперитонеума (последний с появлением высокоинформативных неинвазивных методик практически не используется). При экскреторной урографии оцениваются функциональное и анатомическое состояние почек. Функция пораженной опухолью почки длительное время остается удовлетворительной. Отсутствие выделения контрастного вещества почкой ("немая почка" свидетельствует о весьма распространенном поражении паренхимы или об инфильтрации опухолью сосудов почечной ножки. Может быть выявлено изменение контуров почки за счет опухолевого узла, деформация, дефект наполнения лоханки и чашечек, ампутация последних, смещение верхнего отдела мочеточника к средней линии и полостной системы. На нефротомограмме (выполняется в паренхиматозной фазе экскреторной или инфузионной урографии) выявляется повышенное контрастирование опухоли, что отличает ее от кисты. Ретроградная уретеропиелография высокоинформативна при дифференциальной диагностики патологии верхних мочевых путей благодаря четкому их контрастированию, однако при РП выполняется крайне редко, так как может провоцировать диссеминацию раковых клеток из-за нередко возникающего при повышении внутрилоханочного давления пиелоренального рефлюкса. Показана при подозрении на рак почечной лоханки или мочеточника.
Ультразвуковое исследование среди инструментальных методов диагностики РП в последнее десятилетие прочно заняло лидирующие позиции. Метод позволяет уверенно выявлять очаговое поражение почек от 0,5 см. в диаметре, дифференцировать жидкостные и солидные образования; при достаточных размерах (?) последних высказываться о доброкачественном или злокачественном их характере (для злокачественных опухолей характерна неоднородность эхоструктуры, неровность контуров, отсутствие четкой границы с тканью почки). Эхоскопия дает достаточно точную информацию об отношении опухоли к смежным структурам, их инвазии, наличии и распространенности опухолевого тромбоза почечных и полой вен. Наличие доплеровской приставки позволяет оценить степень нарушения регионарного кровотока. УЗИ весьма информативно при выявлении регионарных и отдаленных метастазов РП. Метастатические очаги в печени более 1 см в диаметре выявляются с достаточной уверенностью, при меньших размерах метастазов эхоскопия позволяет их заподозрить. При необходимости под эхоскопическим контролем может быть выполнена пункция подозрительного участка с целью цитологической или гистологической верификации как первичной опухоли почки, так и ее метастазов. Однако, высокая информативность УЗИ для выявления объемных образований паренхиматозных органов, широкая распространенность и всеобщая доступность этого исследования в последние годы практически не повлияла на состояние диагностики РП. Как в 1988 г., так и в 1998 г., большинство случаев РП выявляется в III–IV стадиях, когда результаты радикального лечения часто неудовлетворительные.
Радиозотопное исследование почек применяется для оценки их функционального состояния (радиоизотопная ренография) (хорошая функция почки не исключает ее опухолевого поражения – при РП функция почки страдает лишь при тотальном поражении или опухолевом тромбозе почечной вены). При диагностике очаговой патологии почек информативность радиоизотопного сканирования значительно уступает эхоскопии.
Рентгеновская компьютерная томография и магнитно-резонансная томография используются при необходимости для уточняющей диагностики. Их разрешающие возможности в дифференциальной диагностике солидных (плотных) образований почек несколько превышают возможности УЗИ.
Ангиография в настоящее время проводится для получения дополнительной информации о кровоснабжении почки или оценки степени инвазии опухоли в магистральные сосуды, в первую очередь в нижнюю полую вену (нижняя кавография), а также для эмболизации почечной артерии в качестве предоперационной подготовки или в паллиативных целях.
Обязательным при опухолях почек является рентгенография органов грудной клетки (необходимо исключить наличие метастазов в легкие и лимфоузлы средостения). При наличии болей в костях показано радиоизотопное сканирование скелета или рентгенография. Радиоизотопное исследование позволяет выявить костные метастазы на 3–4 месяца раньше, чем рентгенография. В подавляющем большинстве случаев метастатическое поражение костей проявляется болевым синдромом – из-за компактной структуры костной ткани рост в ней новообразования приводит к повышению внутритканевого давления. Однако иногда болей может не быть, поэтому при значительном распространении опухолей, часто метастазирующих в кости (рак легкого, рак почки, рак щитовидной, молочной и предстательной желез) иногда сканирование костей производят и в отсутствие болевого синдрома.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА.
Кисты почек при эхоскопии визуализируются в виде эхонегативных образований, характерен симптом дорзального усиления. Парапельвикальные кисты часто растут экстраренально, вызывая симптомы сдавления ворот почки – гипертонию. Поликистоз почек – процесс всегда двусторонний, сопровождается хронической почечной недостаточностью. Патогномонична пиелографическая картина двусторонних изменений (повышенная ветвистость чашечек, сдавление и удлинение лоханок), при УЗИ выявляются множественные кисты разного размера. Мультикистозная почка – всегда одностороннее заболевание, при котором почечная паренхима полностью замещается кистами неправильной формы и размеров. Единственным симптомом его нередко является пальпируемая бугристая опухоль. Эхинококкоз почки – заболевание редкое, диагноз устанавливается на основании эозинофилии, положительной реакции Кацони, гидатидурии. На рентгенограмме может быть видна кольцеобразная или дугообразная тень обызвествленной кисты. Необходимость дифференцировать опухоль почки с гидронефрозом чаще всего связана с наличием пальпируемой опухоли. При гидронефрозе она бывает более эластичной. Если нет присоединившейся инфекции, то похудания, анемии, повышенной СОЭ не бывает. Диагноз уточняется при ЭУ, УЗИ, восходящей УПГ. Карбункул почки проявляется клиникой септического процесса, при эхоскопии выглядит как участок сниженной эхогенности. При туберкулезе почки характерны и "внеурологические" проявления (поражение легких и др.), а также вовлечение мочеточника и мочевого пузыря (укорочение и деформация), иммунологические реакции, данные рентгеноурологического обследования и УЗИ. Мочекаменная болезнь проявляется характерным болевым синдромом, рентгенологически и при УЗИ визуализируется камень.
ЛЕЧЕНИЕ.
Радикальное лечение РП – хирургическое или комбинированное. Выполняется нефрэктомия, при которой вместе с почкой удаляются паранефральная клетчатка и, как минимум, близлежащие регионарные лимфоузлы. При наличии опухолевого тромба в нижней полой вене последний удаляют, при врастании в полую вену выполняют ее резекцию. Используются поясничный (обычно – с поднадкостничной резекцией ребра), трансабдоминальный (раньше – выход на сосуды) и торакоабдоминальный (удобен для удаления обширных опухолевых тромбов и лимфаденэктомии) доступы. Рак почки характеризуется относительно медленным течением. В мировой литературе описано 18 случаев спонтанной регрессии легочных метастазов "гипернефроидного" рака. Паллиативная нефрэктомия показана даже при наличии отдаленных метастазов – она уменьшает интоксикацию, улучшает общее состояние больных. При наличии одиночных отдаленных метастазов выполняют комбинированные операции (например, резекцию легкого), иногда – с резекцией полой вены. Только множественные отдаленные метастазы, выраженная кахексия, обширное прорастание опухоли в окружающие ткани и значительное снижение функции контралатеральной почки служат абсолютным противопоказанием к нефрэктомии.
Нефрэктомия нередко сопровождается повреждением нижней полой вены. Дефект полой вены ушивают. Допустима перевязка нижней полой вены ниже впадения контралатеральной почечной вены. Как казуистический описан способ гемостаза оставлением на полой вене краевого зажима.
При больших размерах опухоли почки операция часто сопровождается выраженной кровопотерей. Летальность после нефрэктомии по поводу РП достигает, по данным разных авторов, 10 %. Из-за многочисленных артериовенозных шунтов в ткани новообразования повышается давление в почечной вене, увеличивается ее диаметр, густая сеть паранефральных вен, анастомозирующих с поясничными венами, пронизывает паранефрий и охватывает почку в виде клубка (паранефральный варикоз). Варикозные паранефральные вены диаметром до 0,75 см., имеют тонкую и чрезвычайно хрупкую стенку. Уже в начале этапа мобилизации появляются многочисленные разрывы этих вен и интенсивное венозное кровотечение. Попытка остановить его путем перевязки или прошивания варикозных вен бывает безуспешна и приводит лишь к серьезной кровопотере. Необходимо, прижав кровоточащие вены салфетками и пеленкой, максимально быстро выделить и перевязать почечную ножку. При раздельной перевязке последней вначале лигируют почечную артерию. Будучи характерным для всех больных РП, паранефральный варикоз особенно выражен у больных с опухолевым тромбом в почечной или нижней полой вене. Существенно облегчает и делает более безопасным оперативное вмешательство предоперационная баллонная окклюзия почечной артерии (по Сельдингеру) – она позволяет оперировать практически на сухой почке.
При раке анатомически или функционально единственной почки и синхронном поражении обеих почек применяют резекцию почки (в т. ч. экстракорпоральную).
ЛТ и ХТ ввиду невысокой чувствительности к ним РП в качестве самостоятельного метода радикального лечения не применяются. Предоперационная ЛТ (ФД – 5 Гр, СОД – 20 Гр; операция в ближайшие 3 суток) позволяет повысить абластичность вмешательства и увеличивает 5летнюю выживаемость примерно на 15 %. В качестве предоперационной подготовки или в паллиативных целях, при неоперабельных опухолях, применяют химиоэмболизацию почечной артерии. Химиотерапия проводится при отдаленных метастазах РП после паллиативной нефрэктомии. Используются фторбензотеф, тиофосфамид, метотрексат, меркапртопурин, винбластин, винкристин, блеомицин. По некоторым данным, при сочетании метотрексата, блеомицина и винбластина частота ремиссий достигает 35 %. ХТ иногда дополняют иммунотерапией (БЦЖ, реаферон). Используется также гормонотерапия (прогестины – фарлутал и др.), при которой частичная регрессия или стабилизация опухолевого процесса отмечается в 6–33 % наблюдений.
Общая гипертермия с гипергликемией позволяет существенно повысить чувствительность опухолевых клеток к химиотерапии.
Опухоли почечной лоханки в нашем регионе встречаются редко, наиболее типичны следующие гистологические формы:
Переходноклеточная папиллома (облигатный предрак – перерождается в 100 % случаев, клинически протекает злокачественно, способна к имплантационному метастазированию в мочеточник и мочевой пузырь, лечится как рак),
Переходноклеточный рак (встречается у большинства больных раком почечной лоханки, излюбленный путь его распространения – имплантационное метастазирование в слизистую нижележащих отделов мочевых путей – мочеточник, мочевой пузырь; имплантационные метастазы обычно предшествуют появлению отдаленных метастазов),
Плоскоклеточный рак (встречается реже, протекает весьма агрессивно, наряду с имплантационными, рано дает лимфогенные и гематогенные метастазы).
Ведущие клинические симптомы являются типичные "урологические" проявления – рецидивирующая тотальная гематурия, тупая или острая боль в поясничной области на стороне поражения, в связи с чем обследуются такие больные обычно у уролога. Радикальное лечение – нефроуретерэктомия с резекцией мочевого пузыря (вокруг устья мочеточника), комбинированное лечение. Результаты хуже, чем при раке почечной паренхимы (РП).
Опухоль Вильмса (нефробластома, эмбриональная аденомиосаркома) чаще наблюдается у детей в возрасте от 2 до 5 лет. ОВ является, наряду с системными новообразованиями (крови), и опухолями ЦНС, наиболее частой злокачественной опухолью детского возраста.
Ведущие клинические симптомы:
Пальпируемая опухоль (у 78 % больных детей опухоль нащупывают родственники, что свидетельствует о низкой онкологической настороженности педиатров). Боли в животе. Гематурия.
Опухоль Вильмса может достигать гигантских размеров, часто – в 10 % случаев – имеется двустороннее поражение.
В диагностике ведущую роль играет УЗИ и экскреторная урография.
Лечение комбинированное или комплексное, изолированное хирургическое лечение не применяется. Операция – только чрезбрюшинным доступом (преимущество – абластичность, при переходе к этому доступу вместо поясничного отдаленные результаты улучшились в 6 раз!). Выполняется нефрэктомия с удалением паранефральной клетчатки, надпочечника, резекцией вовлеченных опухолью смежных структур, при двустороннем поражении – нефрэктомия и резекция менее пораженной почки.
Прогноз при ОВ ввиду ее высокой чувствительности к ЛТ и ХТ лучше, чем при РП у взрослых. Даже при наличии отдаленных метастазов (IV стадия) часть больных ОВ излечивается; 5летняя выживаемость в I стадии составляет 90 %, во II – 70–80 %, в III – около 40 %, и в IV – 5–10 %.
Профилактика РП заключается в отказе от курения, защите окружающей среды от различных загрязнений. Профилактика рака почечной лоханки (как и мочевого пузыря) – терапия пиелонефрита, соблюдение техники безопасности лицами, занятыми в анилиновой промышленности и на других вредных производствах.
Прогноз при РП, ввиду медленного роста опухоли и частого появления метастазов в отдаленные срок после радикальной операции, 5летняя выживаемость не является достоверным критерием излеченности больных. Для оценки отдаленных результатов лечения РП часто используется такой показатель, как 10-летняя выживаемость. Несмотря на совершенствование методов лечения, средняя цифра 5летней выживаемости при РП составляет 50 %, 10летней – 15–27 %. Коренное улучшение результатов лечения РП возможно только при условии его ранней диагностики, для которой необходимо проведение эхоскопического скрининга РП среди широкого круга пациентов с неспецифическими жалобами.
ОПУХОЛИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ ЗОНЫ
Опухоли панкреатодуоденальной зоны (ПДЗ), или, периампулярные опухоли – собирательное понятие, включающее злокачественные новообразования желчевыводящих путей, двенадцатиперстной кишки и поджелудочной железы.
Благодаря тесной анатомической и функциональной связи этих структур сходны и клинические проявления, методы диагностики и лечения периампулярных опухолей. Частота опухолей ПДЗ за последние 10 лет увеличилась в России и Белоруссии в 2 раза и составляет в настоящее время 5–9 % от общего количества всех злокачественных опухолей и 9–17 % новообразований органов пищеварения.
Среди опухолей ПДЗ около 65 % приходится на рак поджелудочной железы (РПЖ). Реже, примерно в 20 % случаев встречаются опухоли Фатерова соска (аденокарцинома, реже – аденома), в 12–14 % – рак внепеченочных желчных протоков и в 1–3 % – рак двенадцатиперстной кишки. При относительно невысокой заболеваемости (6–10 случаев на 100 тыс. населения) РПЖ в структуре онкологической смертности занимает 4–5 место. Это объясняется крайне агрессивным течением заболевания, несвоевременной диагностикой и сложностью лечения. В США, например, одногодичная выживаемость при РПЖ составляет 8 %, пятилетняя – 2 %.
ЭТИОЛОГИЯ
С повышенным риском заболевания опухолями ПДЗ, и прежде всего, РПЖ, сопряжены:
ü Избыточное употребление мяса и животных жиров, недостаток овощей в рационе (стимулирует выработку панкреозимина, вызывающего гиперплазию поджелудочной железы).
ü Курение табака – повышает риск РПЖ в 2 раза (нитрозамины и др. канцерогенные метаболиты попадают в желчь и при ее рефлюксе контактируют с тканью ПЖ; курение приводит к гиперлипидемии, которая способствует гиперплазии паренхимы ПЖ).
ü Алкоголизм (приводит к панкреатиту и секреторной недостаточности ПЖ).
ü Хронический панкреатит (в 50–60 % случаев сочетается с РПЖ).
ü Сахарный диабет (при СД выявляется гиперплазия ткани ПЖ; СД может развиваться на фоне панкреатита и рака).
ü ЖКБ (является этиологическим фактором рака желчных протоков и желчного пузыря; РПЖ чаще встречается в сочетании с холестериновыми камнями и после холецистэктомии).
ü Паразитарные заболевания желчевыводящих путей.
ü Промышленные канцерогены (чаще болеют лица. занятые в резиновой и деревообрабатывающей промышленности).
Рост и распространение опухолей ПДЗ происходит в результате их инвазивного роста, а также лимфогенного, гематогенного и, реже, имплантационного, или контактного, метастазирования.
ДИАГНОСТИКА
Около 80 % больных с механической желтухой опухолевой этиологии, прежде чем "попасть" к онкологу, в течение 2–3 недель и более проходят лечение в инфекционном стационаре по поводу предполагаемого вирусного гепатита. От момента появления механической желтухи опухолевой этиологии до операции проходит, в среднем, около месяца. Радикальное оперативное вмешательство из-за высокого уровня холемии и печеночной недостаточности у больных с длительно существующей механической желтухой возможно лишь на втором этапе, примерно через 3–4 недели после предварительного наружного или внутреннего дренирования желчных путей и ликвидации желтухи. Запоздалое выполнение радикального вмешательства приводит к плохим отдаленным результатам, 5летняя выживаемость при раке головки поджелудочной железы не превышает 5 %.
Для механической желтухи опухолевого генеза характерны:
ü быстрое развитие желтухи,
ü незначительный болевой синдром,
ü ахолия кала при вполне удовлетворительном общем состоянии,
ü пальпируемый (у 30 % больных) увеличенный, эластической консистенции, безболезненный желчный пузырь – см Курвуазье– достоверный признак механической желтухи опухолевого генеза,
ü признаки билиарной гипертензии при УЗИ – достоверный признак механической желтухи,
ü преимущественное повышение уровня связанного билирубина и резкое повышение щелочной фосфатазы, при нормальном (или незначительном повышении) уровня трансаминаз.
РАК ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ.
По передней поверхности поджелудочная железа покрыта брюшиной. Она имеет головку, тело, хвост и крючковидный отросток. Позади поджелудочной железы проходит брюшная аорта. Граница между головкой и телом поджелудочной железы проходит по брыжеечным сосудам. Рядом с артерией проходит верхнебрыжеечная вена, позади хвоста поджелудочной железы – селезёночная вена. Вены сливаются позади головки, образуя воротную вену.
Артериальная кровь поступает от чревного ствола. От него отходит селезёночная артерия, идущая по верхнему краю поджелудочной железы. От селезёночной артерии отходят ветви к телу и хвосту. Кроме того, поджелудочная железа получает кровь из гастродуоденальной артерии, отходящей от общей печёночной.
Лимфоотток осуществляется во все группы чревных лимфоузлов. От дистальных отделов поджелудочной железы лимфа оттекает в лимфоузлы ворот селезёнки.
Ацинарный эпителий поджелудочной железы выделяет литические ферменты. Секрет дренируется в Вирсунгов проток. В толще ткани головки поджелудочной железы проходит дистальная часть холедоха. Островковый эпителий (клетки Лангерганса) больше содержится в дистальных отделах и меньше – в головке поджелудочной железы.
Рак поджелудочной железы.
Опухоли поджелудочной железы делятся на доброкачественные и злокачественные. Они могут быть экзокринного и эндокринного происхождения.
Классификация опухолей поджелудочной железы.
1. Экзокринные.
2. Эндокринные.
Доброкачественные:
а) папиллярная аденома
б) цистаденома. Возникает чаще у молодых женщин. При малигнизации образуется цистаденокарцинома.
Злокачественные – из эпителия протоков, реже ацинусов, 95 % и более – аденокарциномы. Также встречаются плоскоклеточный, недифференцированный рак и цистаденокарцинома.
Частота возникновения рак поджелудочной железы не зависит от социально-экономического уровня. За последние 70 лет она возросла в 3 раза во всём мире. Чаще болеют негры, мексиканцы, жители Ближнего Востока (семиты). Частота встречаемости в Республике Беларусь примерно 7–10 на 100000 человек.
Этиология рака поджелудочной железы не изучена.
Диетарные факторы (предрасполагающие): частое употребление жареного мяса и жареных жиров, алкоголя, кофе (но не чая), курение, длительный контакт с бензидином, нитрозаминами (лаки, олифа, растворители). Также повышает риск развития рака поджелудочной железы хронический панкреатит. Определённую роль играет наследственный фактор (входит в синдром Линча-2).
Соотношение болеющих мужчин и женщин примерно 1,7:1.
Клиника и диагностика.
Отдельно рассматривают рак головки (85 %) и рак дистальных отделов поджелудочной железы. Они по-разному проявляются, так как головка и дистальные отделы поджелудочной железы имеют разные отношения с другими структурами.
Рак головки поджелудочной железы.
Симптомы:
Боли. Могут быть различной интенсивности. Возникают чаще после еды. При синдроме окклюзии Вирсунгова протока сразу после еды возникает очень сильная боль в эпигастрии, мигрирующая затем по всему животу, появляются схваткообразные боли, вздутие живота и профузный понос плохо переваренной пищей. Опухоль из эпителия суживает Вирсунгов проток и ведёт к развитию отёчного панкреатита. Пища, поступающая в 12-перстную кишку, не переваривается там, так как нет пищеварительных ферментов поджелудочной железы и, поступая в тонкую кишку, вызывает метеоризм и понос. При прекращении стимуляции после еды больному становится легче. Рак поджелудочной железы может привести к панкреатиту и, в то же время, он может протекать, как панкреатит.
Анемия. Носит гипопластический характер.
Похудание из-за снижения аппетита, ограничения себя в пище, особенно белковой.
Пальпация опухоли (если опухоль большая).
Желтуха – самый главный признак. Прогредиентно нарастает, никогда не уменьшается. Билирубин достигает 600 мкмоль/л. Желтуха может начинаться, как при остром гепатите: несколько дней длится продромальный период, слабость, тошнота, повышение температуры до 38о С, затем эти явления стихают, а потом снова появляется желтуха. Течение её никогда не бывает ремиттирующим как при подвижных камнях.
Дифференциальный диагноз.
Нельзя полагаться на клинику и лабораторные данные, которые не позволяют различить механическую и паренхиматозную желтухи. Нельзя ориентироваться на биохимический анализ крови, так как желтуха почти сразу же приобретает смешанный характер. Для дифференциального диагноза желтух используют УЗИ. В норме просвет печёночных желчных протоков не определяется, они могут быть расширены до нескольких миллиметров только после еды. При механической желтухе любой этиологии они расширены. Если они не расширены, то это не механическая желтуха. Лабораторные анализы только подтверждают диагноз. УЗИ – основной способ диагностики причины желтухи. Желтуху могут вызывать опухоли, камни, стриктуры желчевыводящих путей, рак поджелудочной железы, панкреатиты, опухоли и отёк Фатерова соска, рак 12-типерстной кишки, метастазы рака в печень, циррозы печени, паразиты и др.
Физикальные данные. Симптом Курвуазье – пальпируется растянутый желчный пузырь (положителен только в 40 % случаев, так как часто попадаются очень жирные пациенты или вообще без желчного пузыря и т. д.).
ЭРХПГ – Эффективность 97–98 %. Выявляется и рак и причина. При Вирсунгографии выявляют деформацию и сужение протока, так как в основном раки растут из эпителия. Кроме того, смотрят Фатеров сосок. Многие опухоли прорастают в 12-перстную кишку и вызывают дуоденальный стеноз.
КТ – дорогостоящий метод. Можно делать одномоментно ЭРХПГ и КТ.
Рак дистальных отделов поджелудочной железы.
Поджелудочная железа не выключается из эндокринной функции.
Симптомы:
Боли в эпигастрии, правом подреберье, спине, пояснице. Не связаны с едой. Возникают из-за поражения внутренностных нервов.
Похудание, снижение аппетита.
Анемия.
Сахарный диабет I типа – появляется за 3–4 месяца до возникновения болей.
Опухоль проявляется клинически тогда, когда достигает значительных размеров. Этим обусловлена более поздняя диагностика рака дистальных отделов поджелудочной железы по сравнению с раком головки.
Диагностика.
Основные методы – УЗИ и КТ. Вирсунгография и ЭРХПГ большого значения не имеют.
УЗИ и КТ часто не позволяют отличить рак от хронического панкреатита (индуративной и псевдотуморозной форм). Клиника их также сходна и поэтому применяют пункцию органа под контролем УЗИ. Головку поджелудочной железы не пунктируют, так как при раке поджелудочной железы всё равно выполняют операцию с использованием лапаротомного доступа.
Стадирование:
TNM классификация злокачественных опухолей, 4 издание, 1997 г.
Поджелудочная железа подразделяется на следующие анатомические области и части:
1. Головка поджелудочной железы (Опухоли, расположенные справа от левой границы верхней мезентериальной вены. Крючковидный отросток является частью головки).
2. Тело поджелудочной железы (Опухоли, расположенные между левой границей верхней мезентериальной вены и левой границей аорты).
3. Хвост поджелудочной железы (Опухоли, расположенные между левой границей аорты и воротами селезенки).
Регионарными для поджелудочной железы являются лимфатические узлы, подразделяющиеся на:
Ø верхние: кверху от головки и тела;
Ø нижние: книзу от головки и тела;
Ø передние: передние панкреатодуоденальные, пилорические и проксимальные мезентериальные;
Ø задние: задние панкреатодуоденальные, вокруг общего желчного протока и проксимальные мезентериальные;
Ø селезеночные: в воротах селезенки и, около хвоста поджелудочной железы.
Отдаленные метастазы РПЖ, как правило, локализуются в печени, парааортальных и надключичных лимфатических узлах слева (метастаз Вирхова).
TNM Клиническая классификация
Т - первичная опухоль
Тх - недостаточно данных для оценки первичной опухоли
Т0 - первичная опухоль не определяется
Tis - преинвазивная карцинома (carcinoma in situ)
T1-опухоль ограничена поджелудочной железой
Т1а - опухоль до 2-х см в наибольшем измерении
Т1б - опухоль более 2-х см в наибольшем измерении
Т2 - опухоль ограничена поджелудочной железой, более 2 см
Т3 - опухоль распространяется на любую из следующих структур: 12-перстная кишка, желчный проток, ткани около поджелудочной железы
Т4 - опухоль распространяется на любую из следующих структур: желудок, селезенки ободочная кишка, прилежащие крупные сосуды.
N - регионарные лимфатические узлы
Nх - недостаточно данных для оценки регионарных лимфатических узлов
N0 - нет признаков метастатического поражения регионарных лимфатических узлов
N1а – одиночный метастаз в регионарный лимфатический узел
N1b- множественные метастазы в регионарные лимфатические узлы
М – отдаленные метастазы
Мх – недостаточно данных для оценки
Группировка по стадиям
| Стадия 0 Стадия I Стадия II Стадия III Стадия IVA Стадия IVB | Тis T1,T2 T3 Т1,Т2,Т3 T4 Любое Т | N0 N0 N0 N1 Любое N Любое N | M0 M0 M0 M0 M0 M1 |
Лечение рака поджелудочной железы зависит от локализации опухоли.
Хирургическое лечение:
Резектабельность РПЖ составляет 10–15 % и зависит от размеров, локализации и отношения опухоли к магистральным сосудам. Существует 3 вида радикальных оперативных вмешательств:
Ø Панкреатодуоденальная резекция (ПДР, операция Whipple),
Ø Дистальная резекция ПЖ со спленэктомией.
Ø Тотальная панкреатдуодеэктомия (ТПДЭ).
Рак головки поджелудочной железы. Лечение начинается с проблемы желтухи. За 2–3 дня до операции проводят инфузионную подготовку, ликвидируют печёночно-почечную недостаточность, нормализуют функцию почек. Затем проводят операцию. Задачи операции:
Ø морфологическое подтверждение диагноза;
Ø интраоперационная оценка распространённости рака;
Ø ликвидация желтухи;
Ø создание условий для дальнейшего лечения.
Морфологическое подтверждение диагноза необходимо для дифференциальной диагностики рака головки поджелудочной железы с головчатым панкреатитом, аденомой головки (т. к. головку не пунктируют до операции). Интраоперационно проводят пункцию или биопсию опухоли. При интраоперационной оценке распространённости рака можно обнаружить метастазы в печень, парапанкреатические лимфоузлы, диссеминаты по брюшине.
Для ликвидации желтухи выполняют операцию. Если после операции планируется проводить лучевое лечение, то интраоперационно металлическими скрепками намечают поля облучения.
Дальнейшее лечение включает 3 варианта. Если имеются отдалённые метастазы, или больной в возрасте старше 70 лет, или имеются тяжёлые сопутствующие заболевания, то лечение заканчивают билиодигестивной операцией.
Если имеется крупная местнораспространённая опухоль с регионарными метастазами, то после операции проводят химиолучевое лечение (во время операции намечают поля облучения). Таким образом можно добиться паллиатива на несколько лет.
Если есть маленькая отграниченная опухоль без метастазов, то выполняют панкреато-дуоденальную резекцию (ПДР).
Показания к ПДР:
1. рак головки поджелудочной железы;
2. рак Фатерова соска;
3. рак дистальной части;
4. экстрапапиллярный рак или рак 12-перстной кишки (лейомиосаркома);
5. рак желудка, врастающий в головку поджелудочной железы;
6. головчатый панкреатит.
|
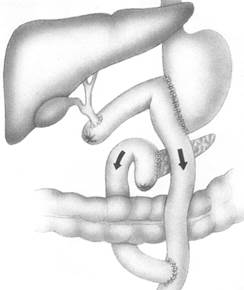 Рак дистальных отделов. Выполняют субтотальную дистальную панкреатэктомию. Поджелудочная железа пересекается по перешейку и удаляется вместе с селезёнкой. Ложе поджелудочной железы облучают и проводят химиотерапию.
Рак дистальных отделов. Выполняют субтотальную дистальную панкреатэктомию. Поджелудочная железа пересекается по перешейку и удаляется вместе с селезёнкой. Ложе поджелудочной железы облучают и проводят химиотерапию.
Послеоперационная летальность после ПДР и ТДПЭ составляет 10–15 %. Отрицательными моментами ТДПЭ являются развитие сахарной диабета и экзокринной недостаточности поджелудочной железы, требующих корригирующей терапии.
Комплексное лечение РПЖ (предоперационная лучевая терапия, радикальная операция и адъювантная ПХТ) позволяет получить 2-летнюю выживаемость у 60–70 % больных.
Прогноз: В связи с быстрым метастазированием прогноз при РПЖ неблагоприятный: 5-летняя выживаемость после радикальных операций составляет 4–8 %. При отсутствии опухолевой инвазии смежных структур и регионарных метастазов 5 лет после радикальных операций переживают 10 % больных РПЖ.
РАК ТЕЛА МАТКИ.
Среди злокачественных заболеваний у женщин рак тела матки занимает 4 место после рака молочной железы, кожи и желудка, в структуре онкогинекологической заболеваемости РТМ находится на первом месте в течение последних 5 лет. Самые высокие показатели заболеваемости РТМ отмечены на Гавайских островах (25,2 случаев на 100000 населения), в США (Калифорния) – 25 на 100000, в РБ – 17–19, в России – 12,9 случаев на 100000 населения.
Диагностика РТМ направлена на решение следующих задач:
Ø определение местной распространенности опухолевого процесса,
Ø выявление отдаленных метастазов,
Ø оценку функционального состояния органов и систем.
Диагностика первого этапа – скрининг РТМ.
УЗИ позволяет косвенно судить о состоянии эндометрия и провести отбор больных для цитологического обследования.
Цитологическое исследование аспирата из полости матки у больных в группах риска развития РТМ.
Диагностика второго этапа.
Гистероскопия позволяет оценить состояние эндометрия, провести топическую диагностику, выполнить биопсию. При отсутствии возможности проведения гистероскопии выполняется раздельное диагностическое выскабливание слизистой цервикального канала и полости матки с гистологическим исследованием препарата для определения степени дифференцировки опухоли.
УЗ-топометрия матки для измерения толщины стенки матки, размеров и формы полости матки, определения топики опухоли, измерения длины шейки и тела матки для выбора оптимального варианта контактного лучевого лечения.
УЗИ органов малого таза, печени, почек, регионарных лимфоузлов с целью исключения метастатического поражения (рецепторы эстрадиола, прогестерона).
Определение уровня гормональных рецепторов для выбора гормонального лечения.
Низкодозная маммография для исключения опухоли в молочных железах.
Эндоскопическое или рентгенологическое исследование толстой кишки (органа – мишени эстрогенов).
Стадирование: Классификация по системе TNM и по стадиям FIGO
| TNM категории | FIGO стадии | |
| Tx | Недостаточно данных для оценки первичной опухоли | |
| T0 | Первичная опухоль не определяется | |
| Tis | Преинвазивная карцинома (carcinoma in situ) | |
| T1 | Опухоль ограничена телом матки | |
| Т1а | 1А | Опухоль ограничена эндометрием |
| T1b | 1B | Опухоль, инвазирующая миометрий до половины его толщины |
| T1c | 1C | Опухоль, инвазирующая на глубину более половины миометрия |
| Т2 | Опухоль распространяется на шейку матки, но не выходит за пределы матки | |
| Т2а | 11А | Распространение только по железам шейки матки |
| Т2b | 11B | Стромальная ивазия ткани шейки матки |
| Т3и/илиN1 | Локальное и или местное распространение, соответствующееT3a, b, N1 и FIGO 111A, B, C | |
| Т3а | 111А | Опухоль распространяется на серозную оболчку и/ или придатки матки (непосредственное рспространение или метастатическое поражение) и/ или раковые клетки обнаружены в асцитической жидкости или смыве из брюшной полости |
| T3b | 111B | Поражение влагалища (непосредственное распространение или метастатическое поражение) |
| N1 | 111C | Метастазы в тазовых и/ или парааортальных лимфатических узлах |
| Т4 | 4 А | Опухоль распространяется на слизистую оболочку мочевого пузыря и/ или кишки |
| М1 | 4 B | Отдаленные метастазы (исключая метастазы во влагалище, брюшину таза и придатки матки, включая метастазы во внутрибрюшинные лимфатические узлы, кроме парааортальных и/ или подвздошных) |
Лечение.
Основными компонентами комбинированного и комплексного лечения больных раком эндометрия являются следующие методы:
Ø хирургическое лечение,
Ø лучевая терапия,
Ø химиотерапия,
Ø гормональное лечение.
Хирургическое лечение.
Для лечения больных раком тела матки используются 3 типа операций.
При переходе опухоли на шеечный канал выполняется расширенная экстирпация матки с придатками, верхней третью влагалища и тазовой клетчаткой (модификация Вертгейма) у больных до 50 лет.
При опухоли в теле матки применяется модификация расширенной экстирпации по Бохману (больным до 50 лет).
При невысокой вероятности лимфогенного метастазирования выполняется простая экстирпация матки с придатками и верхней третью влагалища.
Особенности выполнения хирургического этапа:
Ø Максимальная безопасность вмешательства обеспечивается компетентностью хирургической бригады, подготовкой больного к хирургическому вмешательству и техничным выполнением стандартных объемов.
Ø Онкологическая адекватность заключается в соблюдении принципов абластики и антибластики, в выборе оптимального объема хирургического вмешательства:
а. Отделение мочевого пузыря и прямой кишки от матки производится острым путем, клетчатка, окружающая эти органы, отходит к препарату.
б. Одноблочное радикальное иссечение тазовой клетчатки с заключенными в ней регионарными лимфатическими узлами.
в. Пересечение крестцово-маточных и кардинальных связок непосредственно у стенок таза (дистальный вариант).
г. Удаление не менее трети влагалищной трубки и клетчатки паракольпиев.
Ø Функциональная эффективность:
а. Отказ от перитонизации подвздошных зон после лимфодиссекции[1].
Лучевое и комбинированное лечение. Лучевая терапия применяется как самостоятельный метод, так и в комбинации с хирургическим. Для проведения радикального облучения используется сочетанная лучевая терапия, состоящая из двух компонентов:
а. облучение из внешних источников,
б. облучение контактными источниками.
Химиотерапевтическое лечение больных раком тела матки проводится при выходе опухоли за пределы матки, что соответствует III–IV стадии.
Гормональное лечение. Целью гормонотерапии является:
ü Снижение пролиферативной активности.
ü Повышение функционально-морфологической дифференцировки.
ü Секреторное истощение клеток.
ü Дегенеративно-атрофические изменения в опухолевых клетках.
Основные группы препаратов для гормональной терапии:
Синтетические прогестины:
ü оксипрогестерона капронат 12,5 % раствор, применяется по 500 мг ежедневно в течение 2 месяцев, затем по 500 мг 2 раза в неделю до 6 месяцев, затем 1 раз в неделю до 1 года,
ü депо-провера по 500 мг через день до 2х месяцев, затем 1 раз в неделю до 6 месяцев, затем 1 раз в 10–14 дней до 1 года.
Антиэстрогенные препараты:
ü Тамоксифен применяется по 20–40 мг на протяжении 1 года,
ü зитазониум применяется по 20–40 мг ежедневно на протяжении 1 года.
Прогноз. Пятилетняя выживаемость больных РТМ I стадии составляет 92 %, II стадии – 85 %, III–IVстадии – 57 %.
РАК ШЕЙКИ МАТКИ
В возникновении рака шейки матки (РШМ) наибольшее значение имеют папилломовирусная и герпесвирусная инфекции, раннее начало половой жизни, промискуитет, травмы шейки матки в родах, курение. РШМ занимает в структуре онкологической заболеваемости у женщин 6 место, что составляет 5,4 % всех злокачественных новообразований. Наиболее часто РШМ регистрируется в возрасте от 45 до 75 лет. Заболеваемость РШМ в разных регионах варьирует в широких пределах. Наиболее высокие показатели отмечены в Южной Америке (Бразилия – 83,2/100000 населения), в некоторых районах Индии среди индуистов: 43 на 100000 населения, в Японии при общей заболеваемости всеми видами рака женских половых органов 27,7 на 100000 женщин РШМ составляет 22,4 (80 % по отношению ко всей онкогинекологической заболеваемости), в США – 12,9. В центральных регионах России заболеваемость в 2001 г. составила 10,8 на 100000 населения. За 10 лет в РФ удельный вес опухолей шейки матки снизился с 5,5 % до 2,7 %. В РБ в последние годы заболеваемость колеблется от 15 до17 на 100000 женщин.
Шейка матки представлена влагалищной частью, покрытой многослойным плоским эпителием и эндоцервикальной, покрытой цилиндрическим эпителием. В зоне наружного зева многослойный плоский эпителий переходит в цилиндрический. Переходная зона эпителия является местом образования предраковых процессов и рака шейки матки.
Диагностика РШМ включает:
ü определение местной распространенности опухолевого процесса,
ü выявление отдаленных метастазов,
ü оценку функционального состояния органов и систем.
Скрининговая диагностика рака шейки матки.
Принята концепция двухэтапной системы обследования. На первом этапе производится первичное выявление – скрининг (определение групп риска развития шейки матки и выявление контингента женщин с предраковой патологией). На втором этапе используют методы углубленной диагностики.
I этап включает сбор анамнеза, обследование молочных желез, осмотр наружных половых органов, влагалища и шейки матки, цитологическое исследование мазков с поверхности шейки матки и из цервикального канала, бимануальное ректовагинальное исследование. На основании клинико-цитологических данных решается вопрос о необходимости углубленного обследования.
Классификация цитологических изменений.
1. Цитограмма без особенностей.
2. Воспалительный тип мазка
а) c дисплазией
б) трихомонады, грибы (с дисплазией)
в) пролиферация цилиндрического эпителия (умеренная, выраженная)
3. Дисплазия
а) слабая степень,
б) умеренная степень,
в) выраженная степень
4. Подозрение на рак.
5. Рак.
II этап обследования включает:
Верификацию диагноза.
Установление стадии заболевания.
а). Определение формы опухолевого роста.
б). Отношение исследуемого органа при выявленной патологии к окружающим структурам.
Оценку функционального состояния других органов и систем.
Кольпоскопия предложена Hinselmann в 1928 году, представляет собой обзор слизистой оболочки шейки матки и влагалища с помощью бинокулярного эндоскопа под 15–25 кратным увеличением после обработки 3 % раствором уксусной кислоты Метод позволяет выявлять участки слизистой шейки матки с предраковой и злокачественной трансформацией для биопсии.
Ультразвуковое исследование позволяет выявить метастазы в забрюшинных лимфоузлах, печени и других паренхиматозных органах брюшной полости и забрюшинного пространства. Под контролем УЗИ также выполняется тонкоигольная пункция лимфоузлов через влагалищные своды с целью верификации метастатического поражения регионарных лимфоузлов.
Стадирование рака шейки матки. (5е издание ТNM-классификации, 1997 г.).
Анатомические части.
1.Внутренняя оболочка канала шейки матки (endocervix)
2.Наружная часть шейки матки (exocervix)
Регионарные лимфатические узлы.
1.Парацервикальные (расположенные около шейки матки)
2.Параметральные (расположенные в околоматочной клетчатке)
3.Подчревные (обтураторные, внутренние подвздошные)
4.Наружные подвздошные.
5.Общие подвздошные.
6.Пресакральные.
7.Латеральные сакральные.
Date: 2015-07-02; view: 521; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |