
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

I. Средства, угнетающие нейрональный захват моноаминов 3 page
Аналептики возбуждают не только дыхательный, но и сосудодвигательный центр. Они приводят к увеличению общего периферического сопротивления сосудов и повышению артериального давления. Кровообращение в целом улучшается. Проявляется это главным образом при пониженном артериальном давлении. Прямого влияния на сердце аналептики, за исключением камфоры и кофеина, не оказывают. Камфора, по имеющимся экспериментальным данным, действует
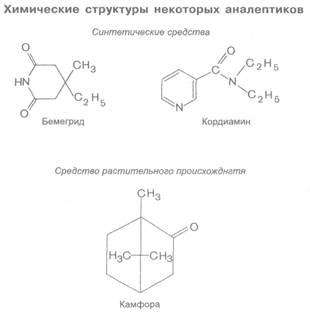
на сердце стимулирующим образом, усиливая эффекты возбуждения адренергической иннервации (о кофеине см. главу 11; 11.6).
Следует учитывать, что диапазон между дозами аналептиков (бемегрида, кордиамина, камфоры), необходимыми для стимуляции дыхательного и сосудодвигательного центров, и дозами, в которых они вызывают судороги, незначителен.
По аналептической активности препараты можно расположить в следующий ряд: бемегрид > кордиамин > камфора.
Аналептики являются функциональными антагонистами веществ наркотического типа и могут способствовать выведению из состояния наркоза (так называемое «пробуждающее действие» аналептиков). Однако этот эффект наблюдается при введении аналептиков в значительных дозах, в которых они могут вызывать судороги. В связи с этим «пробуждающее действие» аналептиков при отравлениях веществами наркотического типа действия практического значения не имеет. В этом случае их применение определяется только аналептическим действием, связанным с возбуждением центров продолговатого мозга. Вместе с тем стимуляторы ЦНС могут быть использованы для ускорения восстановления психомоторных реакций в посленаркозном периоде (аналептик при этом вводят на «выходе» из наркоза).
Бемегрид и кордиамин хорошо всасываются при разных путях введения. Камфора из масляных растворов всасывается медленно.
Для аналептического действия препараты обычно вводят парентерально. Выделяются аналептики и продукты их превращения почками.
Применяют аналептики при легких степенях отравления средствами для наркоза, снотворными наркотического типа, спиртом этиловым, а также при нарушениях внешнего дыхания другой этиологии, например при асфиксии новорожденных. Кордиамин и камфору используют также при сердечно-сосудистой недостаточности, хотя их эффективность при этой патологии признается не всеми.
К стимуляторам ЦНС относятся также коразол, секуринин, барвинкана гидрохлорид. Своеобразной фармакодинамикой обладает стимулятор дыхания этимизол (см. главу 13; 13.1).
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Бемегрид — Bemegridum | Внутривенно 0,01-0,05 г | Ампулы по 10 мл 0,5% раствора |
| Кордиамин — Cordiaminum | Внутрь 30-40 капель; под кожу, внутривенно и внутримышечно 1 мл | Флаконы по 15 мл (для приема внутрь); ампулы по 1 и 2 мл; шприц-тюбики по 1 мл |
| Камфора — Camphora | Под кожу 0,2-1 г | Ампулы по 1 и 2 мл 20% раствора в масле |
ЛЕКАРСТВЕННЫЕ СРЕДСТВА, РЕГУЛИРУЮЩИЕ ФУНКЦИИ ИСПОЛНИТЕЛЬНЫХ ОРГАНОВ И СИСТЕМ (главы 13-19)
Г л а в а 13
ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ВЛИЯЮЩИЕ НА ФУНКЦИИ ОРГАНОВ ДЫХАНИЯ
В этот раздел включены следующие группы:
- стимуляторы дыхания;
- противокашлевые средства;
- отхаркивающие средства;
- средства, применяемые при бронхоспазмах;
- средства, применяемые при острой дыхательной недостаточности.
13.1. СТИМУЛЯТОРЫ ДЫХАНИЯ
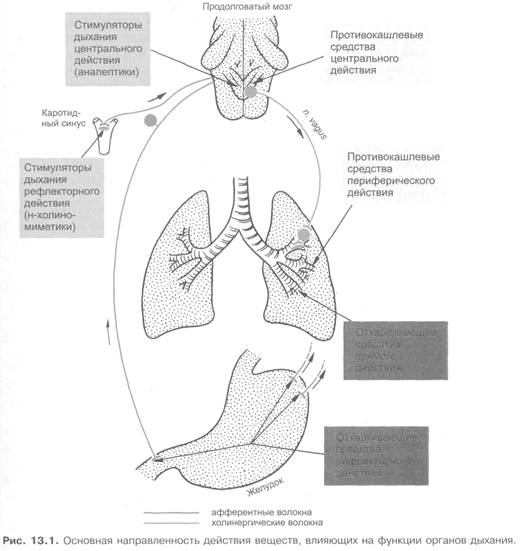
По основной направленности действия стимуляторы дыхания подразделяются на следующие группы (рис. 13.1):
- Средства, непосредственно активирующие центр дыхания, — бемегрид, кофеин, этимизол.
- Средства, стимулирующие дыхание рефлекторно, — цититон, лобелина гидрохлорид.
- Средства смешанного типа действия (1+2) — кордиамин, углекислота.
К средствам, оказывающим прямое возбуждающее влияние на центр дыхания, относятся психостимулирующее средство и аналептик кофеин (см. главу 11; 11.6), аналептик бемегрид (см. главу 12) и препарат этимизол. Последний занимает особое положение среди центрально действующих стимуляторов дыхания. Он активирует подкорковые образования головного мозга и центры продолговатого мозга. Однако от типичных аналептиков этимизол отличается угнетающим влиянием на кору головного мозга, поэтому в практической медицине его используют не только как стимулятор дыхания, но также в психиатрии в качестве успокаивающего средства при состояниях тревоги. Вводят препарат внутрь и парентерально.
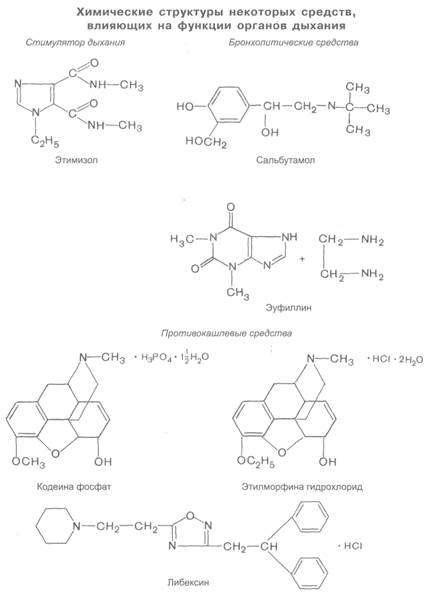 Рефлекторно действующими стимуляторами дыхания являются н-холиномиметики цититон и лобелина гидрохлорид (см. главу 3; 3.4). Механизм их действия заключается в том, что они возбуждают н-холинорецепторы синокаротидной зоны, откуда афферентные импульсы поступают в продолговатый мозг, и повышают активность дыхательного центра. Указанные н-холиномиметики действуют кратковременно (в течение нескольких минут). Вводить их следует только внутривенно.
Рефлекторно действующими стимуляторами дыхания являются н-холиномиметики цититон и лобелина гидрохлорид (см. главу 3; 3.4). Механизм их действия заключается в том, что они возбуждают н-холинорецепторы синокаротидной зоны, откуда афферентные импульсы поступают в продолговатый мозг, и повышают активность дыхательного центра. Указанные н-холиномиметики действуют кратковременно (в течение нескольких минут). Вводить их следует только внутривенно.
У средств смешанного типа действия центральный эффект дополняется стимулирующим влиянием на хеморецепторы каротидного клубочка. К таким препаратам относятся аналептик кордиамин (см. главу 12) и углекислота. Как известно, последняя является физиологическим стимулятором дыхания.
В медицинской практике применяют сочетание 5-7% СО2 и 93-95% О2 Такая смесь получила название карбоген. При ингаляции карбогена здоровым человеком объем дыхания увеличивается в 5-8 раз. Возбуждение дыхания происходит главным образом благодаря снижению в центре дыхания уровня рН и накоплению ионов Н+. Считают, что ионы водорода стимулируют клетки дыхательного центра не непосредственно, а через специальные хеморецепторные образования, расположенные в продолговатом мозге вблизи центра дыхания. Определенное значение в действии СО2 на дыхание имеют и рефлексы с синокаротидной зоны. Стимулирующее действие СО2 на дыхание развивается в течение первых 5-6 мин. При этом улучшается и общее кровообращение. Имеются данные о том, что СО2 увеличивает мозговой кровоток.
Применяют стимуляторы дыхания при легких отравлениях опиоидными анальгетиками, окисью углерода, при асфиксии новорожденных, для восстановления необходимого уровня легочной вентиляции в посленаркозном периоде и т.д. В целом стимуляторы дыхания используют редко. При гипоксических состояниях обычно предпочитают прибегать к вспомогательному или искусственному дыханию.
13.2. ПРОТИВОКАШЛЕВЫЕ СРЕДСТВА
Выделяют две группы противокашлевых средств (см. рис. 13.1).
1. Средства центрального действия.
а) Наркотического типа действия (кодеин, этилморфина гидрохлорид).
б) Ненаркотические препараты (глауцина гидрохлорид, тусупрекс).
2. Средства периферического действия (либексин).
Наиболее широкое распространение в практической медицине получили препараты центрального действия, угнетающие центральные звенья кашлевого рефлекса, локализованные в продолговатом мозге. К этой группе относятся хорошо известные кодеин, а также этилморфина гидрохлорид.
Кодеин (метилморфин) является алкалоидом опия фенантренового ряда (группа морфина; см. главу 8; 8.1). Обладает выраженной противокашлевой активностью. Кроме того, он оказывает слабое болеутоляющее действие. В терапевтических дозах кодеин не угнетает дыхательный центр или это влияние выражено в незначительной степени. При систематическом использовании препарата возможен такой побочный эффект, как запор. Длительное применение кодеина сопровождается развитием привыкания и в некоторых случаях лекарственной зависимости (психической и физической).
В качестве препаратов выпускают кодеин (основание) и кодеина фосфат. Кроме того, кодеин входит в состав ряда комбинированных препаратов: микстуры Бехтерева (содержит настой травы горицвета, натрия бромид и кодеин), таблеток «Кодтерпин» (кодеин с отхаркивающими средствами — натрия гидрокарбонатом и терпингидратом) и др.
К этой группе веществ относится также этилморфина гидрохлорид (дионин), получаемый синтетическим путем из морфина. По влиянию на кашлевой центр этилморфина гидрохлорид аналогичен кодеину, но несколько более активен.
Сильным противокашлевым эффектом обладают опиоидные анальгетики (морфина гидрохлорид и др.). Однако они вызывают угнетение центра дыхания. Кроме того, эти препараты более опасны в отношении развития лекарственной зависимости. Поэтому их можно использовать лишь эпизодически при неэффективности кодеина и других противокашлевых веществ.
Создан ряд препаратов, более избирательно угнетающих кашлевой центр и не вызывающих лекарственной зависимости. Их называют ненаркотическими противокашлевыми средствами. К ним относятся глауцина гидрохлорид (глаувент), окселадина цитрат (тусупрекс). Глауцин является алкалоидом растительного происхождения, тусупрекс получен синтетическим путем. Переносятся препараты хорошо. Глауцин может вызывать головокружение, тошноту.
К противокашлевым средствам периферического действия относится либексин. Механизм его действия связывают с анестезирующим влиянием на слизистую оболочку верхних дыхательных путей, а также с некоторыми бронхолитическими свойствами. На ЦНС он не влияет. Лекарственная зависимость к либексину не развивается. Таким образом, и либексин относится к ненаркотическим противокашлевым средствам.
При сухости слизистой оболочки бронхов, вязком и густом секрете бронхиальных желез уменьшить кашель можно путем увеличения секреции желез слизистой оболочки бронхов, а также разжижением секрета. С этой целью назначают отхаркивающие средства, в том числе ингаляции аэрозолей щелочных жидкостей.
13.3. ОТХАРКИВАЮЩИЕ СРЕДСТВА
Эта группа веществ предназначена для облегчения отделения слизи (мокроты), продуцируемой бронхиальными железами. Имеются две разновидности отхаркивающих средств (см. рис. 13.1): 1) рефлекторного действия, 2) прямого действия.
Рефлекторно действуют препараты ипекакуаны и препараты термопсиса (настои, экстракты). Содержащиеся в них алкалоиды (а в термопсисе и сапонины) при введении внутрь вызывают раздражение рецепторов желудка. При этом рефлекторно увеличивается секреция бронхиальных желез, повышается активность мерцательного эпителия, усиливаются сокращения мышц бронхов. Мокрота становится более обильной, менее вязкой, и отделение ее с кашлем облегчается.
В высоких дозах отмеченные препараты рефлекторно вызывают рвоту, однако для этих целей не используются.
К отхаркивающим средствам прямого действия относятся препараты, разжижающие секрет (муколитические средства).
Активным муколитическим средством является ацетилцистеин (бронхолизин, мукосольвин). Эффект связан с наличием в молекуле свободных сульфгидрильных групп, которые разрывают дисульфидные связи протеогликанов, что вызывает деполимеризацию и снижение вязкости мокроты. Разжижение и увеличение объема мокроты облегчают ее отделение. Применяют ацетилцистеин ингаляционно, иногда парентерально. Созданы также пролонгированные препараты для приема внутрь (АЦЦ-100, АЦЦ-200, АЦЦ-лонг). Из кишечника ацетилцистеин всасывается полностью, но биодоступность у него низкая (примерно 10%), так как большая часть препарата метаболизируется в печени при первом прохождении через нее. Сходным по строению и действию препаратом является карбоцистеин (бронхокод, мукодин).
К эффективным муколитическим и отхаркивающим средствам относятся амброксол (амбробене) и бромгексин, имеющие сходное химическое строение. Муколитическое действие препаратов обусловлено деполимеризацией мукопротеинов и мукополисахаридов мокроты, что приводит к ее разжижению. Считают также, что фармакотерапевтический эффект обоих препаратов связан со стимуляцией продукции эндогенного поверхностно-активного вещества (сурфактанта), образующегося в альвеолярных клетках. При этом нормализуется секреция бронхиальных желез, улучшаются реологические свойства мокроты, уменьшается ее вязкость, облегчается выделение мокроты из бронхов. Эффект развивается через 30 мин и сохраняется 10-12 ч. Вводят препараты внутрь. Из побочных эффектов иногда отмечаются тошнота, рвота, аллергические реакции.
К этой группе относятся также препараты протеолитических ферментов — трипсин кристаллический, химотрипсин кристаллический, дезоксирибонуклеаза (ДНКаза). Препарат рекомбинантной α-ДНКазы выпускается под названием пульмозим. Применяется в качестве муколитика при муковисцидозе. Вводят ингаляционно. Применяют также препараты, оказывающие прямое действие на железы слизистой оболочки бронхов и усиливающие их секрецию, например калия йодид.
Натрия гидрокарбонат также разжижает мокроту, а возможно, и несколько повышает бронхиальную секрецию. Калия йодид и натрия гидрокарбонат назначают внутрь и ингаляционно (в аэрозоле), растворы трипсина кристаллического, химотрипсина кристаллического, ДНКазы — ингаляционно (в аэрозоле).
К отхаркивающим средствам относятся препараты корня алтея, корня истода, корня солодки, терпингидрат, натрия бензоат.
13.4. СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ БРОНХОСПАЗМАХ
В обычных условиях тонус мышц бронхов поддерживается за счет холинергических нервов, возбуждение которых приводит к бронхоспастическому эффекту. Симпатическая иннервация бронхов отсутствует. Однако в бронхах имеются неиннервируемые β2-адренорецепторы, на которые действует циркулирующий адреналин и вводимые извне адренотропные вещества. Стимуляция β2-адренорецепторов сопровождается бронходилатирующим эффектом.
В процессе развития бронхоспастических состояний, и в том числе бронхиальной астмы, возникает гиперреактивность бронхов к действию разнообразных стимулов, провоцирующих бронхоспазм. К их числу относятся аллергены, инфекция, химические вещества, вдыхание холодного воздуха, стресс и др.
В формировании воспалительной реакции, лежащей в основе гиперреактивности бронхов, большую роль играют так называемые медиаторы воспаления. Они продуцируются в клетках эпителия бронхов, в тучных клетках, макрофагах альвеол, в нейтрофилах, эозинофилах, моноцитах. Тучные клетки легких обычно содержат гистамин, аденозин, хемотаксические факторы для нейтрофилов и эозинофилов. Воспалительный процесс индуцирует продукцию многих других медиаторов воспаления — лейкотриенов, простагландинов, тромбоксана, фактора, активирующего тромбоциты (ФАТ). Эти вещества оказывают бронхоспастическое действие, вызывают отек слизистой оболочки бронхов, повышают проницаемость сосудов, способствуют инфильтрации слизистой оболочки лейкоцитами, вызывают гиперсекрецию слизи. Все это отягощает течение бронхоспазмов. Поэтому тактика их лечения заключается не только в устранении действия провоцирующих стимулов (если они известны) и в бронхолитической терапии, но и в подавлении воспалительного процесса. Исходя из имеющихся данных, препараты, применяемые для лечения бронхиальной астмы и других бронхоспастических состояний, можно представить в виде следующих групп.
I. Средства, расширяющие бронхи (бронхолитики).
1. Вещества, стимулирующие β2-адренорецепторы (сальбутамол, фенотерол, тербуталин, изадрин, орципреналина сульфат, адреналина гидрохлорид).
2. М-холиноблокаторы (атропина сульфат, метацин, ипратропия бромид).
3. Спазмолитики миотропного действия (теофиллин, эуфиллин).
II. Средства, обладающие противовоспалительной и бронхолитической активностью.
1. Стероидные противовоспалительные средства (гидрокортизон, дексаметазон, триамцинолон, беклометазон).
2. Противоаллергические средства (кромолин-натрий, кетотифен).
3. Средства, влияющие на систему лейкотриенов.
А. Ингибиторы 5-липоксигеназы (зилеутон).
Б. Блокаторы лейкотриеновых рецепторов (зафирлукаст, монтелукаст).
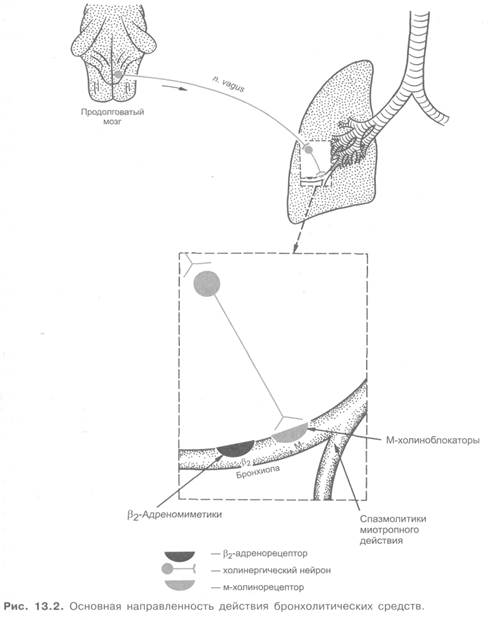
Из группы бронхолитиков большой интерес представляют вещества, стимулирующие β2-адренорецепторы (см. главу 4; 4.2; рис. 13.2).
В настоящее время при бронхоспазмах применяют в основном препараты, возбуждающие преимущественно β2-адренорецепторы, — сальбутамол (вентолин, сальбен, сальгим, сальтос), фенотерол (беротек Н). Они в значительно меньшей степени вызывают тахикардию, чем β-адреномиметики неизбирательного действия. Их применяют обычноингаляционно.
β2-Адреномиметики являются быстродействующими бронходилататорами. Кроме того, они способствуют отделению мокроты.
За последние годы созданы длительно действующие β2-адреномиметики салметерол (серевент), формотерол (форадил) и др. Так, при ингаляции салметерола бронхорасширяющий эффект сохраняется около 12 ч, тогда как для сальбутамола он ограничивается 4-6 ч. Для лечения бронхиальной астмы предложен препарат, включающий салметерол и глюкокортикоид с преимущественно местным действием флутиказона пропионат (фликсотид). Такой комбинированный препарат называется серетид мультидиск. В данном случае бронхорасширяющий эффект салмотерола сочетается с противовоспалительным действием флутиказона, что весьма целесообразно для эффективного лечения бронхиальной астмы. Вводится препарат с помощью порошкового ингалятора.
β2-Адреномиметики могут вызывать тремор, тахикардию, беспокойство, аритмию и другие побочные эффекты.
Одним из препаратов этой группы является также изадрин (изопреналина гидрохлорид), который стимулирует β1,- и β2-адренорецепторы. Он используется для устранения бронхоспазмов. Назначают его для этой цели в растворах ингаляционно. В связи с влиянием на β-адренорецепторы сердца изадрин может вызывать учащение и усиление сердечных сокращений. Артериальное давление при таком применении изадрина практически не изменяется.
Несколько более выраженной тропностью к адренорецепторам бронхов обладает β-адреномиметик орципреналина сульфат (алупент). По бронхолитической эффективности он аналогичен изадрину, но действует более продолжительно. Влияет на β2- и β1-адренорецепторы. Вводят орципреналин парентерально, внутрь и ингаляционно в виде аэрозолей.
При бронхоспазмах нередко используют адреналин, влияющий на α- и β (β1, и β2)-адренорецепторы. При подкожном введении он быстро купирует спазм бронхов разной этиологии, а также уменьшает отек слизистой оболочки. Действует непродолжительно. Из побочных эффектов возможны повышение артериального давления, тахикардия, увеличение минутного объема сердца.
В качестве бронхолитика иногда используют симпатомиметик эфедрин (α- и β-адреномиметик непрямого действия). По активности он уступает адреналину, но действует продолжительнее. Применяется обычно с профилактической целью. Из побочных эффектов, помимо отмеченных для адреналина, наблюдается возбуждение ЦНС. Если оно выражено в значительной степени, его можно уменьшить применением седативных или снотворных веществ. Следует учитывать, что к эфедрину развивается лекарственная зависимость.
Таким образом, один из путей устранения бронхоспазма заключается в активации β2-адренорецепторов бронхов и связанной с ними аденилатциклазы, что приводит к повышению внутриклеточного содержания цАМФ (в свою очередь это уменьшает концентрацию ионов кальция внутри клеток) и снижению тонуса гладких мышц бронхов. Одновременно под влиянием веществ с β2-адреномиметической активностью снижается высвобождение из тучных клеток соединений, вызывающих спазм бронхиол (гистамина, медленно реагирующей субстанции анафилаксии и др.) (рис. 13.3).
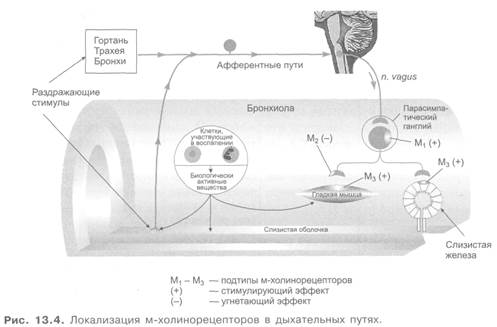
Может быть использован и другой принцип. Бронхолитическими свойствами обладают вещества, блокирующие холинергическую иннервацию бронхов, особенно м-холиноблокаторы (см. главу 3; 3.3; рис. 13.4). При этом происходит также снижение высвобождения из тучных клеток спазмогенных веществ. По активности при бронхиальной астме м-холиноблокаторы уступают адреномиметикам. Из этой группы препаратов применяют (особенно при бронхоспазмах неаллергической природы, связанных с повышенным тонусом холинергической иннервации) атропина сульфат, платифиллин, метацин и ипратропия бромид, являющиеся неизбирательными блокаторами м-холинорецепторов. Недостатками препаратов этой группы являются снижение ими секреции бронхиальных, слюнных и других желез, тахикардия, нарушение аккомодации (менее выражено при применении метацина).

Выраженный эффект наблюдается при ингаляции ипратропия (атровент). Действие этого препарата наступает медленнее, чем у β-адреномиметиков; сохраняется около 6 ч. В ЦНС он не проникает (так как является четвертичным аммониевым соединением).
Ипратропий выпускается также в комбинации с фенотеролом (такой препарат называется беродуал Н).
К бронхолитикам из группы четвертичных аммониевых соединений, помимо метацина и ипратропия, относится также новый препарат тиотропий (табл. 13.1).
| Таблица 13.1 М-холинорецепторы в дыхательных путях | |||||
| Подтип рецепторов1 | Эффекты активации м-холинорецепторов | М-холиноблокаторы, эффективные при хронической обструктивной болезни легких и бронхиальной астме | |||
| нейротропный | гладкие мышцы дыхательных путей | слизистые железы | неизбирательного действия на м-холинорецепторы | избирательного (преимущественного) действия | |
| М1 | Возбуждающие рецепторы в парасимпатических ганглиях; их стимуляция облегчает ганглионарную передачу и вызывает бронхоспазм | Стимуляция секреции желез слизистой оболочки носовых ходов | |||
| М2 | Угнетающие ауторецепторы, локализующиеся пресинаптически на постганглионарных парасимпатических окончаниях; их стимуляция уменьшает бронхоспазм | Функция не выяснена | Ипратропий Метацин Атропин Платифиллин2 | ||
| М3 | Возбуждающие рецепторы; их стимуляция вызывает бронхоспазм | Повышение секреции желез слизистой оболочки носовых ходов и бронхов; регуляция тонуса сосудов в слизистой оболочке носа | Тиотропий3 (М3+М1) | ||
| 1 В стенках альвеол обнаружены М4-холинорецепторы. Функция их неизвестна. 2 Кроме того, оказывает миотропное спазмолитическое и ганглиоблокирующее действие. 3 Блокирует М3-холинорецепторы в 2,5 раза более продолжительно, чем М-холинорецепторы. |
Действует он в основном на м3- и м1-холинорецепторы, но более стойко и длительно связывается с первыми. Поэтому нередко этот препарат относят к преимущественным блокаторам м3-холинорецепторов. Он активнее ипратропия и действует более продолжительно. Однако скорость развития эффекта выше у ипратропия. Максимальный эффект тиотропия развивается через 1,5-2 ч. Назначают тиотропий 1 раз в сутки ингаляционно (в виде порошка в специальных ингаляторах). Основной побочный эффект — сухость слизистой оболочки ротовой полости.
Расширение бронхов достигается, помимо их иннервации, применением препаратов, действующих непосредственно на гладкие мышцы бронхиол. Из миотропных спазмолитиков для бронхолитического действия используют препараты теофиллина, включая эуфиллин (аминофиллин). Последний представляет собой смесь теофиллина (1,3-диметилксантин) с 1,2-этилендиамином.
Отмечено, что в больших концентрациях теофиллин ингибирует фосфодиэстеразу и благодаря этому повышает содержание цАМФ. Как и в случае действия β2-адреномиметиков, последнее сопровождается уменьшением внутриклеточной концентрации ионов кальция и расслаблением мышц бронхов. Одно время это считали причиной бронхолитического действия теофиллина. Однако в дальнейшем выяснилось, что теофиллин угнетает фосфодиэстеразу в концентрациях, значительно превышающих терапевтические. Было высказано предположение, что в диапазоне терапевтических концентраций бронхолитическое действие теофиллина связано с блоком аденозиновых рецепторов бронхиол. Ряду авторов удалось также показать, что теофиллин препятствует высвобождению гистамина из тучных клеток, вызываемому аденозином. Однако и эта гипотеза подвергается сомнению, так как было синтезировано близкое к теофиллину соединение (3-пропилксантин), которое обладает выраженной бронхолитической активностью и не блокирует аденозиновые рецепторы бронхиол.
Теофиллин снижает также давление в малом круге кровообращения, улучшает кровоток в сердце, почках и, очевидно, в головном мозге (при сужении сосудов). Обладает умеренным диуретическим эффектом. Стимулирует деятельность миокарда; потребность сердца в кислороде при этом возрастает. Оказывает возбуждающее влияние на ЦНС.
За последние годы теофиллин, особенно в виде длительно действующих препаратов (продолжительностью 8, 12 и 24 ч), стали широко применять для профилактики бронхоспазмов. По эффективности препараты теофиллина сопоставимы с β-адреномиметиками. Однако следует учитывать небольшую терапевтическую широту теофиллина. Показано, что токсические концентрации вещества в крови превышают терапевтические всего в 2-4 раза. Поэтому дозировать препараты следует с осторожностью. В идеале желательно подбирать оптимальную дозу, сопоставляя концентрацию вещества в крови и выраженность эффекта. При длительном применении целесообразно периодически определять концентрацию теофиллина в плазме крови, тем более что скорость абсорбции и t1/2 варьируют в довольно широких пределах.
Теофиллин почти полностью всасывается из пищеварительного тракта. Метаболизируется в печени. Выводится почками. Следует учитывать, что теофиллин проходит через плаценту и выделяется с молоком кормящей матери.
Применяют препараты теофиллина внутрь, ректально и внутривенно. При назначении внутрь они могут вызывать диспепсические явления. Раздражающее действие наблюдается и при введении эуфиллина в прямую кишку. Побочные эффекты довольно разнообразны и возникают относительно часто. Возможны головная боль, головокружение, тошнота, рвота, задержка мочеотделения, аритмия, возбуждение, бессонница, в токсических дозах — судороги.
При лечении больных бронхиальной астмой и другими бронхоспазмами аллергической природы, помимо истинных бронхолитиков, широко применяют противовоспалительные и противоаллергические средства (см. главу 25). К таким препаратам относятся глюкокортикоиды. Показано, что они стабилизируют мембраны тучных клеток и их гранул, сенсибилизируют β2-адренорецепторы и оказывают некоторое прямое бронхолитическое действие. Важное (если не основное) значение имеет наличие у глюкокортикоидов выраженной противовоспалительной и иммунодепрессивной активности, что весьма благоприятно сказывается на течении бронхиальной астмы.
Глюкокортикоиды применяют в виде аэрозолей (беклометазона дипропионат, флутиказона пропионат, будесонид) и внутрь для системного действия (дексаметазон, триамцинолон и др.). Последние два препарата можно использовать и ингаляционно. При необходимости внутривенно вводят гидрокортизон. При применении аэрозолей глюкокортикоидов возможны развитие кандидамикоза ротовой полости и глотки, кашель.
Большой интерес представляет также синтетический противоаллергический препарат кромолин-натрий (динатрия хромогликат, интал, кропоз). Согласно одной из гипотез, принцип его действия заключается в том, что он блокирует вхождение в тучные клетки ионов кальция и стабилизирует мембрану тучных клеток и их гранул. Все это в целом должно препятствовать процессу дегрануляции тучных клеток и высвобождению из них спазмогенных веществ (гистамина, МРС-А и др.). Однако эта точка зрения ставится под сомнение, так как кромолин-натрий оказывает очень слабое и непостоянное действие на тучные клетки, выделенные из легких человека (сальбутамол в этих исследованиях оказался значительно более активным).
Кромолин-натрий применяют для профилактики приступов бронхиальной астмы. Вводят его ингаляционно.
Сходным с кромолин-натрием препаратом является недокромил.
К противоаллергическим препаратам относится также кетотифен (задитен). По имеющимся представлениям, он тормозит высвобождение медиаторов аллергии из тучных клеток. Применяют его для предупреждения приступов бронхиальной астмы, а также при сенной лихорадке, рините и других аллергических реакциях немедленного типа.
Из побочных эффектов отмечается седативное действие, иногда тромбоцитопения.
Принимают препарат внутрь 2 раза в день. Действие развивается медленно; максимальный эффект отмечается через 3-4 нед.
Date: 2015-07-01; view: 956; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |