
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кинетика элиминации первого и нулевого порядка
После введения лекарства в организм, его концентрация в крови вначале возрастает от нуля до некоторого уровня (при внутривенном введении это происходит практически мгновенно), а затем начинает снижаться, вследствие процессов элиминации и распределения.
Поскольку процесс элиминации лекарства носит вид ферментативной реакции (в случае его биотрансформации) или простого массопереноса (в случае экскреции), то очевидно, что он подчиняется законам химической кинетики и описывается классическим уравнением Михаэлиса-Ментен:
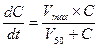
При этом, фактически, при введении в организм лекарственного средства возникают 2 возможные ситуации:
· Если уровень концентрации лекарства в организме (С) значительно меньше, чем величина его полумаксимальной скорости элиминации (V50), т.е. С<<V50, уравнение сводится к виду:
 .
.
Это дифференциальное уравнение 1-го порядка (поэтому и кинетика такой элиминации получила название кинетики первого порядка), которое показывает, что скорость элиминации лекарства пропорциональна его концентрации в организме. Решая это уравнение находим, что: С=С0´е-kt.
Таким образом, кинетикой элиминации первого порядка называют такой вид элиминации лекарства, при котором скорость удаления лекарственного вещества из крови пропорциональна его концентрации в организме и в единицу времени элиминируется постоянная доля (фракция) лекарства. График кинетики элиминации первого порядка имеет вид экспоненциальной кривой и может быть линеаризован в полулогарифмических координатах.
Большинство современных лекарств элиминируется кинетикой первого порядка.
· Если уровень концентрации лекарства в организме значительно превышает полумаксимальную скорость его элиминации (C>>V50), то уравнение сводится к виду:
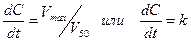 .
.
Это дифференциальное уравнение нулевого порядка, поэтому такой вид кинетики называют кинетикой элиминации нулевого порядка. Данное уравнение показывает, что скорость элиминации лекарства является величиной постоянной и не зависит от его концентрации в организме. Решая уравнение можно найти, что С=С0-kt.
Таким образом, кинетикой элиминации нулевого порядка называют такой вид элиминации, при котором скорость удаления лекарственного вещества из организма постоянна и в единицу времени элиминируется постоянное количество лекарственного вещества. График кинетики нулевого порядка имеет вид прямой линии в обычных координатах.
Кинетика элиминации нулевого порядка встречается относительно редко:
[ При инфузионном капельном введении лекарственного средства с постоянной скоростью. В этом случае она описывает фазу поступления лекарства.
[ При абсорбции лекарства из депо-форм (лекарственные формы продленного действия), которая протекает также с постоянной скоростью.
[ При насыщаемом метаболизме, т.е. в тех случаях, когда вводимая доза лекарства превышает возможности ферментов метаболизма по утилизации лекарственного средства. Такая ситуация возникает при введении высоких доз этанола, ацетилсалициловой кислоты, фенитоина.
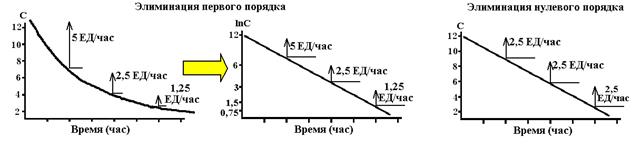
Схема 9. Типичные формы фармакокинетических кривых при различных вариантах кинетики. Слева представлена кривая элиминации лекарства в соответствии с кинетикой первого порядка. В центре – та же кривая после преобразования оси концентраций в логарифмическую форму. Справа представлена кривая кинетики нулевого порядка.
1. Элиминация первого порядка. Термин «первого порядка» обозначает, что скорость элиминации пропорциональна концентрации вещества, то есть, чем выше концентрация тем выше количество вещества, которое элиминируется в единицу времени. В результате концентрация лекарства в плазме снижается во времени экспоненциально (см. рис. 1-5, слева). Лекарственные средства с элиминацией первого порядка характеризуются постоянной величиной периода полуэлиминации, независимо от содержания вещества в организме. Концентрация такого лекарства в крови за каждый период полусуществования будет понижаться на 50%. Большинство лекарств, при клиническом применении, обладают кинетикой первого порядка.
Элиминация нулевого порядка. Термин «нулевой порядок» обозначает, что скорость элиминации постоянна и не зависит от концентрации вещества (см. рис. 1-5, справа). Механизмы элиминации некоторых веществ являются насыщенными уже при низких концентрациях этих соединений. Как результат этого, концентрация таких лекарств в плазме понижается линейно во времени. Это характерно для этанола (при широком диапазоне его концентраций в организме) и фенитоина, а также для аспирина при высоких терапевтических или токсических концентрацях.
Основной целью лекарственной терапии является обеспечение в организме терапевтического уровня лекарства. Для этого используют введение вначале нагрузочной, а затем – поддерживающих доз лекарства. Напомним формулы для расчета этих доз:
Dн=Vd´Cтер
Dп=Cl´Cтер´t, где t - интервал между введениями.
При непрерывном внутрисосудистом введении между поддерживающей и нагрузочной дозами (скоростями введения) существует следующая зависимость:
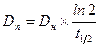 .
.
Период полуэлиминации (t½, мин-1) – это время, необходимое для снижения концентрации лекарственного вещества в крови ровно наполовину. При этом не играет роли каким путем достигается снижение концентрации – при помощи биотрансформации, экскреции или же за счет сочетания обоих процессов. Обычно период полуэлиминации определяют из соотношения:
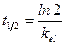
Все три показателя Vd, Cl и t½ связаны между собой следующими соотношениями:
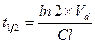 и
и 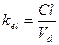 .
.
Концентрация лекарственного средства в плазме крови, которая достигается при условии, что скорость введения лекарства в организм уравновешивает скорость его выведения получила название стационарной концентрации лекарственного вещества (СSS). Из уравнения:
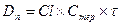 следует, что
следует, что 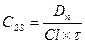 *.
*.
Таким образом, величина CSS прямо пропорциональна вводимой дозе и обратно пропорциональна интервалу между введениями лекарства. Поскольку лекарственное вещество вводится через дискретные интервалы времени, то очевидно, что величина СSS не будет постоянной, а начнет колебаться в каком-то диапазоне от максимального уровня (вскоре после введения лекарства) до минимального уровня перед очередным приемом лекарства. Эти границы колебаний не трудно рассчитать, они составляют:
 и
и 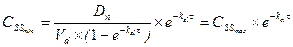
Различают 3 вида эквивалентности:
[ Химическая (фармацевтическая) эквивалентность – означает, что 2 лекарственных препарата содержат одно и то же лекарственное вещество в равных количествах и в соответствии с действующими стандартами. При этом неактивные ингридиенты лекарственных препаратов могут различаться.
[ Биоэквивалентность – означает, что два химически эквивалентных лекарственных препарата различных производителей при введении в организм человека в равных дозах и по одинаковой схеме всасываются и поступают в системный кровоток в равной степени, т.е. обладают сопоставимыми показателями биодоступности.
[ Терапевтическая эквивалентность. Данное понятие означает, что 2 лекарственных препарата, содержащих одно и то же лекарственное средство, которые применяют в равных дозах и по одинаковой схеме вызывают сопоставимый терапевтический эффект. Терапевтическая эквивалентность не зависит от биоэквивалентности лекарственных препаратов. Два препарата могут быть биологически эквивалентны, но при этом иметь разную терапевтическую эквивалентность.
Основным критерием биоэквивалентности является отношение площадей под фармакокинетической кривой для двух изучаемых лекарственных средств, а также отношение максимальных концентраций этих лекарств в крови пациента:
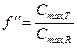 и
и 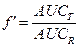
Считают, что допустимыми колебаниями этих параметров является диапазон 0,8-1,2 (т.е. биодоступность двух сравниваемых лекарств не должна различаться более чем на 20%).
Цитоплазматические рецепторы. Находятся в цитозоле клетки. Лиганд рецептора (липофильное вещество) проникает через ее мембрану и связывается с рецептором. В покое эти рецепторы экранированы особым белком теплового шока (hsp-белок). При связывании с лигандом рецептор освобождает этот белок и образует пары с другими рецепторами данного семейства. Затем, активированный рецептор поступает в ядро клетки, где связывается с особыми рецепторными последовательностями нуклеотидов ДНК и регулирует экспрессию генов. К данному семейству относятся рецепторы для стероидных гормонов, витаминов А и D, тиреоидных гормонов.
Трансмембранные рецепторы, связанные с ионными каналами. Представляют собой белки, которые формируют в мембране ионный канал. При взаимодействии лиганда с рецепторной субъединицей белка проницаемость ионного канала меняется. К данной группе рецепторов относят:
] Н-холинорецепторы, связанные с Na+-каналами. При взаимодействии с ацетилхолином рецептор открывает натриевый канал и под влиянием тока ионов натрия в клетку возникает деполяризация мембраны и генерируется потенциал действия.
] ГАМКА-рецепторы, которые связаны с Cl--каналами. При взаимодействии с g-аминомасляной кислотой рецептор открывает канал и обеспечивает поступление в клетку ионов хлора. Возникает гиперполяризация мембраны и переход ее в состояние покоя.
Трансмембранные рецепторы, связанные с G-белками. Эти рецепторы состоят из 3 субъединиц. Рецепторный белок располагается на наружной стороне мембраны. При взаимодействии с лигандом он передает сигнал на внутримембранный G-белок, который за счет энергии ГТФ перемещается к внутренней стороне мембраны и изменяет активность эффекторных белков. Эффекторные белки расположены на внутренней стороне мембраны и представляют собой ферменты, которые образуют «вторичные мессенджеры» – молекулы-посредники, которые передают сигнал в клетку и вызывают развитие ответной реакции. В качестве эффекторных белков выступают:
] Аденилатциклаза – это фермент, который гидролизует АТФ с образованием циклического АМФ
] Гуанилатциклаза – это фермент, который гидролизует ГТФ с образованием цГМФ. Молекула цГМФ активирует в клетке цГМФ-зависимые протеинкиназы, которые также фосфорилируют белки.
] Фосфолипаза
Трансмембранные рецепторы-ферменты. Данный вид рецепторов представлен молекулами, состоящими из 2 субъединиц. Рецепторная субъединица располагается с наружной стороны мембраны, а каталитическая (т.е. обладающая ферментативногй активностью) – прошивает мембрану клетки насквозь. При взаимодействии с лигандом рецепторная субъединица активирует каталитическую часть молекулы. В качестве каталитической субъединицы выступают:
] Тирозинкиназы – ферменты, которые фосфорилируют остатки тирозина в молекулах белков. К такому типу рецепторов относится инсулиновый рецептор.
] Серин-треонинкиназы – ферменты, которые фосфорилируют остатки серина и треонина в молекулах белков. К такому типу относят некоторые из интерлейкиновых рецепторов.

Градуальные кривые зависимости «доза-эффект». А – зависимость изменения частоты сердечных сокращений от дозы лекарства в нормальных координатах, В – та же кривая в полулогарифмических координатах (одна из шкал переведена в форму десятичных логарифмов), С – кривая связывания того же вещества с рецепторами миокарда.
Emax – максимальный эффект, Bmax – максимальное число связанных рецепторов, ЕС50 – концентрация лекарства при которой возникает эффект равный половине максимального, Kd – константа диссоциации вещества от рецептора, при которой связано 50% рецепторов.
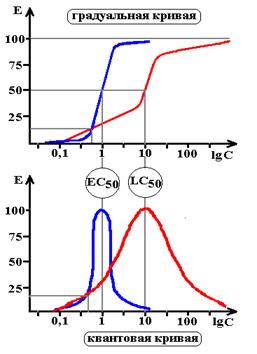
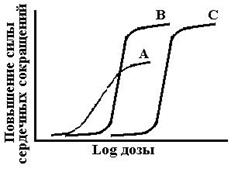
Схема 4. Сравнительная характеристика кардиотонических средств. Как следует из представленных графиков EC50,A<EC50,B<EC50,C – средство А самое сильное, но Emax,A<Emax,B=Emax,C – средства В и С самые эффективные.
Терапевтический индекс – это соотношение между токсической и эффективной дозами лекарства, которые вызывают появление полумаксимального эффекта. ТИ=TD50/ED50. Чем больше величина терапевтического индекса, тем более безопасным является лекарство.
Терапевтический коридор – это диапазон эффективных концентраций лекарственного вещества в крови, которые необходимо создать и поддерживать в организме, чтобы обеспечить достижение желаемого терапевтического действия.
Терапевтическая широта (терапевтическое окно) – это диапазон доз между минимальной терапевтической и минимальной токсической дозами лекарства (ТШ=TD10/ED10). Терапевтическая широта более корректный показатель безопасности лекарства, поскольку он позволяет учитывать степень нарастания нежелательных эффектов на кривой «доза-эффект».
Рецептор (лат. recipere – получать) – специфические молекулярные компоненты клетки, которые при взаимодействии с лигандами подвергаются конформационным изменениям и за счет воздействия на эффекторные системы клетки изменяют функции ткани и органа в целом.
Согласно теории A.J. Clark очевидно, что максимальный эффект лекарства должен возникать в тот момент, когда заняты все рецепторы, а 50% эффект – если занята их половина. Однако, имеются лекарства, которые могут вызвать максимальный эффект даже в том случае, если они оккупировали менее 100% рецепторов. Такая ситуация, когда часть рецепторов оказывается избыточной и не нужна для достижения максимального эффекта получила название «молчащих» рецепторов ткани.
места инертного связывания – молекулярные компоненты с которыми могут взаимодействовать биологически активные вещества, не вызывая их конформационных изменений и передачи сигнала на эффекторные системы.
Антагонисты -это лекарственные вещества, которые связываются с рецепторами, но не вызывают их активации. Конкурентные антагонисты – это вещества, которые обратимо связываются с рецепторами без активации эффекторной системы этого рецептора. Фактически, конкурентный антагонист взаимодействует с рецепторами в том же самом месте, что и агонист и, следовательно, он конкурирует с агонистом за места связывания. Неконкурентный антагонист связывается с рецептором в участке, который функционально и морфологически отличается от связывающего агонист рецепторного сайта. Тем самым, неконкурентные антагонисты либо предотвращают взаимодействие агонистов с их специфическими связывающими сайтами, либо препятствуют процессу активации рецептора его агонистом
| Конкурентный антагонист | Неконкурентный антагонист |
| 1. Похож по строению на агонист. 2. Связывается с активным центром рецептора. 3. Смещает кривую «доза-эффект» вправо. 4. Антагонист снижает чувствительность ткани к агонисту (ЕС50), но не влияет на максимальный эффект (Еmax), который может быть достигнут при более высокой концентрации. 5. Действие антагониста может быть устранено высокой дозой агониста. 6. Эффект антагониста зависит от соотношения доз агониста и антагониста | 1. По строению отличается от агониста. 2. Связывается с аллостерическим участком рецептора. 3. Смещает кривую «доза-эффект» по вертикали. 4. Антагонист не изменяет чувствительность ткани к агонисту (ЕС50), но уменьшает внутреннюю активность агониста и максимальную реакцию ткани на него (Еmax). 5. Действие антагониста не может быть устранено высокой дозой агониста. 6. Эффект антагониста зависит только от его дозы. |
Парциальные агонисты – это вещества, которые связываются с рецепторами и вызывают их активацию, однако, даже если они займут все рецепторы, эти вещества не способны вызвать максимальный ответ для данного типа рецепторов. Действие парциального агониста будет зависеть от того, с какими рецепторами они взаимодействуют – с покоящимися или с рецепторами, которые уже активированы полными агонистами. Если парциальный агонист взаимодействует с покоящимися рецепторами, то он вызывает их активацию и ответ ткани возрастает с нуля до некоторой величины (»30-60%), т.е. это типичное агонистическое воздействие. Если парциальный агонист действует на ткань, рецепторы которой уже активированы полным агонистом, то он начинает вытеснять агонист из связи с рецептором и занимать его место.
Толерантность (привыкание). Под толерантностью понимают снижение ответной реакции организма на повторные введения лекарственного средства. Для того, чтобы восстановить реакцию на лекарство его приходится вводить во все бóльших и бóльших дозах.
Лекарственная зависимость – состояние психики и/или физическое состояние, которое является следствием воздействия на организм лекарственного средства и характеризуется специфическими поведенческими реакциями, трудно преодолимым стремлением повторно принимать лекарство, чтобы добиться особого психического эффекта или избежать дискомфорта при отсутствии лекарства в организме.
Кумуляция – повышение интенсивности ответной реакции организма на повторное введение лекарства. Различают 2 вида кумуляции:
] Материальная кумуляция – связана с накоплением в организме молекул лекарства, если оно вводится со скоростью большей, чем скорость элиминации этого лекарства. Материальная кумуляция имеет как свои положительные, так и отрицательные стороны. Лекарственные средства, способные к кумуляции имеют длительное действие, поэтому их можно применять нечасто и это удобно для пациента. Однако, за счет кумуляциилекарства достаточно высок риск развития интоксикации, если уровень лекарства в организме превысит токсический порог.
] Функциональная кумуляция – связана с тем, что фармакологический эффект лекарства сохраняется в организме больший период времени, чем само это лекарство. При повторном введении такого лекарства суммируются не его количества в организме, а эффекты этого лекарства.
Синергизм – вид взаимодействия при котором эффект комбинации превышает сумму эффектов каждого из веществ взятых по отдельности. Т.е. 1+1=3.
Потенцирование – вид лекарственного взаимодействия, при котором одно из лекарственных средств, которое само по себе не оказывает данного эффекта, может приводить к резкому усилению действия другого лекарственного средства. Т.е. 1+0=3.
Мутагенность – способность лекарственного средства вызывать дефекты генетической информации в генеративных клетках человека и передавать эти изменения по наследству.
Нежелательные эффекты – любые нежелательные изменения, которые как предполагают, обусловлены приемом данного лекарства, возникают при использовании этого лекарства в обычных терапевтических дозах и требуют для своего устранения специального лечения, снижения дозы лекарства или особого внимания при назначении этого лекарства в последующем.
[ ТИП А. Предсказуемые или прогнозируемые реакции. Эти реакции представляют собой количественно усиленные эффекты, которые входят в спектр фармакологической активности данного лекарственного средства. Такие реакции встречаются достаточно часто и являются дозозависимыми (т.е. чем выше используемая доза лекарства, тем выше вероятность развития этой реакции). К данному типу относят побочные реакции, вторичные эффекты лекарства.
[ ТИП В. Непредсказуемые или непрогнозируемые реакции. Это атипичные, т.е. качественно измененные реакции на лекарственное средство, которые не входят в спектр фармакологической активности лекарства. Данная группа нежелательных эффектов не может быть спрогнозирована без специальных тестов. Механизм развития реакций данного типа не всегда ясен. К этой группе относят аллергические реакции, идиосинкразию.
[ ТИП С. Реакции, связанные с длительным применением лекарственных средств. В эту группу включают кумуляцию, привыкание (толерантность), лекарственную зависимость.
[ ТИП D. Отдаленные реакции, проявляющиеся через несколько лет или поколений. В данную группу включают тератогенное, канцерогенное и мутагенное действие лекарств.
[ ТИП E. Реакции, возникающие в связи с прекращением приема лекарственных средств. Сюда относят синдромы рикошета и отмены.
Идиосинкразия – качественно измененная необычная реакция на лекарственное средство, обусловленная, как правило, генетическими аномалиями. Наиболее ярким примером идиосинкразии является злокачественная гипертермия, которая возникает после применения галота (средство для наркоза) или сукцинилхолина (миорелаксант) у 1 человека из каждых 20.000. Реакция связана с аутосомно-доминантным дефектом строения саркоплазматического ретикулума в мышцах. При введении указанных выше лекарств у пациента происходит массивный выброс ионов кальция из депо в цитоплазму мышечного волокна, развиваются клонические судороги и повышается температура тела (за счет усиления термогенеза).
Аллергические реакции (реакции гиперчувствительности). Это группа реакций, связанная с гиперактивацией иммунной системы. Они не зависят от вида лекарственного вещества и величины принятой дозы, протекают стереотипно (т.е. имеют универсальные проявления не зависимо от вызвавшего их лекарственного средства). У чувствительных лиц аллергическую реакцию могут вызвать ничтожные дозы лекарства (запах пенициллина в процедурном кабинете может привести к развитию анафилактического шока у пациента с аллергией к нему)
Для проявления аллергической реакции необходима предварительная сенсибилизация организма, поэтому после первого контакта организма с лекарством-аллергеном латентный период может продолжаться по меньшей мере 1-2 недели (за это время иммунные клетки синтезируют антитела). Только вторичный контакт с аллергеном вызовет развитие аллергической реакции.
Выделяют 4 типа аллергических реакций:
] Тип I – аллергические реакции немедленного типа, анафилактические реакции.
] Тип II – цитолитические реакции.
] Тип III – иммунокомплексные реакции.
] Тип IV – клеточно-опосредованная реакция замедленного типа
Date: 2015-07-01; view: 6694; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |