
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Запись сложных химических уравнений реакций в ионном виде
Молекулярное уравнение реакции обмена с участием воды:
2FeCl3 + 3K2CO3 + 3H2O = 6KCl + 2Fe(ОН)3  + 3СО2
+ 3СО2 
Полное ионное уравнение реакции:

Cокращенное ионное уравнение реакции:
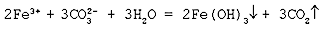
Данная реакция ионного обмена протекает до конца, о чем свидетельствуют сразу два признака: выделение газа и образование осадка.
Молекулярное уравнение реакции металлического цинка с водной щелочью:
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2 
Полное ионное уравнение реакции:
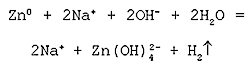
Cокращенное ионное уравнение реакции:
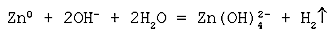
Молекулярное уравнение реакции амфотерного оксида с водной щелочью:
Al2O3 + 6KOH + 3H2O = 2K3[Al(OH)6].
Полное ионное уравнение реакции:
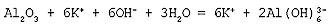
Cокращенное ионное уравнение реакции:
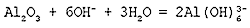
Молекулярное уравнение реакции нерастворимого карбоната с растворимой в воде солью:
СaCO3 + CuCl2 + H2O = Cu(OH)2  + CaCl2 + CO2
+ CaCl2 + CO2 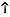
Полное ионное уравнение реакции:
СaCO3 + Cu2+ + 2Cl– + H2O = Cu(OH)2  + Ca2+ + 2Cl– + CO2
+ Ca2+ + 2Cl– + CO2 
Cокращенное ионное уравнение реакции:
СaCO3 + Cu2+ + H2O = Cu(OH)2  + Ca2+ + CO2
+ Ca2+ + CO2 
Date: 2015-07-17; view: 456; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |