
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Формула оксида формула соли
1) SO2 А) Ba(NO2)2
2) SO3 Б) NH4HCO3
3) N2O5 В) Ca(HSO3)2
4) N2O3 Г) Cu(NO3)2
Д) FeS
Е) (NH4)2SO4
В2. Установите соответствие между формулами органических веществ и продуктами их реакций с HCl:
ВЕЩЕСТВО ПРОДУКТ РЕАКЦИИ
1) CH3COONa А) (CH3)3CCl
2) CH3NH2 Б) (CH3)3CCl(CH3)3
3) (CH3)3COH В) CH3COOH
4) CH2CH2 Г) CH3CH2Cl
Д) CH3NH3Cl
Е) CH3Cl
Часть 3
С1. Напишите уравнения реакций, с помощью которых можно осуществить превращения:
этилен → этанол → этаналь→ этановая кислота → метиловый эфир этановой кислоты→ оксид углерода (IV).
Вариант 3
Часть 1
А1. Оксиду серы (VI) соответствует формула гидроксида:
1. Н2SO4
2. Н2SO3
3. Sn(OH)2
4. K2SO4
А2. Общая схема  соответствует цепочке превращении:
соответствует цепочке превращении:
1. кальций, оксид кальция, гидроксид кальция
2. натрий, оксид натрия, гидроксид натрия
3. алюминий, оксид алюминия, гидроксид алюминия
4. азот, оксид азота(V), гидроксид азота(V)
А3. Глицерин реагирует со всеми веществами группы:
1. водород, метиловый спирт, уксусная кислота
2. раствор перманганата калия, бромная вода, азотная кислота
3. свежеприготовленный гидроксид меди(II), кислород, металлический натрий
4. серная кислота, цинк, гидроксид натрия
А4. Сульфат меди(II) реагирует по отдельности с веществами:
1. Fe, Na2S, KOH
2. Ag, K2CO3, BaCl2
3. Zn, HNO3, CaCO3
4. Al, KCl, KOH
А5. В схеме превращений сахароза→ глюкоза → Х → диэтиловый эфир
веществом «X» является:
1. этанол
2. этаналь
3. этилен
4. этан
А6. Назовите промежуточные вещества «X» и «Y» в следующей схеме синтеза:

1. X – C2H5Cl, Y – CH3COOH
2. X – C2H5Cl, Y – CH3CH2OH
3. X – C2H5Cl, Y – CH3OH
4. X – C2H5Cl, Y – CH3CHO
А7. Назовите вещество «А» в следующей схеме синтеза

1. ацетилен
2. этанол
3. уксусная кислота
4. углекислый газ
А8. В схеме превращений 
веществами «X» и «Y» соответственно являются:
1. Fe и Cl2
2. Fe2O3 и HCl
3. Fe и HCl
4. Fe3O4 и HCl
А9. Веществами «X» и «Y» в цепочке превращений

соответственно являются:
1. I2, HBr
2. Cl2, HBrO
3. Cl2, HBr
4. I2, HBrO
А10. Из какого оксида невозможно получить щёлочь, действуя водой при обычных условиях:
1. оксид натрия
2. оксид кальция
3. оксид калия
4. оксид алюминия
Часть 2
В1. И азотная кислота, и гидроксид кальция способны реагировать с:
1. карбонатом натрия
2. оксидом меди(II)
3. цинком
4. гидроксидом хрома(III)
5. гидроксидом натрия
6. оксидом серы (VI)
В2. При растворении алюминия в избытке щёлочи образуется комплексная соль с координационным числом 4. Составьте уравнение реакции и укажите в ответе сумму коэффициентов в нём.
Часть 3
С1. Химики XIX века считали, что органические вещества нельзя получить из неорганических. Опровергните это мнение, написав уравнения реакций, с помощью которых можно получить уксусную кислоту из мрамора. Укажите условия осуществления каждой реакции.
Вариант 4
Часть 1
А1. Веществами Х и Y в схеме превращений
карбид алюминия  являются:
являются:
1. Х – метан, Y – этан;
2. Х – метан, Y – ацетилен;
3. Х – ацетилен, Y – водород;
4. Х – ацетилен, Y – сажа.
А2. В цепочке превращений
 веществами Х и Y соответственно являются:
веществами Х и Y соответственно являются:
1. CaC2 и H2O;
2. CaO и H2;
3. CaH2 и H2O;
4. Ca(OH)2 и H2.
А3. В цепочке превращений
NaCl→X --- +Y → Br2 веществами Х и Y соответственно являются:
1. NaOH и HBr;
2. H2 и NaBr;
3. Cl2 и NaBr;
4. NaBr и HCl.
А4. В схеме превращений 
веществами Х1, Х2, Х3 соответственно являются:
1. CO, CO2, Na2CO3;
2. CO, CO2, NaHCO3;
3. C2H2, CO2, Na2CO3;
4. C2H2, CO2,NaHCO3.
А5. В схеме превращений  FeO
FeO  веществами Х и Y соответственно являются:
веществами Х и Y соответственно являются:
1. Fe и Cl2;
2. Fe2O3 и HCl;
3. Fe и HCl;
4. Fe3O4 и HCl;
А6. Оксиду СuO соответствует основание:
1. гидроксид меди(II);
2. гидроксид меди (I);
3. гидроксид кальция;
4. гидроксид магния.
А7. В цепочке превращений  конечным веществом Х4 является:
конечным веществом Х4 является:
1. оксид железа (II);
2. оксид железа (III);
3. гидроксид железа (II);
4. гидроксид железа (III).
А8. Веществом Х в цепочке превращений
C2H5OH →X → CH3COOCH3
является:
1. этиловый спирт;
2. диэтиловый эфир;
3. уксусная кислота;
4. бутадиен – 1,3.
А9. Для осуществления превращений:
оксид кальция  карбонат кальция
карбонат кальция  оксид углерода (IV) необходимы вещества:
оксид углерода (IV) необходимы вещества:
1. а – углекислый газ и вода, б – соляная кислота;
2. а – углекислый газ, б – хлорид натрия;
3. а – углекислый газ, б – соляная кислота;
4. а – карбонат натрия, б – хлорид натрия.
А10. В цепочке химических превращений
FeS2→X→SO3→H2SO4 вещество Х – это:
1. H2SO4
2. SO2
3. S
4. H2SO3
Часть 2
В1. Какое вещество образуется в результате следующих превращений:

(В ответе запишите название вещества)
В2. Каков объём углекислого газа (н.у.), выделившегося при термическом разложении карбоната магния, если при этом было получено 10г оксида магния? (В ответе укажите число с точностью до десятых)
Часть 3
С1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения (укажите условия протекания реакций):


Одной стрелке соответствует одна реакция.
Ответы и решения по теме «Реакции, подтверждающие генетическую связь между классами неорганических и органических соединений»
| Код задания | Вариант 1 | Вариант 2 | Вариант 3 | Вариант 4 |
| А1 | ||||
| А2 | ||||
| А3 | ||||
| А4 | ||||
| А5 | ||||
| А6 | ||||
| А7 | ||||
| А8 | ||||
| А9 | ||||
| А10 | ||||
| В1 | ВЕГА | Нитрат аммония | ||
| В2 | ЭТАНОЛ | ВДАГ | 5,6 |
Часть 3
Вариант 1
(C6H10O5)n + nH2O → nC6H12O6
C6H12O6 → 2CO2 + 2C2H5OH
C2H5OH → C2H4 + H2O
C2H4 → C2H2 + H2
3C2H2 → C6H6
Вариант 2
Составлены уравнения реакций, соответствующие схеме превращений:
1. C2H4 + H2O  C2H5OH
C2H5OH
2. C2H5OH + CuO  C2H4O + H2O + Cu
C2H4O + H2O + Cu
3. C2H4O + Ag2O 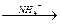 C2H4O + 2Ag
C2H4O + 2Ag
4. CH3COOH + CH3OH  CH3COOCH3 + H2O
CH3COOCH3 + H2O
5. 2CH3COOCH3 + 7O2 → 6CO2 + 6 H2O
Вариант 3

Вариант 4

Список литературы
1. Аргишева А.И., Задумина Э.А. Химия: Подготовка к государственному централизованному тестированию. – Саратов: Лицей, 2002. – 144с.
2. Горбунцова С.В. Тесты по основным разделам школьного курса химии: 8 – 9 классы. – М.: «ВАКО», 2006. – 208с. – (Мастерская учителя).
3. Егоров А.С. Как сдать ЕГЭ по химии на 100 баллов. – Ростов н/Д: Феникс, 2003. – 288с. (Серия «100 баллов».)
4. ЕГЭ-2008. Химия. Тренировочные задания / П.А. Оржековский, Н.Н. Богданова, М.В. Дорофеев и др. – М.: Эксмо, 2008. – 128с.
5. Сборник тестовых заданий для тематического и итогового контроля. Химия 10-11 класс. /Богданова Н.Н., Васюкова Е.Ю. – под общей редакцией Оржековского П.А., Татура А.О. М.: «Интеллект-Центр», 2007.-208с.
Date: 2016-11-17; view: 410; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |