
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Болезни надпочечников 1 page
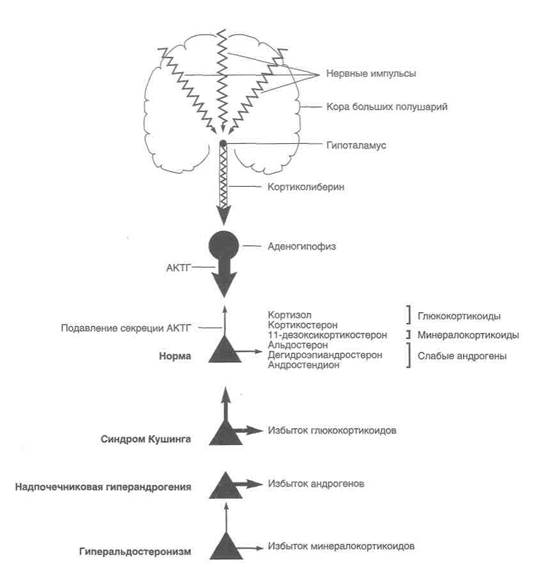
Классические проявления болезней надпочечников — синдром Кушинга, надпочечниковая недостаточность, гиперальдостеронизм, гиперандрогения и катехолами-новые кризы (рис. 32.1). Кроме того, при опухолях надпочечников могут наблюдаться боль и объемное образование в животе. Чтобы установить природу нарушений, необходимо детальное лабораторное исследование и во многих случаях визуализация надпочечников.
Помимо заболеваний, сопровождающихся гормональными нарушениями, и злокачественных опухолей, не секретирующих гормоны, встречаются и другие болезни надпочечников, которые также нужно учитывать при дифференциальной диагностике.
БОЛЕЗНИ КОРЫ НАДПОЧЕЧНИКОВ Синдром Кушинга
Термин «синдром Кушинга» объединяют состояния, обусловленные избытком глюкокортикоидов. Большинство случаев представлены гипофизарным синдромом Кушинга, известным также как болезнь Кушинга, — двусторонней гиперплазией коры надпочечников в результате избыточной секреции АКТГ. Примерно в 10% случаев причиной синдрома Кушинга бывает эктопическая секреция АКТГ или кортиколиберина негипофи-зарными опухолями, чаще всего овсяноклеточным раком легкого, а также карциноидами бронхов, тимуса и ЖКТ, опухолями из островковых клеток, медуллярным раком щитовидной железы, феохромоцитомой и недифференцированным раком предстательной железы. По 5% случаев синдрома Кушинга приходится на аденому и рак надпочечников. Последний служит самой частой причиной синдрома Кушинга у детей.
Патогенез
Избыточная продукция кортизола корой надпочечников приводит к усилению катаболизма. Из мышечной ткани высвобождаются аминокислоты, которые служат субстратом для глюконеогенеза. Часть образовавшейся при этом глюкозы преобразуется в печени в гликоген. Распад белка приводит к атрофии соединительной ткани и мышц (прежде всего плечевого и тазового пояса и брюшной стенки), мышечной слабости, плохому заживлению ран и тяжелому остеопорозу, который еще больше усугубляется из-за потерь кальция с мочой. Часть глюкозы расходуется на синтез жирных кислот и три-глицеридов, что приводит к отложению жира на животе, лице и над ключицами. У 20% больных повышается
уровень глюкозы в плазме натощак, а у 80% — нарушается толерантность к глюкозе.
Избыток кортизола приводит к иммунодефициту и рецидивирующим инфекциям. Угнетение функции фиб-робластов препятствует заживлению ран и делает организм больного еще более беззащитным перед инфекцией.
У 90% больных наблюдается артериальная гипертония. Уровень альдостерона, как правило, не повышается, однако кортизол в больших концентрациях сам обладает минералокортикоидным действием, подобно 11-дезоксикортикостерону. Возможны и другие проявления избытка минералокортикоидов — гипокалиемия и алкалоз. Они особенно часто встречаются при эктопическом синдроме Кушинга и раке надпочечников.
Патоморфология
При гипофизарном и эктопическом синдроме Кушинга наблюдается гиперплазия клеток пучковой зоны коры надпочечников. Для рака надпочечников характерны клеточный полиморфизм и прорастание опухолью капсулы органа и сосудов (рис. 32.2). Рак надпочечников метастазирует в печень, легкие, кости и головной мозг. Злокачественную опухоль зачастую бывает трудно отличить от аденомы. Кортизол, секретируемый аденомой или раком надпочечников, подавляет секрецию АКТГ гипофизом. В связи с этим неизмененная кора надпочечников атрофируется, в то время как опухоль продолжает расти.
Диагностика
Клиническая картина. Вероятность синдрома Кушинга высока при наличии по крайней мере трех из перечисленных симптомов (рис. 32.3 и 32.4).
1. Ожирение туловища, лунообразное лицо и отложение жира над ключицами и между лопатками. Подобное распределение подкожной клетчатки независимо от степени ожирения весьма характерно для синдрома Кушинга.
2. Багровые стрии на животе и бедрах. Иногда наблюдаются плохое заживление ран и язвы ног.
3. Артериальная гипертония (почти у всех больных).
4. Атрофия и слабость проксимальных мышц конечностей. Особенно характерна атрофия четырехглавых мышц бедра, из-за которой больному бывает трудно встать со стула без посторонней помощи.
5. Эмоциональная лабильность, раздражительность, бессонница, иногда — психозы.
6. Часто наблюдается остеопороз, для которого характерна боль в спине из-за компрессионных переломов позвонков и переломов ребер.
7. В 80% случаев наблюдается гипергликемия после еды, а в 20% случаев — натощак.
8. У женщин могут наблюдаться проявления надпочеч-никовой гиперандрогении. Гиперандрогения наиболее характерна для рака надпочечников. При аденоме надпочечников и гипофизарном синдроме Кушинга она бывает реже и менее выражена. Симптомы гипер-
Глава 32. Болезни надпочечников
|
| Стресс |
Рисунок 32.1. Гипоталамо-гипофизарно-надпочечниковая система при различных болезнях коры надпочечников.
андрогении включают андрогенетическую алопецию, гирсутизм, уменьшение размеров молочных желез, развитую мускулатуру и изменение тембра голоса. Клиническая картина не позволяет определить тип синдрома Кушинга. Для эктопического синдрома Кушинга характерны более острое начало и более выраженный избыток глюкокортикоидов, чем при раке надпочечников. Увеличенный надпочечник при раке иногда удается пропальпировать.
Лабораторные исследования. Число лейкоцитов в крови может повышаться до 12 000—20 000 мкл-1, причем лимфоциты, как правило, составляют не более 20%. Эо-зинофилов мало или нет совсем. Более чем в половине случаев наблюдается эритроцитоз, а уровень гемогло-
бина составляет 14—16 г%. У больных со злокачественными опухолями и эктопическим синдромом Кушинга возможна анемия. При биохимическом исследовании крови обнаруживают повышение уровней натрия и снижение уровня калия в плазме. Возможна гипергликемия.
Пробы для подтверждения диагноза синдрома Кушшгй позволяют отличить синдром Кушинга от гиперкорти-золемии, обусловленной стрессом. Суточная экскреция кортизола. Уровень кортизола в суточной моче определяют с помощью высокоэффективной жидкостной хроматографии. В норме экскреция кортизола составляет 10—50 мкг/сут. Чтобы проконтролировать правильность сбора мочи, одновременно
Глава 32. Болезни надпочечников

|
 Рисунок 32.2. Аденома и рак надпочечников. А. Гистологическое строение аденомы из клеток пучковой зоны коры надпочечников, удаленной у больной 39 лет с синдромом Кушинга. Б. Гистологическое строение опухоли надпочечника (аденокарцинома), удаленной у больной 36 лет, страдающей диссеминированным раком надпочечников. Обращает внимание выраженный полиморфизм клеток. Опухоль врастает в крупную вену (на микрофотографии этого не видно). Следует отметить, что иногда так выглядят и аденомы надпочечников, но они никогда не врастают в кровеносные сосуды. Forsham PH: The adrenal cortex. In: Williams RH (ed.): Textbook ofEndocrinology, 4th ed. Saunders, 1968.
Рисунок 32.2. Аденома и рак надпочечников. А. Гистологическое строение аденомы из клеток пучковой зоны коры надпочечников, удаленной у больной 39 лет с синдромом Кушинга. Б. Гистологическое строение опухоли надпочечника (аденокарцинома), удаленной у больной 36 лет, страдающей диссеминированным раком надпочечников. Обращает внимание выраженный полиморфизм клеток. Опухоль врастает в крупную вену (на микрофотографии этого не видно). Следует отметить, что иногда так выглядят и аденомы надпочечников, но они никогда не врастают в кровеносные сосуды. Forsham PH: The adrenal cortex. In: Williams RH (ed.): Textbook ofEndocrinology, 4th ed. Saunders, 1968.
 с кортизолом определяют креатинин. При синдроме Кушинга суточная экскреция кортизола повышается по крайней мере вдвое. При острых заболеваниях, депрессии и алкоголизме возможны ложноположительные результаты. Однако при ожирении уровень свободного кортизола в моче остается в норме. Короткая проба с дексаметазоном. В норме небольшие дозы дексаметазона подавляют секрецию АКТГ и кортизола по принципу отрицательной обратной связи. Если назначить дексаметазон в 23:00, к утру секреция кортизола у здорового человека снизится, а при синдроме Кушинга останется высокой. Дексаметазон используют для супрессивных проб, потому что он в 30 раз сильнее, чем кортизол, подавляет секрецию АКТГ и не искажает результаты определения уровня кортизола в плазме и моче.
с кортизолом определяют креатинин. При синдроме Кушинга суточная экскреция кортизола повышается по крайней мере вдвое. При острых заболеваниях, депрессии и алкоголизме возможны ложноположительные результаты. Однако при ожирении уровень свободного кортизола в моче остается в норме. Короткая проба с дексаметазоном. В норме небольшие дозы дексаметазона подавляют секрецию АКТГ и кортизола по принципу отрицательной обратной связи. Если назначить дексаметазон в 23:00, к утру секреция кортизола у здорового человека снизится, а при синдроме Кушинга останется высокой. Дексаметазон используют для супрессивных проб, потому что он в 30 раз сильнее, чем кортизол, подавляет секрецию АКТГ и не искажает результаты определения уровня кортизола в плазме и моче.
Чтобы провести короткую пробу с дексаметазоном, вечером в 23:00 больному назначают дексаметазон в дозе 1 мг внутрь, а в 8:00 берут кровь и определяют уровень кортизола в плазме. Если он окажется ниже 5 мкг% (в норме уровень кортизола в плазме составляет 5—20 мкг%), диагноз синдрома Кушинга можно исключить. Диагноз синдрома Кушинга считается подтвержденным, если уровень кортизола превышает 10 мкг%. При уровне кортизола 5—10 мкг% результат считают сомнительным иповторяют пробу через некоторое время или измеряют содержание кортизола в моче (рис. 32.5).

Рисунок 32.3. Клинические проявления синдрома Кушинга. Forsham PH: The adrenal cortex. In: Williams RH (ed.): Textbookof Endocrinology, 4th ed. Saunders, 1968.
Глава 32. Болезни надпочечников
 | |
 |

|
Уровни андрогенов в плазме. При аденомах коры надпочечников уровни андрогенов, как правило, нормальные или снижены, в то время как при раке надпочечников возможна выраженная гиперандрогения. Уточнение локализации патологического процесса. Гипо-физарный и эктопический синдром Кушинга. Если данные лабораторных исследований указывают на гиперсекрецию АКТГ, следует выявить ее источник. Поскольку ги-пофизарный синдром Кушинга встречается намного чаще других, а у большинства больных эктопическим синдромом Кушинга имеется уже выявленная злокачественная опухоль, обследование начинают с МРТ головы. При этом у 50—60% больных выявляют аденому гипофиза, а оставшимся больным определяют уровень АКТГ в крови из пещеристых или нижних каменистых синусов (мест венозного дренажа аденогипофиза). Если данные МРТ и определения уровня АКТГ в крови из пещеристых или нижних каменистых синусов позволяют исключить гипофизарный синдром Кушинга, проводят КТ грудной клетки и живота в поисках опухоли, секретирующей АКТГ или кортиколиберин. Надпочечниковый синдром Кушинга. При низком уровне АКТГ в плазме и других признаках надпочечникового синдрома Кушинга проводят КТ надпочечников с толщиной среза 3 мм. Как правило, диаметр опухолей, вызывающих синдром Кушинга, превышает 3 см (рис. 32.6), поэтому выявить их не составляет труда. Диаметр аденом надпочечников обычно составляет 3—6 см. Диаметр опухоли при раке надпочечников превышает 5 см. Кроме того, на момент постановки диагноза часто обнаруживают
Рисунок 32.4. Внешний вид больной с синдромом Кушинга. Обращают на себя внимание багровое лунообразное лицо, залысины, отложение жира в области седьмого шейного позвонка, выступающий живот и непропорционально тонкие руки и ноги.
Эстрогены стимулируют синтез транскортина, поэтому уровень кортизола в плазме повышается при беременности и приеме пероральных контрацептивов. Пе-роральные контрацептивы следует отменить по крайней мере за 3 нед до проведения пробы. Кроме того, причиной ложноположительного результата может быть острое заболевание, депрессия или алкоголизм. Кроме того, дексаметазон не подавляет секрецию кортизола у 15% больных ожирением.
Дифференциальная диагностика синдрома Кушинга. В 95% случаев лабораторные исследования позволяют точно установить причину синдрома Кушинга. Уровень АКТГ в плазме позволяет отличить гипофизар-ный и эктопический синдромы Кушинга от надпочеч-никового. Уровень АКТГ определяют высокочувствительным иммунорадиометрическим методом. В норме он составляет 10—50 пг/мл, при гипофизарном синдроме Кушинга — 10—200 пг/мл, при эктопическом — более 200 пг/мл, а при надпочечниковом, когда секреция АКТГ подавлена, — менее 5 пг/мл.
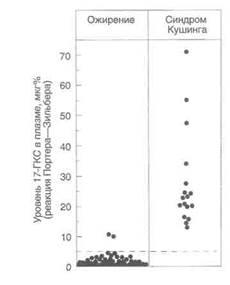
Рисунок 32.5. Результаты пробы с дексаметазоном при ожирении и синдроме Кушинга. Описание пробы приведено в тексте, 17-ГКС — 17-гидроксикортикостероиды. Pavlatos FC, SmiloRP, Forsham PH: A rapid screening test for Cushing's syndrome. JAMA 1975; 193:720.
Глава 32. Болезни надпочечников

|
 Рисунок 32.6. Уточнение локализации опухолей надпочечников с помощью КТ. Аденома левого надпочечника диаметром 3 см (показана стрелкой) расположена спереди и медиально от левой почки. П — почка. Korobkin MT et al.: Am J Roentgenol 1979; 132:231.
Рисунок 32.6. Уточнение локализации опухолей надпочечников с помощью КТ. Аденома левого надпочечника диаметром 3 см (показана стрелкой) расположена спереди и медиально от левой почки. П — почка. Korobkin MT et al.: Am J Roentgenol 1979; 132:231.

 признаки инвазивного роста и метастазы в печень или легкие. Гиперсекреция кортизола опухолью подавляет функцию здорового надпочечника, который на томограмме выглядит нормальным или атрофичным. Увеличение обоих надпочечников указывает на гипофизарный или эктопический синдром Кушинга. Для визуализации надпочечников применяют также УЗИ и МРТ, хотя они не имеют явных преимуществ перед КТ.
признаки инвазивного роста и метастазы в печень или легкие. Гиперсекреция кортизола опухолью подавляет функцию здорового надпочечника, который на томограмме выглядит нормальным или атрофичным. Увеличение обоих надпочечников указывает на гипофизарный или эктопический синдром Кушинга. Для визуализации надпочечников применяют также УЗИ и МРТ, хотя они не имеют явных преимуществ перед КТ.
Осложнения
Артериальная гипертония может привести к сердечной недостаточности или инсульту. Часто встречаются плохо поддающиеся лечению кожные и системные инфекции. При остеопорозе возможны патологические переломы позвонков и ребер. Усиление резорбции кости нередко приводит к гиперкальциурии и образованию мочевых камней. Нередки психические расстройства, которые проходят после удаления опухоли.
Лечение
Гипофизарный синдром Кушинга. При микроаденомах гипофиза уточняют их локализацию и выполняют селективную транссфеноидальную аденомэктомию. Эта операция, выполненная опытным нейрохирургом, представляет собой оптимальный метод лечения. Она позво-
ляет добиться излечения в 80% случаев и избежать гипо-питуитаризма у большинства больных. Эктопический синдром Кушинга. Лечение опухолей, сек-ретирующих АКТГ, представляет собой трудную задачу, поскольку большинство из них выявляются на поздних стадиях и сопровождаются выраженной гиперкортизо-лемией. По возможности опухоль следует удалить, однако операция приводит к излечению лишь при доброкачественных опухолях, например при карциноиде бронха. При остаточных опухолях назначают ингибиторы ферментов стероидогенеза, а при их неэффективности прибегают к двусторонней адреналэктомии. Двусторонняя адреналэктомия. Эту операцию выполняют больным с гипофизарным синдромом Кушинга, у которых невозможно удалить опухоль гипофиза и не удалось устранить избыток кортизола с помощью лучевой терапии и лекарственных средств. Еще одно показание к операции — угрожающий жизни эктопический синдром Кушинга, не поддающийся лечению ингибиторами ферментов стероидогенеза.
В настоящее время предпочитают выполнять эндоскопическую адреналэктомию. Для этого используют боковой внебрюшинный доступ. Сначала удаляют один надпочечник, потом переворачивают больного и удаляют другой. Лапароскопическая операция занимает при-
Глава 32. Болезни надпочечников
мерно столько же времени, что и открытая, но при ней реже наблюдаются послеоперационные осложнения и меньше время пребывания в стационаре. Предоперационная подготовка. Поскольку адреналэкто-мия неизбежно приводит к первичной надпочечнико-вой недостаточности, чрезвычайно важно еще до операции назначить больному глюкокортикоиды в/в с тем, чтобы продолжить заместительную терапию после операции. В послеоперационном периоде переходят на прием глюкокортикоидов внутрь, постепенно снижая дозу до минимальной эффективной.
Послеоперационный период. После операции больной чувствует себя удовлетворительно, пока доза гидрокортизона превышает физиологическую примерно на 20 мг. По мере снижения дозы могут появляться симптомы отмены — тошнота, боль в животе и слабость. Поэтому снижать дозу следует постепенно, за несколько суток. В день операции больному вводят 200 мг гидрокортизона в/в, на следующий день — 150 мг, затем — 100 мг, а в последующие дни переходят на прием препарата внутрь (соответственно 80,60 и 40 мг) в сочетании с флудрокортизоном. Поддерживающая доза гидрокортизона составляет 20—30 мг, флудрокортизона — 0,1 мг. Аденома и рак надпочечников. Чтобы ускорить выздоровление и сократить пребывание в стационаре, почти всем больным с доброкачественными и небольшими злокачественными опухолями надпочечников выполняют лапароскопическую операцию. При злокачественных опухолях надпочечников диаметром более 8—10 см высок риск метастазов и врастания в соседние органы. Если имеются признаки поражения соседних органов или инвазии надпочечниковой либо нижней полой вены, выполняют открытую операцию, используя передний чрезбрюшинный или боковой внебрюшинный доступ. Предоперационная подготовка. Предоперационная подготовка такая же, как и перед двусторонней адреналэк-томией, поскольку оставшийся надпочечник атрофирован и не сможет обеспечить потребность в кортико-стероидах.
Послеоперационный период. В день операции и после нее назначают гидрокортизон в тех же дозах, что и при двусторонней адреналэктомии, постепенно снижая дозу до 30 мг/сут. Эту дозу делят на 3 приема, а потом в течение нескольких недель ее доводят до 10 мг утром (в 7:00—8:00). В зависимости от того, как быстро будет восстанавливаться функция оставшегося надпочечника, заместительную терапию продолжают от полугода до 2 лет. В назначении минералокортикоидов, как правило, нет необходимости, поскольку атрофированный надпочечник секретирует достаточно альдостерона. При раке надпочечников операция не всегда приводит к излечению, и больным требуется дополнительное лечение. Медикаментозное лечение. Лекарственных средств, способных подавить секрецию АКТГ, не существует, однако во многих случаях удается устранить избыток корти-зола, назначив ингибиторы ферментов стероидогенеза. Медикаментозное лечение показано при противопока-
заниях к операции (например, из-за тяжелого общего состояния или недавно перенесенного инфаркта миокарда) либо в случаях, когда больному не удалось удалить опухоль, секретирующую АКТГ, кортиколиберин или кортизол.
Препаратом выбора служит кетоконазол, блокирующий 20,22-десмолазу и lip-гидроксилазу. Его назначают внутрь в дозе 800—1600 мг/сут; суточную дозу делят на 2 приема. Побочные эффекты препарата — надпо-чечниковая недостаточность, повышение активности печеночных ферментов и гепатотоксическое действие.
Ингибитор 1 ip-гидроксилазы метирапон добавляют к кетоконазолу при его неэффективности либо применяют самостоятельно. Обычная доза составляет 1—4 г/сут внутрь в 4 приема.
Другие ингибиторы ферментов стероидогенеза — ами-ноглутетимид и трилостан — в настоящее время используют редко.
Адренолитическое средство митотан (изомер инсектицида ДДТ) угнетает секрецию кортизола и разрушает клетки коры надпочечников. Препарат используют почти исключительно при раке надпочечников, если не удалось полностью удалить опухоль. Обычная доза составляет 6—12 г/сут внутрь в 3—4 приема. Почти у 70% больных, принимающих митотан, снижается секреция кортизола, а у 35% — уменьшается размер опухоли. Однако убедительных данных, что препарат повышает выживаемость, нет. Побочные эффекты — тошнота, рвота, понос, депрессия и сонливость — наблюдаются в 80% случаев.
Прогноз
Большинство проявлений синдрома Кушинга, в частности артериальная гипертония и сахарный диабет, при лечении исчезают в течение нескольких дней или недель. Исключение составляет остеопороз, который у взрослых сохраняется. При аденомэктомии по поводу гипофизар-ного синдрома Кушинга ближайший прогноз благоприятный, однако длительное наблюдение за такими больными показывает, что примерно у 10% из них опухоль рецидивирует. При злокачественных опухолях, секре-тирующих АКТГ, прогноз в целом неблагоприятный. Как правило, больные погибают в течение нескольких месяцев после постановки диагноза. Удаление доброкачественной опухоли может привести к излечению. При аденомах надпочечников прогноз благоприятный. Односторонняя адреналэктомия дает отличные результаты. Прогноз при раке надпочечников неблагоприятный. Митотан в дозе 6—12 г/сут уменьшает проявления синдрома Кушинга, но почти не увеличивает выживаемость. Другие противоопухолевые средства, равно каки лучевая терапия, неэффективны.
Надпочечниковая гиперандрогения
Надпочечниковая гиперандрогения чаще встречается у женщин. Ее причиной могут быть врожденная гипер-
Глава 32. Болезни надпочечников
 плазия коры надпочечников или доброкачественная либо злокачественная вирилизирующая опухоль. В отличие от глюкокортикоидов, ускоряющих катаболизм, андрогены обладают анаболическим действием. У больных наблюдаются андрогенетическая алопеция, усиленный рост волос на лице и в других андрогензависи-мых зонах. У мужчин увеличивается половой член, в то время как яички, наоборот, атрофируются. У женщин наблюдаются гипертрофия клитора, атрофия молочных желез и аменорея (рис. 32.7). Мышечная масса увеличивается, а содержание жира уменьшается, поэтому фигура у больных массивная, но подтянутая. Тембр голоса снижается, особенно у женщин. Поскольку этот эффект обусловлен увеличением гортани, голос остается низким и после лечения. У представителей обоего пола повышаются агрессивность и половое влечение.
плазия коры надпочечников или доброкачественная либо злокачественная вирилизирующая опухоль. В отличие от глюкокортикоидов, ускоряющих катаболизм, андрогены обладают анаболическим действием. У больных наблюдаются андрогенетическая алопеция, усиленный рост волос на лице и в других андрогензависи-мых зонах. У мужчин увеличивается половой член, в то время как яички, наоборот, атрофируются. У женщин наблюдаются гипертрофия клитора, атрофия молочных желез и аменорея (рис. 32.7). Мышечная масса увеличивается, а содержание жира уменьшается, поэтому фигура у больных массивная, но подтянутая. Тембр голоса снижается, особенно у женщин. Поскольку этот эффект обусловлен увеличением гортани, голос остается низким и после лечения. У представителей обоего пола повышаются агрессивность и половое влечение.
Врожденная гиперплазия коры надпочечников
Патогенез. Врожденная гиперплазия коры надпочечников — это группа заболеваний, обусловленных генетическими дефектами ферментов стероидогенеза. Многие из них приводят к усилению секреции надпочечниковых андрогенов и в результате — к псевдогермафродитизму у девочек и увеличению полового члена и мошонки у мальчиков. Избыточная секреция андрогенов начинается еще внутриутробно. У девочек яичники и производные мюллеровых протоков (матка и влагалище) развиваются нормально, а дифференцировка мочеполового
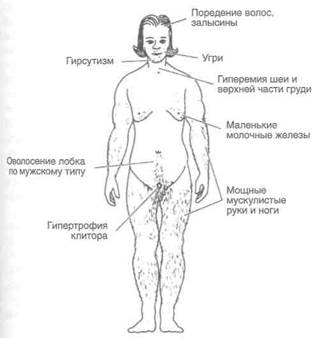
Рисунок 32.7. Клинические проявления вирилизации при врожденной гиперплазии коры надпочечников. Forsham PH: The adrenal cortex. In: Williams RH (ed.): Textbook of Endocrinology, 4th ed. Saunders, 1968.
синуса и полового бугорка нарушается: наблюдается сращение губно-мошоночных складок, а мочеиспускательный канал открывается в тело гипертрофированного клитора. Часто гипертрофируются губно-мошо-ночные складки. Клиническая картина напоминает мужской фенотип с тяжелой гипоспадией и криптор-хизмом.
Надпочечники секретируют промежуточные продукты синтеза глюкокортикоидов и минералокортикоидов, обладающие лишь анаболическим и андрогенным действием, поэтому у больных наблюдается надпочечнико-вая недостаточность, тяжесть которой зависит от того, какой из ферментов дефектен. При этом усиливается секреция АКТГ, что приводит к двусторонней гиперплазии коры надпочечников. При некоторых формах врожденной гиперплазии коры надпочечников наблюдается накопление 11-дезоксикортикостерона, вызывающего артериальную гипертонию. Стероидогенез может нарушаться на разных уровнях.
Недостаточность 20,22-десмолазы приводит к врожденной липоидной гиперплазии коры надпочечников, для которой характерен тяжелый дефицит всех стероидных гормонов. В отсутствие заместительной терапии большинство больных умирают в грудном возрасте.
Недостаточность Зр-гидроксистероиддегидрогеназы проявляется дефицитом прогестерона, альдостерона и кортизола и избытком дегидроэпиандростерона. Это редкое заболевание проявляется надпочечниковой недостаточностью, синдромом потери соли, мужским и женским псевдогермафродитизмом. В легких случаях проявления ограничиваются нарушениями менструального цикла, бесплодием, угрями и гирсутизмом.
Недостаточность 21 -гидроксилазы — самое частое заболевание этой группы. При нем нарушается превращение 17-гидроксипрогестерона в 11-дезоксикортизол и прогестерона в 11-дезоксикортикостерон. Заболевание может протекать с синдромом потери соли, но чаще он отсутствует. У новорожденных наблюдаются надпочеч-никовая недостаточность, а у девочек — наружные половые органы промежуточного типа. В более старшем возрасте возможны ускоренный рост, преждевременное закрытие зон роста и ложное преждевременное половое развитие.
Недостаточность 17а-гидроксилазы приводит к дефициту глюкокортикоидов и половых гормонов. У мальчиков наблюдается псевдогермафродитизм, и многие из них воспитываются как девочки, так как имеют феноти-пически нормальные наружные женские половые органы. Изредка у новорожденных с генетическим мужским полом встречаются наружные половые органы промежуточного типа. В этом случае они воспитываются как мальчики. Часто болезнь выявляют только в пубертатном периоде. Характерны снижение уровня кортизола, повышение уровня АКТГ, первичная аменорея или задержка полового развития. Избыток минералокортикоидов, особенно 11-дезоксикортикостерона, приводит к артериальной гипертонии.
Глава 32. Болезни надпочечников
Недостаточность 1 ip-гидроксилазы приводит к нарушению синтеза кортизола и кортикостерона и накоплению 11-дезоксикортикостерона и андрогенов. У больных обычно наблюдаются артериальная гипертония, гипокалиемия и легкая гиперандрогения.
Недостаточность 18-гидроксилазы приводит к нарушению синтеза альдостерона в клубочковой зоне коры надпочечников. Заболевание проявляется гипоальдо-стеронизмом, артериальной гипотонией и гиперкалие-мией.
Диагностика. Клиническая картина. У новорожденных с генетическим женским полом наблюдается различная степень вирилизации наружных половых органов. В тяжелых случаях фенотип напоминает мужской с тяжелой гипоспадией и крипторхизмом. У новорожденных мальчиков наружные половые органы могут быть нормальными. Чем раньше началось воздействие избытка андрогенов на плод, тем сильнее выражены изменения при рождении.
У девочек в отсутствие лечения наблюдаются гирсу-тизм, хорошо развитая мускулатура, аменорея и недоразвитие молочных желез. У мальчиков увеличен размер полового члена, а вот яички часто атрофичны, поскольку избыток надпочечниковых андрогенов подавляет секрецию ЛГ и ФСГ гипофизом. Изредка в яичках увеличиваются надпочечниковые остатки, и они становятся большими и плотными. В большинстве случаев сперматогенез отсутствует.
Больные обоего пола поначалу быстро растут, обгоняя в росте своих одноклассников, но к 9—10 годам избыток андрогенов приводит к закрытию эпифизарных зон роста, больные прекращают расти и остаются низкорослыми.
Лабораторные исследования. Уровень 17-кетостероидов в моче превышает норму для данного пола и возраста. В сыворотке повышены уровни андростендиона, дегид-роэпиандростерона, дегидроэпиандростерона сульфата, тестостерона и АКТГ, а при недостаточности 21-гидро-ксилазы — 17-гидроксипрогестерона. Цитогенетическое исследование не выявляет отклонений. Рентгенография. Костный возраст превышает паспортный.
ЛТпозволяет обнаружить двустороннее увеличение надпочечников.
Урологическое и гинекологическое исследования проводятся для выявления пороков развития половых органов. Дифференциальная диагностика. За проявления врожденной гиперплазии коры надпочечников часто принимают многие пороки развития. В их числе: 1) тяжелая гипоспа-дия в сочетании с крипторхизмом; 2) женский псевдогермафродитизм (может быть обусловлен не только избытком надпочечниковых андрогенов, но и приемом андрогенов или прогестагенов матерью во время беременности); 3) мужской псевдогермафродитизм; 4) истинный гермафродитизм. У детей с этой патологией уровни гормонов не выходят за пределы нормы и отсутствует ускорение закрытия эпифизарных зон роста.
Лечение. Ранняя диагностика чрезвычайно важна и служит залогом успешного лечения. Цель лечения — подавить секрецию АКТГ и тем самым уменьшить секрецию надпочечниковых андрогенов. Для этого назначают гидрокортизон или преднизон внутрь в дозах, достаточных для того, чтобы подавить секрецию андрогенов и тем самым предотвратить вирилизацию и преждевременное закрытие эпифизарных зон роста. При синдроме потери соли назначают флудрокортизон, 0,05—0,3 мг внутрь (в зависимости от возраста и тяжести заболевания), и увеличивают потребление поваренной соли. Это позволяет устранить артериальную гипотонию и стабилизировать вес. После полового созревания у девочек можно провести хирургическую коррекцию наружных половых органов — разделение мочеполового синуса и формирование нормального входа во влагалище. Разумное применение эстрогенов и пероральных контрацептивов позволяет сделать фигуру больных более женственной и тем самым повысить их самооценку.
Date: 2016-11-17; view: 567; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |