
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Изопроцессы идеального газа
Если в термодинамическом процессе один из трех параметров (P, V, T) остается постоянным, то процесс называют изопроцессом.
 Рис. 28
Рис. 28
|
Следовательно  и
и  ; График процесса представлен на рис. 28.
; График процесса представлен на рис. 28.
Первый закон термодинамики примет вид 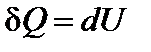
 (для изохорного процесса)
(для изохорного процесса)
Тогда 
Если  не зависит от температуры, то изменение внутренней энергии в изохорном процессе пропорционально изменению температуры.
не зависит от температуры, то изменение внутренней энергии в изохорном процессе пропорционально изменению температуры.
Для произвольной массы газа  ; Последняя формула справедлива для любого процесса в идеальном газе.
; Последняя формула справедлива для любого процесса в идеальном газе.
 Рис. 29
Рис. 29
|
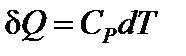 ;
;  ;
;  ;
;
Запишем первый закон термодинамики с учетом приведенных формул для одного моля

 – уравнение Р. Майера
– уравнение Р. Майера
Из этого уравнения следует физический смысл универсальной газовой постоянной R. Она численно равна работе изобарного расширения одного моля идеального газа при нагревании его на один Кельвин.
в) Изотермический процесс (Т = const) (рис. 30). dU = 0;
 Рис. 30
Рис. 30
|
 .
.
 , но
, но  .
.
Тогда 
Используя уравнение состояния идеального газа, запишем для одного моля
 ;
;
Работа расширения газа  – положительна; работа сжатия газа
– положительна; работа сжатия газа  – отрицательна (рис. 29). Теплоемкость вещества в изотермическом процессе бесконечно велика.
– отрицательна (рис. 29). Теплоемкость вещества в изотермическом процессе бесконечно велика.
Адиабатный процесс
В этом процессе отсутствует теплообмен энергией в форме теплопередачи между системой и внешней средой, т.е.  . Тогда первый закон примет вид:
. Тогда первый закон примет вид:
 .
.
Для одного моля газа получим:

Для нахождения dT продифференцируем уравнение Менделеева-Клапейрона  :
:


 ;
;
Подставим это в предыдущее уравнение:
 ;
;
 ;
;

 ;
;
Разделим последнее уравнение на PV:

Интегрируем это уравнение

 Рис. 31
Рис. 31
|
 и перепишем последнее уравнение в виде:
и перепишем последнее уравнение в виде:  – это уравнение адиабаты или уравнение Пуассона, где γ – коэффициент Пуассона.
– это уравнение адиабаты или уравнение Пуассона, где γ – коэффициент Пуассона.
На рис. 31 приведен график адиабаты. График идет круче, чем изотерма. Давление при сжатии в адиабатном процессе увеличивается не только за счет уменьшения объема, но и за счет повышения температуры.
Date: 2016-05-25; view: 489; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |