
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кинетика и механизм процесса
В настоящее время в мире производство кальцинированной соды базируется на четырех основных способах: аммиачном, из природной соды, комплексной переработкой нефелинов, карбонизацией гидроксида натрия.
Карбонизация гидроксида натрия как промышленный способ получения кальцинированной соды получила некоторое распространение в конце 60-х–начале 70-х годов. В настоящее время во всем мире действует лишь несколько небольших установок по получению соды с использованием этого способа, и доля его в мировом производстве кальцинированной соды составляет около 1 % [1].
Процесс переработки нефелинов с получением глинозема, кальцинированной соды, поташа и цемента на основе апатит-нефелиновых месторождений, а также нефелиновых руд – третий по значимости из промышленных способов получения соды.
Вторым по значимости способом, по которому получают соду, является получение соды из природного содосодержащего сырья. Особенно этот способ получил распространение за рубежом, в США, после того, как там были открыты залежи троны (Na2CO3–NaHCO3–2H2O). С 1977 года в США для производства соды используют также рапу озера Сиэрлз (Калифорния).
Недавно в США были открыты новые богатейшие залежи природной соды - нахколита (NaHCO3) и даусонита (NaАl(ОН)2СО3). Источники природной соды, но несравненно меньше чем в США имеют и другие страны: Бельгия, Бразилия, Индия, Китай, Турция, Канада, ЮАР. В 1990–1993 годах долю соды, получаемой из природного содосодержащего сырья в мировой практике можно оценить в 32,1 % [7].
Аммиачный способ получения соды продолжает оставаться основным и на сегодняшний день. По состоянию на 1993 год его доля в производстве карбоната натрия составила около 65 % [6].
Следует упомянуть о разновидности аммиачного способа, который основан на замене аммиака органическими соединениями – алифатическими аминами. Однако этот способ на сегодняшний день не получил достаточного широкого распространения и на Украине не применяется [8].
Украина имеет лишь незначительные запасы нефелиновых руд, и не обладает природными запасами, содержащими соду. Поэтому на сегодняшний день единственным способом, по которому производят соду на Украине, является аммиачный способ. Рассмотрим аммиачный способ более подробно.
В общем виде для любых химико-технологических систем химизм основных стадий аммиачно-содового процесса можно представить в виде следующих уравнений [9]:
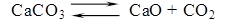
CaO + H2O = Ca(OH)2(1.2)
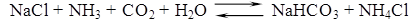
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3 +2H2O(1.4)
2NaHCO3 = Na2CO3 + H2O + CO2(1.5)
На содовых заводах гидрокарбонат аммония получают из аммиака и углекислого газа, растворяя их в водных растворах NaCl. Это уравнение характеризует только конечный результат взаимодействия хлорида натрия и гидрокарбоната аммония. В действительности процесс карбонизации протекает гораздо сложнее [3].
Так как диоксид углерода плохо растворяется в воде в отсутствие аммиака, то на первой стадии сначала раствор хлорида натрия насыщают аммиаком, а потом аммонизированный рассол насыщают диоксидом углерода. Процесс насыщения раствора хлорида натрия аммиаком и диоксидом углерода проводят при сравнительно низких температурах, что обеспечивает протекание реакции слева на право.
На первом стадии карбонизации большая часть диоксида углерода связывается в карбомат аммония:
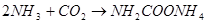 ,
,
который затем гидролизуется

с образованием пересыщенного по НСО3– раствора. Затем из пересыщенного раствора кристаллизуется гидрокарбонат натрия, образующийся по реакции:

Кристаллизация гидрокарбоната натрия подчиняется общим закономерностям и зависит, прежде всего, от температуры, пересыщения и скорости перемешивания раствора. Необходимо отметить, приведенная схема только условно отображает процесс.
Процесс насыщения аммонизированного рассола диоксидом углерода является экзотермическим. Поэтому выделяющееся тепло необходимо отвести, чтобы обеспечить требуемые степени карбонизации раствора и утилизации натрия [1].
Наиболее простое кинетическое уравнение процесса карбонизации имеет вид:
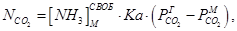
где 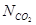 – количество диоксида углерода, поглощенного в единицу времени единицей поверхности раствора, моль/м3;
– количество диоксида углерода, поглощенного в единицу времени единицей поверхности раствора, моль/м3;
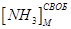 – концентрация активного компонента (не связанного в хлорид и углеаммонийные соли аммиака), н.д.;
– концентрация активного компонента (не связанного в хлорид и углеаммонийные соли аммиака), н.д.;
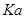 – константа, включающая константу Генри и частичный коэффициент абсорбции для жидкостной пленки;
– константа, включающая константу Генри и частичный коэффициент абсорбции для жидкостной пленки;
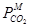 – давление диоксида углерода над метастабильным раствором, кПа;
– давление диоксида углерода над метастабильным раствором, кПа;
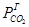 – парциальное давление CO2 в карбонизующем газе, кПа.
– парциальное давление CO2 в карбонизующем газе, кПа.
Следует отметить, что температурный режим влияет на процесс образования кристаллов NaHCO3. Для получения крупных кристаллов правильной формы, которые не забивают поверхность вакуум-фильтров и малорастворимые в процессе фильтрации, необходимо поддерживать температуру 60–72 °С в зоне образования и в начальных период роста кристаллов. В процессе дальнейшего роста кристаллов температура уже не оказывает существенного влияния на рост кристаллов. При нормальном росте кристаллов образуются кристаллы типа "бочка", при ухудшении процесса кристаллизации образуются длинные кристаллы склонные к образованию сростков в виде снопов – кристаллы "друза". Такие кристаллы забивают вакуум-фильтры и способствуют тому, что в осадке гидрокарбонат натрия содержится больше воды, чем в кристаллах типа "бочка".
На основе горизонтальной проекции изотермической диаграммы растворимости для 15 °С в системе NaCl–NH4Cl–NH4HCO3–NaHCO3, изученной П.П. Федотьевым (см. рис. 1.1), можно определить оптимальные условия для проведения процесса карбонизации. Они находятся вблизи точки Р1 и линии P1–IV.
Выпавший осадок гидрокарбоната натрия отфильтровывают, и далее его подвергают прокаливанию с получением соды. Температура разложения гидрокарбоната натрия составляет 160–180 °С. Эта операция протекает в отделении кальцинации. Выделяющийся диоксид углерода используется в процессе карбонизации.
I–Р2 – растворы, насыщенные NaHCO3 и NaCl; P2–P1 – растворы, насыщенные NaHCO3 и NaCl; P1–IV – растворы, насыщенные NaHCO3 и NH4HCO3;
P1 – раствор, насыщенный NaHCO3, NH4HCO3 и NH4Cl; Р2 – раствор, насыщенный NaCl, NH4C1 и NaHCO3.
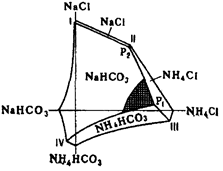
Рис. 1.1 – Диаграмма системы NaCl–NH4Cl–NH4HCO3–NaHCO3
Аммиак обычно регенерируют из хлорида аммония и возвращают в производство. С этой целью раствор, содержащий хлорид аммония подвергают обработке известковым молоком. Образующийся аммиак отгоняют из раствора и направляют на абсорбцию [1].
Для получения известкового молока необходим оксид кальция, который получают путем обжига карбонатного сырья (мела или известняка) в известково-обжигательных печах при температуре 1100–1200 °С. Образующийся диоксид углерода используют в отделении карбонизации, а СаО используют для получения известкового раствора.
Поступающий сырой рассол (водный раствор хлорида натрия) подвергают предварительной очистке от примесей солей кальция и магния с помощью Na2CO3 и Са(ОН)2. В процессе очистки образуются плохо растворимые Mg(OH); и СаСО3, выпадающие в осадок:
MgCl2 + Ca(OH)2 → Mg(OH)2↓ + CaCl2
CaCl2 + Na2CO3 → CaCO3↓ + 2NaCl
Осадки Mg(OH)2 и СаСО3 удаляют, а очищенный рассол направляют дальше в производство.
Date: 2015-06-05; view: 836; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |