
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Обмен углеводов”, часть 2
Челночные механизмы
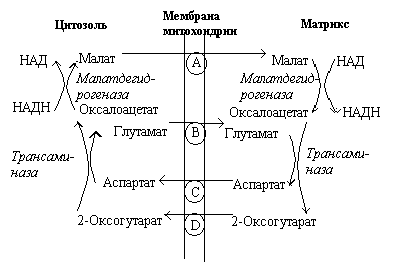 |
Поскольку ферменты гликолиза локализованы в цитоплазме, то и НАДН·Н+, образовавшийся в ходе глицеральдегид-3-фосфатдегидрогеназной реакции, находится в цитоплазме. Для переноса водорода с цитоплазматического НАДН·Н+ в дыхательную цепь существуют специальные механизмы, называемые челночными: 1) малат-аспартатный – дает на выходе 3 молекулы АТФ, и 2) α-глицеролфосфатный (глицерол-3-фосфатный) – дает на выходе 2 молекулы АТФ.
 |
Рис. Малат-аспартатный челнок
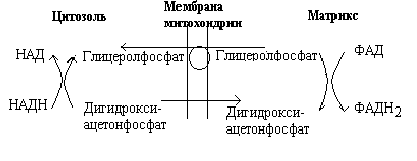 |
Рис. Глицеролфосфатный челнок
Выход АТФ при аэробном распаде глюкозы
Аэробный распад глюкозы не следует путать с аэробным гликолизом. Аэробный распад глюкозы это процесс полного распада глюкозы до СО2 и Н2О. И в этом процессе аэробный гликолиз представляет собой лишь первый этап:
Глюкоза
Глицеральдегид-3-фосфат
Пируват
Ацетил-КоА
СО2 и Н2О
Поскольку в результате подготовительной стадии гликолиза глюкоза окисляется с образованием 2 молекул глицеральдегид-3-фосфата, начиная с глицеральдегид-3-фосфата вводим коэффициент 2.
При окислении 1 мол. ацетил-КоА до СО2 и Н2О (ЦЛК) образуется 3 молекулы НАДН·Н+, молекула ФАДН2 и молекула ГТФ.
При окислении 1 мол. пирувата до ацетил-КоА образуется 1 мол. НАДН·Н+.
При окислении глицеральдегид-3-фосфата до пирувата образуется 2 молекулы АТФ (путем субстратного фосфорилирования) и молекула НАДН·Н+. Наконец, при окислении глюкозы в глицеральдегид-3-фосфат затрачивается 2 молекулы АТФ.
Итого, 38(40) – 2 = 36(38) молекул АТФ в расчете на 1 молекулу глюкозы.
Аэробный распад глюкозы может происходить во всех органах и тканях. В наибольшей зависимости от аэробного распада глюкозы находится мозг. Он расходует около 100 г глюкозы в сутки. В состоянии основного обмена около 20% всего поступающего в организм кислорода потребляется мозгом (при том, что на долю мозга приходится лишь 2% массы тела). Поэтому как недостаток глюкозы, так и недостаток кислорода проявляют себя прежде всего симптомами со стороны ЦНС – головокружением, потерей сознания, судорогами.
Анаэробный гликолиз
В анаэробных условиях образовавшийся при гликолизе НАДН·Н+ реокисляется не за счет кислорода (который отсутствует), а за счет пирувата, восстанавливающегося в лактат:
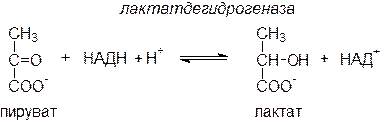 |
Лактатдегидрогеназа представляет собой тетрамер, содержащий протомеры двух типов - М (muscle) и Н (heart). Известно 5 изоферментов, различающихся набором протомеров.
Изомерные формы ЛДГ1 и ЛДГ2 обнаруживаются в мозге, сердце, корковом веществе почек, т.е. в тканях с интенсивным снабжением кислородом. Форма ЛДГ3 - в поджелудочной железе, ЛДГ4 и ЛДГ5 в скелетных мышцах, печени, мозговом веществе почек, т.е. в тканях с менее интенсивным снабжением кислородом. Все эти формы ферментов значительно различаются максимальной скоростью реакции и константами Михаэлиса для лактата и пирувата. ЛДГ5 быстро катализирует восстановление пирувата в лактат при низких концентрациях лактата. ЛДГ1 катализирует быстрое окисление лактата в пируват в сердечной мышце.
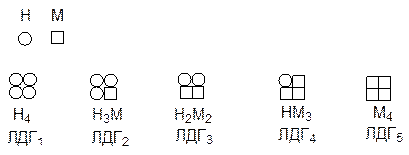 |
Суммарное уравнение анаэробного гликолиза выглядит следующим образом:
Глюкоза + 2 АДФ + 2 H3PO4 = 2 Лактат + 2 АТФ + 2 Н2О
Т.о. десять ферментов, превращающих глюкозу в пируват, совместно с ЛДГ способны обеспечить синтез АТФ в отсутствие кислорода. В анаэробных условиях АТФ образуется только за счет двух реакций субстратного фосфорилирования. В этих реакциях в расчете на 1 моль глюкозы образуется 4 моль АТФ. После вычитания 2 моль АТФ, потребляемых в подготовительной стадии, получаем чистый выход АТФ при гликолизе – 2 моль АТФ на 1 моль глюкозы.
Гликолиз у животных и человека протекает во многих типах клеток, но его значение для разных органов различно. В интенсивно работающих скелетных мышцах аэробный процесс не может обеспечить потребности мышц в энергии. В этих условиях резко усиливается анаэробный путь синтеза АТФ и в мышцах накапливается молочная кислота. Если после ночного сна концентрация лактата в крови составляет 1-2 ммоль/л, то после тяжелой мышечной работы может достигать 20 ммоль/л. Особенно большое значение анаэробный гликолиз имеет при кратковременной интенсивной работе продолжительностью от 30 секунд до 2,5 минут. При более продолжительной интенсивной мышечной работе скорость анаэробного гликолиза довольно быстро уменьшается, а аэробного процесса – возрастает. Через 4-5 минут бега (дистанция 1,5 км) энергия поставляется поровну аэробным и анаэробным процессами, а через 30 минут (10 км) – почти целиком аэробным процессом. В продолжение первой минуты работы благодаря анаэробному процессу достигается гораздо большая мощность, чем при дальнейшей работе. Следует отметить, что при длительной работе в аэробном процессе все в большей мере используется не глюкоза, а жирные кислоты.
Эритроциты вообще не имеют митохондрий, и их потребность в АТФ целиком удовлетворяется за счет анаэробного гликолиза. Интенсивный гликолиз характерен также для клеток злокачественных опухолей.
Глюконеогенез
Образование D-глюкозы из неуглеводных предшественников называется глюконеогенезом. Глюконеогенез протекает в основном в печени и значительно менее интенсивно – в корковом веществе почек и слизистой оболочке кишечника.
Механизм глюконеогенеза
Центральным путем глюконеогенеза является превращение пирувата в глюкозу. Т.о. глюконеогенез можно рассматривать как процесс обратный гликолизу. В гликолизе, однако, имеются три необратимые реакции (гексокиназная, фосфофруктокиназная и пируваткиназная), которые по этой причине не могут использоваться в глюконеогенезе. В обход этих реакций в глюконеогенезе протекают реакции, катализируемые другими ферментами. Эти обходные реакции тоже необратимы, но идут в направлении синтеза глюкозы.
Первый обходной путь – образование фосфоенолпирувата из пирувата в обход пируваткиназной реакции. Катализируется двумя ферментами: пируваткарбоксилазой (Е1) и фосфоенолпируваткарбокикиназой (Е2):
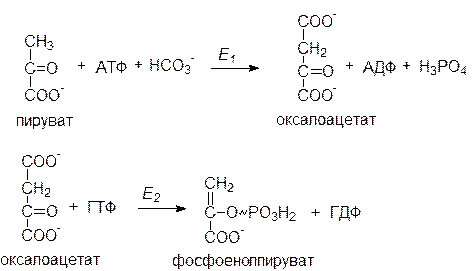 |
Пируваткарбоксилаза – регуляторный фермент. В отсутствие ацетил-КоА, являющимся для нее положительным регулятором, она практически неактивна. Реакция протекает в митохондриях, куда пируват поступает с помощью пируваттранслоказы. Образовавшийся оксалоацетат не способен проникать через внутреннюю митохондриальную мембрану и поступать в цитоплазму, где протекают остальные реакции (в том числе вторая) глюконеогенеза. Поэтому он обратимо восстанавливается за счет НАДН·Н+ в малат под действием митохондриальной малатдегидрогеназы (МДГ):
Оксалоацетат + НАДН·Н+ ––––––––––→ малат + НАД+
Малат при участии специальной транспортной системы переходит из митохондрий в цитоплазму, где под действием цитоплазматической малатдегидрогеназы окисляется с образованием оксалоацетата:
малат + НАД+ ––––––––––→ оксалоацетат + НАДН·Н+
И, образовавшийся таким образом, оксалоацетат вступает в реакцию глюконеогенеза, катализируемую фосфоенолпируваткарбоксикиназой.
Второй обходной путь связан с образованием фруктозо-6-фосфата из фруктозо-1,6-дифосфата в обход фосфофруктокиназной реакции. Реакция катализируется фруктозо-1,6-дифосфатазой:
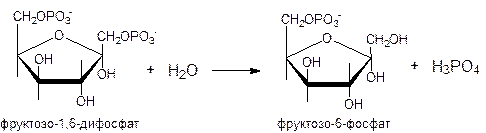 |
Третий обходной путь связан с образованием из глюкозо-6-фосфата свободной глюкозы в обход гексокиназной реакции. Реакция катализируется
глюкозо-6-фосфатазой:
 |
Свободная глюкоза, образующаяся в результате реакции, поступает из печени в кровь.
Суммарное уравнение процесса:
2 пируват + 4 АТФ + 2 ГТФ + 2 НАДН·Н+ + 4 Н2О → глюкоза + 4 АДФ + 2ГДФ + 6 Н3РО4 + 2 НАД+
Неуглеводные источники для глюконеогенеза
условно можно разделить на три группы:
1) вещества, способные превращаться в один из метаболитов гликолиза. Например, глицерин.
2) вещества, способные превращаться в пируват. Например, лактат.
3) вещества, способные превращаться в оксалоацетат. К ним относятся метаболиты ЦЛК.
Однако, главными источниками глюконеогенеза являются аминокислоты, превращающиеся в пируват или оксалоацетат. Аминокислоты, способные превращаться в глюкозу, называются гликогенными. К ним относятся все протеиногенные аминокислоты, кроме лейцина.
Значение глюконеогенеза
1) В организме взрослого человека за сутки может синтезироваться около 80 г глюкозы. Особенно важное значение глюконеогенез играет в обеспечении глюкозой мозга при недостатке углеводов в организме.
2) Возвращение лактата в метаболический фонд углеводов.
Регуляция гликолиза и глюконеогенеза в печени
Каждая из необратимых реакций гликолиза вместе с соответствующей ей необратимой реакцией глюконеогенеза составляет субстратные циклы. Эти циклы служат точками приложения регуляторных механизмов. Переключение печени с гликолиза на глюконеогенез и наоборот происходит при участии инсулина и глюкагона.
Направление реакций первого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови повышается (до10-20 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы.
Направление реакций второго субстратного цикла зависит от активности фосфофруктокиназы 1 и фруктозо-1,6-дифосфатазы. Активность этих ферментов зависит от концентрации фруктозо-2,6-дифосфата. Фруктозо-2,6-дифосфат образуется путем фосфорилирования фруктозо-6-фосфата при участии фосфофруктокиназы-2 (ФФК-2). ФФК-2 является бифункциональным ферментом, поскольку катализирует не только прямую, но и обратную реакцию (дефосфорилирования). Киназная активность проявляется, когда ФФК-2 находится в дефосфорилированной форме, которая характерна для абсорбтивного периода, когда инсулин-глюкагоновый индекс (ИГИ) высокий. При низком ИГИ, характерном для периода голодания, происходит фосфорилирование ФФК-2 и проявление ее фосфатазной активности, результатом чего является снижение количества фруктозо-2,6-дифосфата.
Фруктозо-2,6-дифосфат аллостерически активирует ФФК-1, фермент гликолиза, и одновременно ингибирует фруктозо-1,6-дифосфатазу, фермент глюконеогенеза. Поэтому при накоплении фруктозо-2,6-дифосфата происходит активация гликолиза и угнетение глюконеогенеза и наоборот, при снижении концентрации фруктозо-2,6-дифосфата происходит угнетение гликолиза и активация глюконеогенеза.
В регуляции третьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная активна.
Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори)
При выполнении кратковременной интенсивной работы, когда основным процессом, обеспечивающим работающие мышцы энергией, является анаэробный гликолиз, глюкоза, а затем и мышечный гликоген быстро расщепляются с образованием лактата. Лактат не подвергается в мышцах дальнейшим превращениям и диффундирует в кровь. В период восстановления лактат удаляется из крови печенью и превращается в глюкозу путем глюконеогенеза. Глюкоза поступает в кровь и далее в мышцы. Т.о. цикл замыкается. Этот цикл получил название глюкозо-лактатного цикла или цикла Кори.
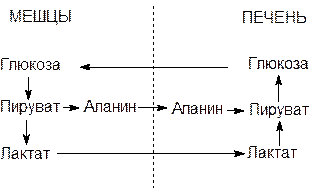 |
Рис. Цикл Кори и глюкозо-аланиновый цикл
Метаболизм гликогена
Гликоген представляет собой разветвленный полисахарид, мономером которого служит глюкоза. Остатки глюкозы соединены в линейных участках α-1,4-гликозидными связями, а в местах разветвления - α-1,6-гликозидными связями. Молекула гликогена более разветвлена, чем крахмал, точки ветвления встречаются через каждые 8-10 остатков глюкозы.
Гликоген – основной резервный полисахарид в клетках животных. Гликоген плохо растворим в воде и не влияет на осмотическое давление в клетке, поэтому в клетке депонируется гликоген, а не свободная глюкоза.
Гликоген депонируется главным образом в печени и скелетных мышцах, запасаясь в цитозоле клеток в форме гранул. С гранулами связаны и ферменты, участвующие в обмене гликогена. Синтез и распад гликогена протекают разными метаболическими путями.
Гликогенолиз
Мобилизация гликогена происходит в основном в период между приемами пищи и ускоряется во время физической работы.
Этот процесс происходит в результате действия ключевого фермента гликогенолиза гликогенфосфорилазы, которая катализирует реакцию:
(глюкоза)n + Н3РО4 ¾® (глюкоза)n-1 + глюкозо-1-фосфат
Реакция практически необратима. Поскольку в результате реакции глюкоза образуется в фосфорилированной форме, данный процесс распада гликогена называется фосфоролитическим. Гликогенфосфорилаза катализирует расщепление только концевых a-1,4-гликозидных связей в боковых цепях гликогена. Поскольку участки разветвления гликогена для гликогенфосфорилазы не доступны (она не действует на a-1,6-гликозидные связи), на полисахарид в этом случае действует другой фермент – a-1,6-гликозидаза, катализируя гидролитическое расщепление a-1,6-связи в точке ветвления с образованием одной молекулы D-глюкозы и открывая для действия гликогенфосфорилазы новый участок цепи гликогена.
Образовавшийся под действием гликогенфосфорилазы глюкозо-1-фосфат превращается в глюкозо-6-фосфат (метаболит гликолиза) под действием фермента фосфоглюкомутазы.
Распад гликогена в печени и мышцах имеет одну различающую их реакцию, обусловленную наличием в печени фермента глюкозо-6-фосфатазы. Присутствие в печени этого фермента обусловливает главную функцию гликогена печени – освобождение глюкозы в кровь в период между приемами пищи. Т.о. мобилизация гликогена печени обеспечивает поддержание уровня глюкозы в крови на постоянном уровне. Через 10-18 ч после приема пищи запасы гликогена в печени значительно истощаются, а голодание в течение 24 ч приводит к полному его исчезновению.
Функция мышечного гликогена заключается в высвобождении глюкозо-6-фосфата, используемого в самой мышце для окисления и получения энергии.
Синтез гликогена
Гликоген синтезируется практически во всех тканях, особенно активно в печени и скелетных мышцах. Синтез происходит в период пищеварения, спустя 1-2 ч после приема углеводной пищи. Синтез гликогена требует энергии. При включении одного мономера в полисахаридную цепь протекают 2 реакции, сопряженные с расходованием АТФ и УТФ.
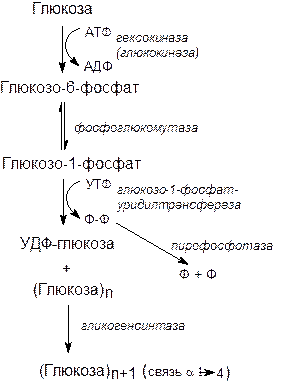 |
Перенос глюкозильных групп от УДФ-глюкозы на нередуцирующий конец разветвленной молекулы гликогена катализируется ферментом гликогенсинтазой. При этом образуется новая a-1,4-гликозидная связь. Образование a-1,6-связей, находящихся в точках ветвления цепей гликогена, гликогенсинтаза не способна. Эти связи образует специальный «ветвящий» фермент путем переноса коротких фрагментов (из 6-7 остатков глюкозы) с одного участка гликогена на другой с образованием a-1,6-гликозидных связей. Таким образом, наращивание молекулы гликогена осуществляется путем чередования действия этих двух ферментов.
Регуляция депонирования и мобилизации гликогена
Переключение процессов синтеза и мобилизации гликогена в печени происходит при переходе состояния пищеварения в постабсорбтивный период или состояния покоя на режим мышечной работы. В переключении этих метаболических путей в печени участвуют гормоны инсулин, глюкагон и адреналин, а в мышцах – инсулин и адреналин.
Влияние этих гормонов на синтез и распад гликогена реализуется на уровне ключевых ферментов - гликогенсинтазы и гликогенфосфорилазы – и осуществляется путем их фосфорилирования и дефосфорилирования.
Первичным сигналом для синтеза инсулина и глюкагона является изменение концентрации глюкозы в крови. Инсулин и глюкагон постоянно присутствуют в крови, но при переходе из абсорбтивного состояния в постабсорбтивное изменяется их относительная концентрация – инсулин-глюкагоновый индекс (ИГИ). Т.о., главным переключающим фактором в печени является инсулин ИГИ.
В постабсорбтивном периоде ИГИ снижается и решающим фактором является влияние глюкагона, который стимулирует распад гликогена в печени. Механизм действия глюкагона включает каскад реакций, приводящий к активации гликогенфосфорилазы:
аденилатциклаза (неакт)
гормон® ¯ АТФ
аденилатциклаза (акт) ® ¯ ПК А (неакт)
цАМФ® ¯ киназа фосфорилазы (неакт)
ПК А (акт)® ¯ фосфорилаза В
киназа фосфорилазы (акт)® ¯ гликоген
фосфорилаза А→ ↓
глюкозо-1-Ф
В период пищеварения преобладающим является влияние инсулина, т.к. ИГИ в этом случае повышается. Под влиянием инсулина происходит:
а) стимуляция транспорта глюкозы в клетки мышечной ткани.
б) изменение количества некоторых ферментов путем индукции и репрессии их синтеза. Например, инсулин индуцирует синтез глюкокиназы, ускоряя тем самым фосфорилирование глюкозы в печени.
в) изменение активности ферментов путем фосфорилирования и дефосфорилирования. Инсулин снижает содержание цАМФ в клетке (а значит и цАМФ-зависимое фосфорилирование) путем активации фосфодиэстеразы – фермента, гидролизующего цАМФ, с одной стороны. С другой стороны, он активирует фосфатазу гликогенсинтазы. Последняя дефосфорилируется и переходит в активное состояние.
Пентозофосфатный путь превращений глюкозы
ПФП является альтернативным путем окисления глюкозы. Он не приводит к синтезу АТФ, но поставляет клеткам кофермент НАДФН·Н+, а также обеспечивает клетки рибозой. НАДФН·Н+, использующийся как донор водорода в реакциях восстановления, участвует в реакциях биосинтеза жирных кислот и холестерина, а также в реакциях гидроксилирования, играющих важную роль в функционировании микросомальной цепи обезвреживания чужеродных веществ. Рибоза участвует в синтезе нуклеотидов и нуклеиновых кислот, а также аминокислоты гистидина.
ПФП может функционировать в печени, жировой ткани, молочной железе, коре надпочечников, эритроцитах и органах, где активно протекают восстановительные синтезы, например синтез жирных кислот. Все ферменты ПФП локализованы в цитозоле.
Химизм
1 реакция: дегидрирование глюкозо-6-фосфата
Реакцию катализирует глюкозо-6-фосфатдегидрогеназа, ключевой фермент пентозофосфатного цикла. Образовавшийся в ходе реакции 6-фосфоглюконолактон - соединение нестабильное, которое спонтанно, либо под действием специфической лактоназы гидролизуется.
2 реакция: гидролиз 6-фосфоглюконолактона с образованием 6-фосфоглюконата. Равновесие суммарной реакции сильно смещено в сторону образования НАДФ·Н+.
3 реакция: дегидрирование и декарбоксилирование 6-фосфоглюконата с образованием рибулозо-5-фосфата.
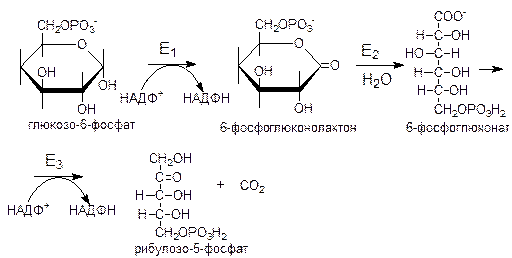 |
Превращение глюкозо-6-фосфата до рибулозо-5-фосфата принято называть окислительной фазой пентозофосфатного цикла. Фаза от рибулозо-5-фосфата до образования вновь глюкозо-6-фосфата называется неокислительной или анаэробной фазой этого цикла.
4 реакция: изомеризация пентозофосфатов. Рибулозо-5-фосфат под действием ферментов рибозофосфатизомеразы и рибулозо-5-фосфат-3-эпимеразы может обратимо изомеризоваться в другие пентозы: рибозо-5-фосфат, ксилулозо-5-фосфат.
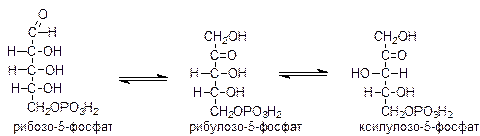 |
В некоторых случаях ПФП на этом заканчивается. И тогда суммарное уравнение реакции выглядит так:
глюкозо-6-фосфат + Н2О + 2НАДФ+ ® рибозо-5-фосфат + 2НАДФН·Н+ +СО2
Однако многие клетки нуждаются в большем количестве НАДФН·Н+ (для восстановительных синтезов), чем требуется рибозо-5-фосфата (для включения в нуклеотиды). В таких случаях рибозо-5-фосфат превращается в глицеральдегид-3-фосфат и фруктозо-6-фосфат под действием двух ферментов: транскетолазы и трансальдолазы. Эти ферменты создают обратимую связь между ПФП и гликолизом, катализируя следующие реакции:
5) ксилулозо-5-фосфат + рибозо-5-фосфат ® седогептулозо-7-фосфат + глицеральдегид-3-фосфат
6) седогептулозо-7-фосфат + глицеральдегид-3-фосфат ® эритрозо-4-фосфат + фруктозо-6-фосфат*
7) ксилулозо-5-фосфат + эритрозо-4-фосфат ® фруктозо-6-фосфат* + глицеральдегид-3-фосфат*
Суммируя эти реакции, получаем: 2 ксилулозо-5-фосфат + рибозо-5-фосфат ® 2 фруктозо-6-фосфат + глицеральдегид-3-фосфат
Итак, избыток рибозо-5-фосфата, образованный в ПФП, может превращаться в метаболиты гликолиза.
Метаболизм фруктозы
Фруктоза, поступающая в организм человека, образуется либо при гидролизе сахарозы, либо поступает в составе растений, являясь их основным сахаром. У здорового человека фруктоза может превращаться по двум путям: 1) под действием гексокиназы (в печени, мышцах, почках, жировой ткани) образуется фруктозо-6-фосфат. Однако, сродство этого фермента к фруктозе гораздо ниже, чем к глюкозе, поэтому в присутствии глюкозы реакция фосфорилирования фруктозы протекает с низкой скоростью; 2) под действием фруктокиназы (в печени, почках и кишечнике) образуется фруктозо-1-фосфат. Фермент обладает высоким сродством к своему субстрату и в присутствии глюкозы становится основным путем метаболизма фруктозы.
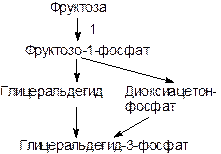 |
Фруктоза включается в гликолиз на стадии триозофосфатов.
Е1 – фруктокиназа
Е2 – фруктозо-1-фосфатальдолаза
Е3 - триозофосфатизомераза
Расщепление фруктозы по пути гликолиза происходит быстрее, чем глюкозы, т.к. минуется стадия, катализируемая фосфофруктокиназой-I.
Метаболизм фруктозы в сперматозоидах
Фруктоза является основным источником энергии для сперматозоидов. Она образуется в семенных пузырьках из глюкозы в результате 2-х последовательных реакций:
1)D-глюкозы + НАДФН·Н+ ® D-сорбитол + НАДФ+
реакция катализируется сорбитолдегидрогеназой.
2) D-сорбитол + НАД+ ® D-фруктоза + НАДН·Н+
реакция катализируется сорбитолдегидрогеназой.
Концентрация фруктозы в семенной жидкости может достигать 10 мМ.
Метаболизм галактозы
Галактоза, поступающая в организм человека, образуется при гидролизе лактозы (молочного сахара). Галактоза включается в метаболизм путем превращения в глюкозо-1-фосфат.
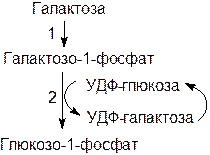 |
Образовавшийся глюкозо-1-фосфат после превращения в глюкозо-6-фосфат подключается к основным путям метаболизма глюкозы.
Date: 2015-05-23; view: 1228; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |