
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Ученица: Бисинбаева Динара Учитель: Анищук Ю.В
МОУ Гимназия №1
РЕФЕРАТ
НА ТЕМУ:
«Вирусы и Рак»
Ученица: Бисинбаева Динара Учитель: Анищук Ю.В.
Вирусы
Вирус- возбудители инфекционных болезней растений, животных и человека, размножающиеся только в живых клетках.
Согласно одному из определений вирусы представляют собой форму жизни, согласно другому вирусы являются комплексами органических молекул, взаимодействующими с живыми организмами. Вирусы похожи на живые организмы в том, что они имеют свой набор генов и эволюционирует путём естественного отбора, а также в том, что способны размножаться, создавая собственные копии путём самосборки. Вирусы имеют генетический материал, однако лишены клеточного строения, а именно эту черту обычно рассматривают как фундаментальное свойство живой материи. У вирусов нет собственного обмена веществ, и для синтеза собственных молекул им необходима клетка-хозяин. По этой причине они не способны размножаться вне клетки.. Общепризнанные формы жизни размножаются делением клетки, в то время как вирусные частицы самопроизвольно собираются в инфицированной клетке. От роста кристаллов размножение вирусов отличается тем, что вирусы наследуют мутации находятся под давлением естественного отбора. Самосборка вирусных частиц в клетке даёт дополнительное подтверждение гипотезы, что жизнь могла зародиться в виде самособирающихся органических молекул.
Свойства и происхождение вирусов.
Наиболее простоустроенныевирусы состоятизнуклеиновой кислоты, являющейсягенетическимматериалом(геномом) вируса, ипокрывающегонуклеиновуюкислоту белковогочехла. Всоставнекоторыхвирусоввходяттакжеуглеводыижиры(липиды). Такимобразом, вирусыможнорассматриватьпростокакмобильныенаборыгенетическойинформации. Вирусылишены некоторыхферментов, необходимыхдлярепродукции, имогутразмножатьсятольковнутриживойклетки, метаболизмкоторойпослезараженияперестраиваетсянавоспроизводствовирусных, анеклеточных компонентов. Этосвойствовирусовпозволяетотнестиихкоблигатным(обязательным) клеточным паразитам. Послесинтезаотдельныхкомпонентовформируютсяновыевирусныечастицы. Симптомы вирусногозаболеванияразвиваютсякакследствиеповреждениявирусамиотдельныхклеток. Принято считать, чтовирусыпроизошливрезультатеобособления(автономизации) отдельныхгенетических элементовклетки, получивших, крометого, способностьпередаватьсяоторганизмакорганизму. В нормальнойклеткепроисходятперемещениянесколькихтиповгенетическихструктур, напримерматричной,илиинформационной, РНК(мРНК), транспозонов, интронов, плазмид. Такиемобильныеэлементы,возможно, былипредшественниками, илипрародителями, вирусов. Внутри зараженной клетки вирусы проявляют себя как интегральные компоненты более сложных живых систем, но вне клетки представляют собой метаболически инертные нуклеопротеины. Вирусы содержат генетическую информацию, но не могут самостоятельно реализовать ее, не обладая собственным механизмом синтеза белка.
Размеры вирусов.
Величинавирусовварьируетот20до300нм(1нм= 10-9м). Практическивсевирусыпо своимразмераммельче, чем бактерии.Однаконаиболеекрупныевирусы, напримервирус коровьейоспы, имеюттакиежеразмеры, как инаиболеемелкиебактерии(хламидииириккетсии), которые тожеявляютсяоблигатнымипаразитамииразмножаютсятольковживыхклетках. Поэтомуотличительными чертамивирусовпосравнениюсдругимимикроскопическимивозбудителямиинфекцийслужатнеразмеры илиобязательныйпаразитизм, аособенностистроенияиуникальныемеханизмырепликации(воспроизведениясамихсебя).
СТРОЕНИЕ ВИРУСОВ.
Полноценнаяпостроениюиинфекционная, т.е. Способнаявызватьзаражение, вируснаячастицавнеклетки называетсявирионом. Вирусные частицы (вирионы) состоят из двух или трёх компонентов: генетического материала в виде ДНК или РНК (некоторые, например мимивирусы, имеют оба типа молекул); белковой оболочки (капсида), защищающей эти молекулы, и, в некоторых случаях, — дополнительных липидных оболочек. Наличие капсида отличает вирусы от вирусоподобных инфекционных нуклеиновых кислот — вироидов. В зависимости от того, каким типом нуклеиновой кислоты представлен генетический материал, выделяют ДНК-содержащие вирусы и РНК-содержащие вирусы; на этом принципе основана классификация вирусов по Балтимору. Ранее к вирусам также ошибочно относили прионы, однако впоследствии оказалось, что эти возбудители представляют собой особые инфекционные белки и не содержат нуклеиновых кислот. Форма вирусов варьирует от простой спиральной и икосаэдрической до более сложных структур. Размеры среднего вируса составляют около одной сотой размеров средней бактерии. Большинство вирусов слишком малы, чтобы быть отчётливо различимыми под световым микроскопом.
Вирусы являются облигатными паразитами, так как не способны размножаться вне клетки. Вне клетки вирусные частицы не проявляют признаки живого и ведут себя как частицы биополимеров. От живых паразитарных организмов вирусы отличаются полным отсутствием основного и энергетического обмена и отсутствием сложнейшего элемента живых систем — аппарата трансляции (синтеза белка), степень сложности которого превышает таковую самих вирусов.
ПРИ ИКОСАЭДРИЧЕСКОМ ТИПЕ СИММЕТРИИ:
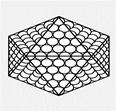
Капсомеры,или белковые субъединицы вируса, образуют
изометрический белковый чехол, состоящий из 20 правильных
треугольников.
В СЛУЧАЕ СПИРАЛЬНОЙ СИММЕТРИИ:
капсомеры, или субъединицы вируса, формируют спираль вокруг полой трубчатой сердцевины.
Вирионы со спиральным типом симметрии, как у вируса
табачной мозаики, имеют форму удлиненного цилиндра;внутри
белкового чехла, состоящего из отдельных субъединиц 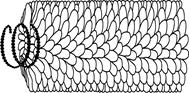
- капсомеров, находится свернутая спираль нуклеиновой кислоты
(РНК). Вирионы с икосаэдрическим типом симметрии, как у
полиовируса, имеют сферическую, а точнее, многогранную форму;
их капсиды построены из 20 правильных треугольных фасеток
(поверхностей) и похожи на геодезический купол.
КОМБИНИРОВАННАЯ:
симметрия у вирусов может быть представлена разными
вариантами. Частица бактериофага, показанная на схеме,
имеет "головку" правильной геометрической формы и "хвост"
со спиральной симметрией. 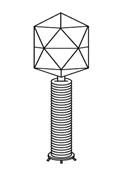
У отдельных бактериофагов (вирусов бактерий; фагов) смешанный
тип симметрии. У т.н. "хвостатых" фагов головка имеет вид
сферического капсида; от нее отходит длинный трубчатый
отросток - "хвост".
Встречаются вирусы с еще более сложным строением. Вирионы поксвирусов (вирусы группы оспы) не имеют правильного, типичного капсида: между сердцевиной и наружной оболочкой у них располагаются трубчатые и мембранные структуры.
РЕПЛИКАЦИЯ ВИРУСОВ
Репликация вирусных геномов — это матричный комплементарный синтез нуклеиновых кислот, преследующий целью наработку геномных последовательностей для их последующей инкапсидации в вирион.
ДНК-геномы реплицируются клеточными или вирусоспецифическими ДНК-полимеразами. РНК-геномы реплицируются вирусоспецифическими РНК-полимеразами, которые также являются и транскриптазами. Репликация вирусных геномов происходит или одновременно с транскрипцией, или эти два процесса разделены во времени.
Механизмы репликации вирусных геномов различны и определяются видом генома. Существует три модели репликации — полуконсервативная, консервативная и дисперсная. Консервативная и дисперсная модели репликации нуклеиновых кислот установлены только у вирусов.
Полуконсервативная модель предполагает, что после первого раунда репликации одна цепь в каждой из двух дочерних молекул является родительской, другая — синтезируемой заново. По такой схеме репликацируются днДНК-геномы.
При реализации консервативной модели репликации одна дочерняя молекула состоит из двух родительских цепей, а другая — из вновь синтезированных цепей. Согласно консервативной модели реплицируются двухнитевые РНК реовирусов. ДНК-содержащие вирусы, реплицирующиеся таким образом, неизвестны.
Дисперсная модель репликации приводит к образованию молекулы нуклеиновой кислоты, состоящей из фрагментов как родительских цепей, так и вновь синтезированных. Дисперсная модель реализуется на промежуточной стадии репликации онДНК генома парвовирусов.
Единицей репликации является так называемый репликон — нуклеотидная последовательность, расположенная между точкой начала репликации (origin) и точкой окончания репликации (terminus). Процесс репликации ДНК разделен на три стадии: инициация цепи, элонгация (удлинение) цепи и терминация.
Инициация синтеза цепи ДНК может происходить только при наличии затравки для ДНК-полимеразы. Вид затравки и способ ее образования различаются у разных вирусов и определяют своеобразие вирусных репликативных систем. Различают три основных способа инициации синтеза ДНК:
Инициация на внутренних участках ДНК — характерна для кольцевых матриц. Затравкой служит олигорибонуклеотид, который может быть синтезирован ДНК-зависимой РНК-полимеразой, праймазой или праймосомой. Эти ферменты могут иметь клеточное происхождение, или быть вирус-специфическими. Синтезироваться может одна затравка или несколько затравок.
На однонитевой матрице затравка синтезируется на определенном участке, узнаваемом ферментом. Двухнитевая матрица сначала подготавливается к инициации. На участке ori происходит присоединение хеликазы. Этот фермент расплетает участок матрицы, что приводит к образованию репликативной вилки с последующим синтезом затравки. Инициация на концах ДНК (терминальная инициация) — характерна для линейных матриц. Различают две группы способов концевой инициации ДНК-синтеза: с использованием нуклеотидбелковой затравки и с использованием самозатравочного механизма.
Инициация синтеза с использовании разрывов и брешей — затравкой для дальнейшего удлинения цепи может быть 3'-ОН конец разорванной цепи ДНК.
Элонгация цепи при репликации вирусных геномов принципиально не отличается от процесса синтеза клеточных ДНК. Используются ферменты, вспомогательные белки и репликационные белки, принадлежащие как клетке хозяина, так и вирусу. Синтез ДНК, как правило, осуществляет ДНК-зависимая ДНК-полимераза II, в редких случаях — ДНК-полимераза III. Основным свойством синтеза является его полярность, при которой очередной нуклеотид присоединяется к 3'-концу растущей цепи. То есть направление синтеза идет от 5'- к 3'-концу, считывание - от 3'- к 5'-концу. Особенности синтеза комплементарных нитей связаны со способом инициации. На днДНК матрице синтез идет через образование репликативной вилки или с вытеснением цепи, на онДНК-матрице — по-репарационному механизму.
Жизненный цикл
Вирусы не размножаются клеточным делением, поскольку не имеют клеточного строения. Вместо этого они используют ресурсы клетки-хозяина для образования множественных копий самих себя, и их сборка происходит внутри клетки.
Условно жизненный цикл вируса можно разбить на несколько взаимоперекрывающихся этапов:
· Прикрепление представляет собой образование специфичной связи между белками вирусного капсида и рецепторами на поверхности клетки-хозяина. Это специфичное связывание определяет круг хозяев вируса. Например, ВИЧ поражает только определённый тип человеческих лейкоцитов. Это связано с тем, что оболочечный гликопротеин вируса gp120 специфично связывается с молекулой CD4 — хемокиновым рецептором, который обычно встречается на поверхности CD4-положительных T-лимфоцитов. Этот механизм обеспечивает инфицирование вирусом только тех клеток, которые способны осуществить его репликацию. Связывание с рецептором может вызвать конформационные изменения белка оболочки (или белка капсида в случае безоболочечного вируса), что в свою очередь служит сигналом к слиянию вирусной и клеточной мембран и проникновению вируса в клетку.
· Проникновение в клетку. На следующем этапе вирусу необходимо доставить внутрь клетки свой генетический материал. Некоторые вирусы также переносят внутрь клетки собственные белки, необходимые для её реализации (особенно это характерно для вирусов, содержащих негативные РНК). Различные вирусы для проникновения в клетку используют разные стратегии: например, пикорнавирусы впрыскивают свою РНК через плазматическую мембрану, а вирионы ортомиксовирусов захватываются клеткой в ходе эндоцитоза и попадают в кислую среду лизосом, где происходит депротеинизация вирусной частицы, после чего РНК в комплексе с вирусными белками преодолевает лизосомальную мембрану и попадает в цитоплазму. Вирусы также различают по тому, где происходит их репликация: часть вирусов (например, те же пикорнавирусы) размножается в цитоплазме клетки, а часть (например, ортомиксовирусы) в её ядре. Процесс инфицирования вирусами клеток грибов и растений отличается от инфицирования клеток животных. Растения имеют прочную клеточную стенку, состоящую из целлюлозы, а грибы — из хитина, так что большинство вирусов могут проникнуть в них только после повреждения клеточной стенки. Однако почти все вирусы растений (включая вирус табачной мозаики) могут перемещаться из клетки в клетку в форме одноцепочечных нуклеопротеиновых комплексов через плазмодесмы. Бактерии, как и растения, имеют крепкую клеточную стенку, которую вирусу, чтобы попасть внутрь, приходится повредить. Но в связи с тем, что клеточная стенка бактерий намного тоньше таковой у растений, некоторые вирусы выработали механизм впрыскивания генома в бактериальную клетку через толщу клеточной стенки, при котором капсид остаётся снаружи.
· Лишение оболочек представляет собой процесс потери капсида. Это достигается при помощи вирусных ферментов или ферментов клетки-хозяина, а может быть и результатом простой диссоциации. В конечном счёте вирусная геномная нуклеиновая кислота освобождается.
· Репликация вирусов подразумевает, прежде всего, репликацию генома. Репликация вируса включает синтез мРНК ранних генов вируса (с исключениями для вирусов, содержащих положительную РНК), синтез вирусных белков, возможно, сборку сложных белков и репликацию вирусного генома, которая запускается после активации ранних или регуляторных генов. Вслед за этим может последовать (у комплексных вирусов с крупными геномами) ещё один или несколько кругов дополнительного синтеза мРНК: «поздняя» экспрессия генов приводит к синтезу структурных или вирионных белков.
· Вслед за этим происходит сборка вирусных частиц, позже происходят некоторые модификации белков. У вирусов, таких как ВИЧ, такая модификация (иногда называемая созреванием) происходит после выхода вируса из клетки-хозяина.
· Выход из клетки. Вирусы могут покинуть клетку после лизиса, процесса, в ходе которого клетка погибает из-за разрыва мембраны и клеточной стенки, если такая есть. Эта особенность есть у многих бактериальных и некоторых животных вирусов. Некоторые вирусы подвергаются лизогенному циклу, где вирусный геном включается путём генетической рекомбинации в специальное место хромосомы клетки-хозяйки. Тогда вирусный геном называется провирусом, или, в случае бактериофага, профагом.Когда клетка делится, вирусный геном также удваивается. В пределах клетки вирус в основном не проявляет себя; однако в некоторый момент провирус или профаг может вызвать активацию вируса, который может вызвать лизис клеток-хозяев.
Активно размножающийся вирус не всегда убивает клетку-хозяина. Оболочечные вирусы обычно отделяются от клетки путём отпочковывания. В ходе этого процесса вирус обзаводится своей оболочкой, которая представляет собой модифицированный фрагмент клеточной мембраны хозяина или другой внутренней мембраны. ом, клетка может продолжать жить и продуцировать вирус.
Особенности жизненного цикла различных групп
Генетический материал внутри вирусных частиц и способ его репликации, значительно отличается у различных вирусов.
· ДНК-содержащие вирусы. Репликация генома у большинства ДНК-содержащих вирусов происходит в клеточном ядре. Если клетка имеет соответствующий рецептор на своей поверхности, эти вирусы проникают в клетку либо путём непосредственного слияния с клеточной мембраной (напр. герпесвирусы), либо — что бывает чаще — путём рецептор-зависимого эндоцитоза. Большинство ДНК-содержащих вирусов полностью полагаются на синтетический аппарат клетки-хозяина для производства их ДНК и РНК, а также последующего процессинга РНК. Однако вирусы с крупными геномами (например, поксвирусы) могут сами кодировать большую часть необходимых для этого белков. Геному вируса эукариот необходимо преодолеть ядерную мембрану для того, чтобы получить доступ к ферментам, синтезирующим ДНК и РНК, в случае же бактерифагов ему достаточно просто проникнуть в клетку.
· РНК-содержащие вирусы. Репликация таких вирусов обычно происходит в цитоплазме. РНК-содержащие вирусы можно подразделить на 4 группы в зависимости от способа их репликации. Механизм репликации определяется тем, является ли геном вируса одноцепочечным или двухцепочечным, вторым важным фактором в случае одноцепочечного генома является его полярность (может ли он непосредственно служить матрицей для синтеза белка рибосомами). Все РНК-вирусы используют собственную РНК-репликазу для копирования своих геномов.
· Вирусы, использующие обратную транскрипцию. Эти вирусы содержат одноцепочечную РНК (Retroviridae, Metaviridae, Pseudoviridae) или двухцепочечную ДНК (Caulimoviridae и Hepadnaviridae). РНК-содержащие вирусы, способные к обратной транскрипции (ретровирусы, например, ВИЧ), используют ДНК-копию генома как промежуточную молекулу при репликации, а содержащие ДНК (параретровирусы, например, вирус гепатита B) — РНК. В обоих случаях используется обратная транскриптаза, или РНК-зависимая-ДНК-полимераза. Ретровирусы встраивают ДНК, образующуюся в процессе обратной транскрипции, в геном хозяина, такое состояние вируса называется провирусом. Параретровирусы же этого не делают, хотя встроенные копии их генома могут давать начало инфекционным вирусам, особенно у растений. Вирусы, использующие обратную транскрипцию, восприимчивы к противововирусным препаратам, ингибирующим обратную транскриптазу, в том числе к зидовудину и ламивудину.
Классификация
Главной задачей классификации является описание разнообразия вирусов и группировка их на основании общих свойств. В 1962 году Андре Львов, Роберт Хорн и Пауль Турнье были первыми, кто разработал основные принципы классификации вирусов на основании Линнеевской иерархической системы. Основными таксонами в этой системе являются отдел, класс, порядок, семейство, род и вид. Вирусы были разделены на группы по общим свойствам (но не таковым у их хозяев) и типу нуклеиновых кислот в геномах.
Позднее был создан Международный комитет по таксономии вирусов. Однако в таксономии вирусов не применяются понятия «отдел» и «царство», поскольку их малый размер генома и высокая частота мутаций затрудняет выяснение родства групп старше порядка. По существу, классификация вирусов по Балтимору является дополнением более традиционной классификации.
Систематику и таксономию вирусов в настоящий момент кодифицирует и поддерживает Международный Комитет по Таксономии Вирусов (International Committee on Taxonomy of Viruses, ICTV), поддерживающий также и таксономическую базу The Universal Virus Database ICTVdB.
Классификация ICTV
Международный комитет по таксономии вирусов разработал современную классификацию вирусов и выделил основные свойства вирусов, имеющие больший вес для классификации с сохранением единообразия семейств.
Была разработана объединённая таксономия (универсальная система для классификации вирусов). Седьмой отчёт ICTV закрепил для первых пор понятие о виде вируса как о низшем таксоне в иерархии вирусов. Однако к настоящему моменту была изучена лишь небольшая часть от общего разнообразия вирусов, анализ образцов вирусов из человеческого организма выявил, что около 20 % последовательностей вирусных нуклеиновых кислот ещё не было рассмотрено ранее, а образцы из окружающей среды, например, морской воды и океанского дна, показали, что подавляющее большинство последовательностей являются совершенно новыми.
Основными таксономическими единицами являются:
- Отряд (-virales)
- Семейство (-viridae)
- Подсемейство (-virinae)
- Род (-virus)
- Вид (-virus)
Классификация по Балтимору
Лауреат Нобелевской премии биолог Дейвид Балтимор разработал классификацию вирусов по Балтимору. Классификация ICTV в настоящее время объединяется с классификацией по Балтимору, составляя современную систему классификации вирусов.
Классификация вирусов по Балтимору основывается на механизме образования мРНК. Вирусы должны синтезировать мРНК из собственных геномов для образования белков и репликации своей нуклеиновой кислоты, однако каждое семейство вирусов имеет собственный механизм осуществления этого. Вирусные геномы могут быть одноцепоченые (оц) или двухцепочечные (дц), ДНК- или РНК-содержащие, могут использовать или не использовать обратную транскриптазу. Кроме того, одноцепочечные РНК-вирусы могут иметь положительную (+) или отрицательную (-) цепь РНК в составе своего генома.
Эта система включает в себя семь основных групп:
- (I) Вирусы, содержащие двуцепочечную ДНК и не имеющие РНК-стадии (например, герпесвирусы, поксвирусы, паповавирусы, мимивирус).
- (II) Вирусы, содержащие одноцепочечную молекулу ДНК (например, парвовирусы). В этом случае ДНК всегда положительной полярности.
- (III) Вирусы, содержащие двуцепочечную РНК (например, ротавирусы).
- (IV) Вирусы, содержащие одноцепочечную молекулу РНК положительной полярности (например, пикорнавирусы, флавивирусы).
- (V) Вирусы, содержащие одноцепочечную молекулу РНК негативной или двойной полярности (например, ортомиксовирусы, филовирусы).
- (VI) Вирусы, содержащие одноцепочечную положительную молекулу РНК и имеющие в своем жизненном цикле стадию синтеза ДНК на матрице РНК, ретровирусы (например, ВИЧ).
- (VII) Вирусы, содержащие двуцепочечную ДНК и имеющие в своём жизненном цикле стадию синтеза ДНК на матрице РНК, ретроидные вирусы (например, вирус гепатита B).
Дальнейшее деление производится на основе таких признаков как структура генома (наличие сегментов, кольцевая или линейная молекула), генетическое сходство с другими вирусами, наличие липидной оболочки, таксономическая принадлежность организма-хозяина и так далее.
Роль в заболеваниях человека
Примерами наиболее известных вирусных заболеваний человека могут служить простуда (она может иметь и бактериальную этиологию), грипп, ветряная оспа и простой герпес. Многие серьёзные болезни, например, геморрагическая лихорадка Эбола, СПИД, птичий грипп и тяжёлый острый респираторный синдром вызываются вирусами. Относительная способность вируса вызывать заболевание характеризуется термином вирулентность. Некоторые заболевания исследуются на наличие вирусов в числе вызывающих агентов, например, возможна связь между человеческим герпесвирусом 6 типа нейрологическими заболеваниями, такими как рассеянный склероз и синдром хронической усталости. Идут споры по поводу того, что борнавирус, ранее считавшийся возбудителем нейрологических заболеваний у лошадей, возможно, вызывает психические расстройства у людей. Вирусы имеют различные механизмы, вызывающие болезнь у хозяина, и эти механизмы сильно зависят от вида. Такой механизм на клеточном уровне включает, прежде всего, лизис клеток, приводящий к их смерти. У многоклеточных организмов, при гибели большого числа клеток, начинает страдать организм в целом. Хотя вирусы подрывают нормальный гомеостаз, приводя к заболеванию, они могут существовать внутри организма и относительно безвредно. В качестве примера можно привести способность вируса простого герпеса первого типа пребывать в состоянии покоя внутри тела человека. Такое состояние называется латентностью. Оно характерно для вирусов герпеса, в том числе вируса Эпштейна-Барр, вызывающего инфекционный мононуклеоз, а также вируса, вызывающего ветрянку и опоясывающий лишай. Большинство людей переболели по крайней мере одним из этих типов вируса герпеса. Однако такие латентные вирусы могут и принести пользу, поскольку присутствие этих вирусов может вызвать иммунный ответ против бактериальных патогенов, например, чумной палочки (Yersinia pestis).
Некоторые вирусы могут вызывать пожизненные или хронические инфекции, при которых вирус продолжает размножаться в теле организма, несмотря на его защитные механизмы[148]. Так происходит, например, при инфекциях, вызванных вирусами гепатита B и C. Хронически больные люди известны как носители, поскольку они выступают в роли резервуара для заразного вируса. Если в популяции имеется высокая доля носителей, то в этом случае говорят об эпидемии.
Защитная реакция хозяина
Первой защитной линией организма против вируса является врождённый иммунитет. Он включает клетки и другие механизмы, обеспечивающие неспецифическую защиту. Это значит, что клетки врождённого иммунитета распознают и реагируют на патогены общими способами, одинаково по отношению ко всем патогенам, но, в отличие от приобретённого иммунитета, врождённый иммунитет не даёт продолжительной и надёжной защиты хозяину.
Важным врождённым способом защиты организма эукариот против вирусов является РНК-интерференция. Стратегия репликации многих вирусов предполагает наличие стадии двуцепочечной РНК. Для борьбы с подобными вирусами, клетка имеет систему неспецифической деградации одно- и двуцепочечных РНК. Когда подобный вирус попадает в клетку и освобождает геномную РНК в цитоплазму, белковый комплекс Dicer связывает и вирусную РНК на короткие фрагменты. Активируется биохимический путь, называемый RISC, который разрушает вирусную РНК, и препятствует размножению вируса. Ротавирусам удаётся избежать РНК-интерференции, сохраняя часть капсида даже внутри клетки и выпуская новообразованные мРНК через поры во внутреннем капсиде. Геномная двуцепочечная РНК же остаётся внутри него.
Когда система приобретённого иммунитета у позвоночных сталкивается с вирусом, она образует специфические антитела, присоединяющиеся к вирусу и часто делающие его неопасным. Это называется гуморальным иммунитетом. Наиболее важными являются два типа антител. Первый, называемый IgM, обладает высокой эффективностью в нейтрализации вирусов, но образуется клетками иммунной системы лишь в течение нескольких недель. Синтез второго — IgG — продолжается неопределённо долго. Присутствие IgM в крови хозяина говорит о наличии острой инфекции, в то время IgG свидетельствует об инфекции, перенесённой в прошлом. Именно количество IgG измеряется при тестах на иммунитет. Антитела могут продолжать оставаться эффективным защитным механизмом даже тогда, когда вирусу удаётся проникнуть в клетку. Клеточный белок TRIM21 может прикреплять антитела к поверхности вирусных частиц. Это вызывает последующее разрушение вирусной частицы ферментами клеточной протеосомной системы.
Второй защитный механизм позвоночных против вирусов называется клеточным иммунитетом и включает иммунные клетки, известные как T-лимфоциты. Клетки тела постоянно несут короткие фрагменты собственных белков на своих поверхностях, и, если Т-лимфоциты распознают здесь подозрительные вирусные фрагменты, клетка-хозяин разрушается клетками, называемыми Т-киллерами, и начинается образование специфичных к вирусу T-лимфоцитов. Такие клетки, как макрофаги, специализируются на презентации антигенов. Важной защитной реакцией хозяина является продукция интерферона. Интерферон — это гормон, образуемый организмом в ответ на присутствие вируса. Его роль в иммунитете — комплексная, в конце концов он останавливает вирус, прекращая образование новых вирусов поражёнными клетками, убивая их и их близких соседей.
Не против всех вирусов образуется такой защитный иммунный ответ. ВИЧ удаётся избежать иммунного ответа, постоянно меняя последовательность аминокислот поверхностных белков вириона. Такие устойчивые вирусы уходят от иммунной системы, изолируясь от иммунных клеток, блокируя презентацию антигенов, благодаря устойчивости к цитокинам, уклоняясь от естественных киллеров, останавливая апоптоз клеток-хозяев, а также за счёт антигенной изменчивости. Другие вирусы, называемые нейротропными вирусами, распространяются среди нервных клеток, то есть там, где иммунная система не в состоянии добраться до них.
Рак
Рак — вид злокачественной опухоли, развивающейся из клеток эпителиальной ткани различных органов (кожи, слизистых оболочек и многих внутренних органов).
Рак составляет подавляющее большинство всех злокачественных новообразований человека, к которым также относятся многочисленные саркомы, гемобластозы, глиальные, костные и другие опухоли. В некоторых странах под раком понимают любое злокачественное новообразование.
Общей характеристикой злокачественных опухолей является их выраженный клеточный атипизм (утрата клетками способности к дифференцировке с нарушением структуры ткани, из которой происходит опухоль), агрессивный рост с поражением как самого органа, так и других близлежащих органов, склонность к метастазированию, то есть к распространению клеток опухоли с током лимфы или крови по всему организму с образованием новых очагов опухолевого роста во многих органах, удалённых от первичного очага. По темпам роста большинство злокачественных опухолей превосходят доброкачественные и, как правило, могут достигать значительных размеров в короткие сроки. Различают также вид злокачественных местнодеструктирующих опухолей, которые растут с образованием инфильтрата в толще ткани, приводя к её разрушению, но, как правило, не метастазируют.
Раковая опухоль состоит из основной ткани, определяющей её природу (эпителиальной паренхимы), и соединительнотканного «каркаса» (стромы) с кровеносными и лимфатическими сосудами. В соответствии с выделением двух типов нормального эпителия ≈ цилиндрического и плоского ≈ различают цилиндроклеточный Р. (железистый Р., аденокарционома) и плоскоклеточный Р. Первый берёт начало чаще всего из клеток желёз, расположенных в слизистых оболочках желудочно-кишечного тракта, второй ≈ из покровных клеток кожи и слизистых оболочек рта, дыхательных, мочевых и половых путей. В зависимости от степени развития стромы опухоль может быть плотной (скирр) и мягкой (медуллярный, или мозговидный, Р.).
Возникновение раковой опухоли
Опухоль возникает вследствие нарушения процессов обмена веществ в клетках и ослабления контроля за внутриклеточными процессами со стороны организма. В результате приобретения новых качеств и частичной независимости от регуляторных систем организма, молодые делящиеся клетки теряют способность к дифференцировке — они не приобретают должных функций и не формируют нормально работающую ткань. Не участвуя в жизнедеятельности организма, такие клетки становятся ненужными ему, лишними. Организм пытается избавиться от них при помощи иммунных реакций, которые не всегда оказываются эффективными. Избыток молодых, все время размножающихся, но не работающих клеток, к тому же требующих все возрастающего количества энергетических и пищевых ресурсов, ведет к тому, что такие клетки нападают на породившую их ткань или орган. Эти клетки (они и называются опухолевыми) внедряются в ткани органа, инфильтрируют (см. Инфильтрат) и разрушают их, захватывают кровеносные и лимфатические сосуды, по которым распространяются по организму — метастазируют.
Причины рака. Онкогенез
О причинах появления опухоли известно не все. Предрасположенность к раку того или иного органа (например, молочной железы, желудка) наследуется, то есть носит семейный характер. Наследуются гормональные отклонения в организме или местные структурные нарушения в каком-либо органе (полипоз кишечника, родимые пятна на коже и т. д.). Эти отклонения и неправильности и могут привести к развитию опухоли, что отметил еще более ста лет тому назад немецкий патолог Юлиус Фридрих Конгейм. Однако для возникновения опухоли — онкогенеза — одних тканевых уродств недостаточно. Необходимы мутагенные стимулы, вызывающие изменения в наследственном аппарате клетки и затем опухолевую трансформацию. Такие стимулы могут быть внутренними (например, повышенная выработка гормонов или других продуктов метаболизма, их дисбаланс) или внешними — физическими (например, ионизирующее или ультрафиолетовое излучения), химическими, вирусной природы и т. д. Эти факторы обладают мутагенным и, тем самым, канцерогенным воздействием, которое запускает механизм, производящий раковые клетки во все возрастающем количестве.
Считается, что программу опухолевого роста имеет любая клетка. Эта программа записана в специальных генах — онкогенах. В обычных условиях онкогены жестко блокированы (репрессированы), но под воздействие мутагенов блокада может сниматься, и онкогены получают возможность работать. Известно также, что многие канцерогены подавляют иммунную систему организма, освобождая от ее жесткого и постоянного контроля отклонившиеся от нормы клетки. Контрольные и восстанавливающие функции иммунной системы резко ослабевают в старости, когда чаще всего и появляется злокачественная опухоль.
Инфекции (вирусы), вызывающие рак
Как правило, вирусы, вызывающие рак, вызывают опухолевую трансформацию, сопровождающуюся включением генома вируса в геном клетки. Часть вирусного генома в опухолевых клетках активна и определяет синтез нескольких специфических антигенов, локализующихся на поверхности клеток (специфический трансплантационный антиген) и в ядре (так называемый Т-антиген). В клетках опухолей, индуцированных. ДНК-содержащими вирусами (аденовирусы и вирусы группы папова), синтеза полных вирусных частиц обычно не происходит, но такой синтез может быть индуцирован специальными экспериментальными приемами. В клетках лейкозов и опухолей, индуцированных РНК-содержащими вирусами, может иметь место синтез полных вирусных частиц.
В зависимости от ответа на вирусную инфекцию клетки делятся на два класса:
1. Пермиссионные (позволяющие) клетки продуктивно инфицируются, то есть в них
происходит полный жизненный цикл вируса, сопровождающийся репликацией вируса,
лизисом клетки и выходом наружу вирусных частиц.
2. Непермиссионные клетки подавляют репликацию вируса. При этом может
происходить интеграция вирусного генома в клеточный, что может
сопровождаться трансформацией.
Вирус полиомы – малый ДНК-содержащий вирус, найденный у мышей. Его аналоги
найдены у макаки резус (вирус SV40) и человека (вирусы BK и JC). В пермиссионных
клетках естественных хозяев они не вызывают трансформации. Например, вирусы ВК и JC онкогенны для грызунов, но не человека. Геном вирусов разделен на две части – раннюю и позднюю в соответствии со временем ее активной экспрессии в жизненном цикле вируса. В ранней области закодированы два белка – большой и малый Т-антиген (Tumor), транскрибируемые с одного гена в результате альтернативного сплайсинга. В пермиссионных клетках они инициируют репликацию вирусной ДНК и стимулируют синтез ДНК и экспрессию генов хозяина, в том числе и контролирующих пролиферацию. В непермиссионных клетках, где репликация вируса подавлена, повышенная пролиферация может приводить к трансформации.
Вирус папилломы – малый ДНК вирус, вызывающий эпителиальные опухоли.
Известно 75 видов вируса HPV (Human Papilloma Virus), многие из которых связаны с
доброкачественным ростом, например, возникновением бородавок. Некоторые же из этих
вирусов вызывают рак. В частности, цервикальный рак может быть связан с экспрессией
вирусных белков Е6 и Е7, иммортализующих клетку путем подавления активности Rb и р53 соответственно.
Аденовирус человека был изолирован из аденоидов. Сходные вирусы найдены у
других млекопитающих. Это большая группа близкородственных вирусов, состоящая из более 80 индивидуальных членов. Наиболее охарактеризованы аденовирусы человека, так как они вызывают простудные заболевания. Эти вирусы способны инфицировать большое число клеток. Клетки человека являются пермиссионным, и, следовательно, продуктивно инфицируются. Все аденовирусы способны трансформировать лишь непермиссионные клетки, к которым относятся клетки некоторых грызунов. Наиболее эффективно трансформирующее действие аденовируса проявляется на новорожденных грызунах. Трансформирующее действие аденовируса аналогично действию вируса полиомы и связано с подавлением действия Rb и р53 продуктами ранних генов Е1А и Е1В.
Вирус Эпштейна-Барра (EBV) – один из представителей семейства вирусов
герпеса, связанный со многими болезнями человека (мононуклеозис, назофарингальная
карцинома, лимфома Беркита и другие лимфопролиферативные болезни). В-лимфоциты человека инфицируются этим вирусом in vitro и становятся иммортализованными. Вирусную ДНК находят и в трансформированных клетках. Остается до конца неизвестным, какие гены EBV вызывают трансформацию. Идентифицирован белок BNLF-1, который, видимо, активирует определенные клеточные гены.
Ретровирусы кардинально отличаются от вирусов, упомянутых ранее, по их
способности переносить генетическую информацию не только горизонтально, но и
вертикально. Горизонтальный перенос – это нормальный процесс вирусной инфекции, при котором увеличивается число пораженных клеток у одного хозяина. Вертикальный перенос связан с интеграцией вируса в половые клетки в качестве эндогенного провируса. Он наследуется по законам Менделя. Жизненный цикл вируса осуществляется при помощи обратной транскрипции: РНК- оцДНК-дцДНК – интеграция в геном- инфекционная РНК. Интеграция в геном приводит к вертикальной трансмиссии провируса. Экспрессия провируса может генерировать ретровирусные частицы, которые передают генетическую информацию горизонтально.
По способности вызывать рак опухолевые ретровирусы делятся на две большие группы:
1. Недефективные вирусы, которые имеют обычный для ретровирусов жизненный
цикл. Они имеют длинный латентный период и часто связаны с возникновением лейкемий. Существует две классические модели: FeLV (Feline leukemia virus) и MMTV (mouse mammary tumor virus). Опухолеобразование не связано с определенными вирусными ПО, а со способностью вируса активировать клеточные ПО.
2. Быстро трансформирующие вирусы передают новую для клетки генетическую
информацию в виде ПО. Если в вирусе не содержится онкоген, то вирус не представляет
опасности. ПО становится оригинальным клеточным геном. Быстро трансформирующие вирусы быстро вызывают рак и могут трансформировать клетки in vitro. Ретровирус захватывает клеточный ген путем обмена своей собственной последовательности на клеточную. Такая трансдукция вируса имеет два очень важных свойства:
1. Такой вирус, содержащий клеточный ген, обычно не может сам
реплицироваться, так как вирусным генам для репродукции не нужен обмен с клеточным
геном. Все такие вирусы дефектны, но они могут инфицировать с помощью «помощника» – вируса дикого типа, который обеспечивает функции, потерянные при рекомбинации.
2. Во время инфекции трансдуцирующий вирус несет клеточные гены, которые
получены им в результате рекомбинантных событий и их экспрессия может повреждать
фенотип инфицированной клетки. Вирус, несущий информацию о росте клетки, имеет
преимущество в будущем цикле инфекции. После захвата вирусом клеточного гена, в нем
может случиться мутация и его влияние на фенотип клетки усилится. Конечно, трансфекция не является единственным механизмом влияния ретровируса на клетку хозяина. Вирус иммунодефицита человека (ВИЧ-1 или HIV-1) инфицирует и убивает Т -
лимфоциты, снижая таким образом активность иммунной системы и индуцируя СПИД. ВИЧ не трансформирует клетки, однако больные часто страдают некоторыми видами рака, в частности лимфомами и саркомой Капоши. В вирусах идентифицировано более 30 клеточных онкогенов. Обычно вирусы несут один онкоген. Вирусный онкоген обозначают как v-onc, а клеточный – c-onc. Существует две модели, объясняющие различие между вирусными и клеточными онкогенами. Количественная модель предполагает, что вирусные онкогены качественно не отличаются от клеточных, но их экспрессия повышена или ее не возможно выключить. Качественная модель предполагает, что клеточные онкогены действительно теряют онкогенные свойства, но могут быть конвертированы мутацией в онкоген. Каждый онкоген может вести себя в соответствии с какой-либо из этих двух моделей.
Об онкогенном потенциале трансформирующих вирусов свидетельствуют следующие
факторы:
1. Мутации в вирусных онкогенах понижают их трансформационную активность.
2. Обнаружены события, при которых клеточный онкоген становится онкогеным.
Например, это происходит при изменении последовательности клеточного онкогена. Прямые доказательства того, что экспрессия вирусных онкогенов сопровождается трансформацией, получены на примере вируса саркомы Рауса. Чувствительные к температуре мутации в v-src при повышении температуры возвращали клетки от трансформированного фетотипа к нормальному, тогда как понижение температуры реверсировало трансформированный фенотип. Src – пример гена, свойства которого напоминают c-onc. V-src онкогенен при низких
уровнях экспрессии белка, c-src – при высоких (более 10 от нормы). Некоторые ПО слабо
онкогенны при повышении их экспрессии, но найденные изменения в v-onc или появляющиеся изменения в c-onc обладают более эффективной трансформирующей способностью (Например, ras и myc). В некоторых случаях v-onc образуются при потере последовательностей, кодирующих С-конец или N-конец (или оба), вероятно, в результате рекомбинантных процессов. Потеря этих областей может устранять регуляторный контроль над v-onc, который в норме лимитирует активность c-onc. Такие изменения в последовательности необходимы для src. V-src – онкоген при низкой концентрации, c-src – не онкоген даже при относительно высоком содержании белка (в десять раз больше нормы). Концепция, что ОГ активируются от ПОГ – важная парадигма для рака животных. У человека в большинство событий вирусные интермедиаты не вовлечены в процесс трансформации.
Формы рака
Раковая ткань представляет собой весьма подвижное и изменчивое образование. Поведение ее зависит от множества факторов, в том числе от интенсивности защитных противораковых реакций, на которые способен организм в том или ином конкретном случае. Иммунная система человека может частично или полностью разрушить опухоль. Она также может блокировать раковые клетки на начальной стадии и не дать им возможности проникнуть вглубь органа (неинвазивный рак, или «рак на месте» — «in situ»). В названии формы рака находят отражение: принадлежность к тому или иному органу (рак легких, рак яичников и т. д.), вид эпителия, служащий источником опухоли (рак плоскоклеточный, железистый — аденокарцинома, базальноклеточный и т. д.), скорость роста, гистологическим эквивалентом которой служит степень зрелости раковой ткани (рак дифференцированный и недифференцированный), свойства, связанные со степенью зрелости опухоли и эффективностью иммунных реакций в ней (рак агрессивный, стабильный, регрессивный).
Клиника, диагностика, профилактика и лечение рака
Симптомы заболевания раком появляются сравнительно поздно, когда опухоль достигает значительных размеров и нарушает функции органа, в котором растет. Если орган полый, может нарушиться его проходимость, появляются патологические (воспалительного или иного характера) выделения, возможны кровотечения. Больной ощущает слабость, худеет, у него повышается температура тела, он испытывает боли, увеличивается скорость оседания эритроцитов.
Важнейший принцип диагностики рака — ее своевременность, выявление опухоли на ранней (доклинической) стадии, когда выздоровление наступает у 80-95% больных. Для этого используются все известные современной медицине методы: клинические, биохимические, иммунологические, рентгенологические, ультразвуковые, эндоскопические, цитологические, гистологические со взятием биопсии. Эффективность совокупного их применения очень высока.
Профилактика рака — это, во-первых, выявление его на начальной стадии при массовом обследовании той части населения, которую относят к группе повышенного риска. Для этого используют флюорографию легких, маммографию, мазки из шейки матки и т. д. Другая задача профилактики — создание для людей оптимальных условий существования со сведением к минимуму загрязненности среды обитания, с уменьшением вероятности контакта организма с канцерогенными факторами, общее оздоровление населения. Подобные мероприятия могут существенно снизить заболеваемость злокачественными опухолями.
Лечение рака — хирургическое, а также с применением гормонов, лучевой терапии и химиотерапевтических средств. Для повышения защитных сил организма прибегают к воздействию на иммунную систему. Различные методы лечения часто используют в сочетании друг с другом — в зависимости от стадии заболевания, локализации опухоли, тканевой ее принадлежности и других факторов. Существует множество хороших клиник для лечения этой болезни. В России хороший онкологический центр в Екатеринбурге, возможно лечение в клиниках Германии, и в др.
Лечение рака зависит от типа опухоли, её локализации, строения, стадии заболевания в соответствии с классификацией TNM.
Различают следующие типы лечения:
- Хирургическое удаление опухоли с прилежащими тканями. Эффективно для лечения опухолей небольших размеров, доступных для хирургического вмешательства, и при отсутствии метастазов. Нередко после хирургического лечения могут возникать рецидивы опухоли.
- Лучевая терапия применяется для лечения малодифференцированных опухолей, чувствительных к радиации. Также применяются для локального разрушения метастазов.
- Химиотерапия используется для лечения различных, зачастую, поздних стадий рака с использованием цитотоксических средств, гормональных/антигормональных средств, иммунных препаратов, ферментных препаратов, противоопухолевых антибиотиков и других лекарственных препаратов, которые разрушают или замедляют рост раковых клеток.
- Генная терапия наиболее современный метод лечения, суть которого заключается в воздействии на систему STAT (signal transduction and activator of transcription) и другие системы, тем самым регулируя процесс деления клеток.
- Нейтронная терапия — новый метод лечения опухоли, похожий на лучевую терапию, но отличающийся от неё тем, что используются нейтроны вместо обычного облучения. Нейтроны проникают глубоко в ткани опухоли, поглотившие, например, бор, и уничтожают их, не повреждая при этом здоровые ткани в отличие от радиотерапии. Данная терапия показала очень высокий процент полного выздоровления в лечении опухолей, составляющий 73,3 % даже на запущенной стадии. По данным на начало 2011 года на территории Российской Федерации имеется 2 центра лечения онкологических заболеваний нейтронной терапией.
- Иммунотерапия. Иммунная система стремится уничтожить опухоль. Однако она в силу ряда причин часто не в состоянии это сделать. Иммунотерапия помогает иммунной системе бороться с опухолью, заставляя её атаковать опухоль эффективнее или делая опухоль более чувствительной. Вакцина Вильяма Коли, а также вариант данной вакцины — пицибанил, являются эффективными при лечении некоторых форм новообразований благодаря стимулированию активности натуральных киллеров и выработке ряда цитокинов, таких как фактор некроза опухоли и интерлейкин-.Для активации защитных иммунных механизмов может применяться эпигенетическая терапия.
На данный момент наиболее хорошие результаты в лечении рака наблюдаются при использовании комбинированных методов лечения (хирургического, лучевого и химиотерапевтического).
Распространенность рака (эпидемиология)
Рак — болезнь пожилых людей. В индустриально развитых странах Запада он занимает второе место после сердечно-сосудистых заболеваний в перечне причин смерти и, несмотря на усилия медиков, не уступает его уже много десятилетий подряд. Происходит даже рост заболеваемости раком в этих странах (с 1960 по 1980 год — в полтора раза), связанный, как полагают, с постарением населения и ухудшением экологических условий в больших городах. Шесть миллионов умерших (в 1996 году — 6,3 млн.) — такова ежегодная дань человечества злокачественной опухоли.
В некоторых случаях рак отступает. Так, реализация социальной программы по борьбе с раком желудка в Японии за сравнительно короткое время привела к снижению заболеваемости почти в два раза. Значительное снижение заболеваемости раком желудка отмечено также в Соединенных Штатах Америки и странах Европы. Связано оно, однако, с немедицинскими факторами. «Виновником» частичной победы над опухолью оказался бытовой холодильник, коренным образом изменивший традиционные методы консервации пищевых продуктов солением и копчением.
У разных народов и в разных географических зонах распространены разные формы рака. Япония и Россия «больны» раком желудка. В США, развитых странах Европы, а также в крупных городах России преобладают рак легких и рак молочной железы (в Москве в 1996 году от всех форм рака умерло 225 тысяч человек). Это результат загрязнения среды обитания промышленными отходами, выхлопными газами автомобилей, курения табака, а также не всегда оправданного отказа от грудного вскармливания новорожденных. В Африке национальное бедствие — рак печени (малобелковая пища), в Монголии и Казахстане — рак пищевода (обжигающе горячая и жирная пища), в Индии и Средней Азии — рак полости рта (привычка жевать бетель). Пристрастие американцев к легко усваиваемым продуктам без клетчатки (к «быстрой еде») привело к росту в стране рака толстой и прямой кишок.
Перемена места жительства людей сопровождается постепенным снижением (через поколение) заболеваемости «родным» раком и приобретением предрасположенности к раку, преобладающему в новой стране проживания. Распространенность различных форм рака изучают, анализируя условия жизни, привычки и особенности питания населения, минеральный состав почвы и воды, всю совокупность экологических условий; составляются и специальные карты, отражающие число заболеваний различными формами рака в конкретных населенных пунктах определенного региона.
Наука о раке называется — онкология (от греческого onkos — опухоль и logos — слово, учение) — медико-биологическая наука, изучающая теоретические, экспериментальные и клинические аспекты онкогенеза у человека, животных, растений и разрабатывающая методы распознавания, лечения и профилактики опухолей.
Онкология сформировалась в 20 веке на основе достижений экспериментальной медицины. В экспериментальной (начиная с трудов российского ученого Мстислава Александровича Новинского, 1876) и теоретической онкологии сложились 3 основных направления: вирусное (французский ученый Амадей Боррель, 1903; американский патолог и онколог — Фрэнсис Роус, 1911), химическое (японские ученые К. Ямагива и К. Итикава, 1915) и радиационное (французский ученый и радиолог Антуан Лакассань, 1932, и другие) в зависимости от индуцирующего агента. В СССР ученый, микробиолог и иммунолог Лев Александрович Зильбер создал вирусогенетическую теорию опухолей. Быстрое развитие клинической онкологии связано с достижениями хирургии, радиологии, химиотерапии и иммунологии.
| <== предыдущая | | | следующая ==> |
| Коллективы | | | Понятие информационной культуры |
Date: 2015-05-22; view: 545; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |