
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химические формулы
Любое вещество может быть охарактеризовано качественным и количественным составом. Под качественным составом понимают набор химических элементов, образующих вещество, под количественным, в общем случае, соотношение между числом атомов этих элементов. Атомы, образующие молекулу, соединяются между собой в определенной последовательности, эта последовательность называется химическим строением вещества (молекулы).
Состав и строение молекулы может быть изображено с помощью химических формул. Качественный состав записывается в виде символов химических элементов, количественный – в виде подстрочных индексов у символа каждого элемента. Например: С6Н12О6.
Химическая формула - это условная запись состава вещества с помощью химических знаков (предложены в 1814 г. Й. Берцелиусом) и индексов (индекс - цифра, стоящая справа внизу от символа. Обозначает число атомов в молекуле). Химическая формула показывает, атомы каких элементов и в каком отношении соединены между собой в молекуле.
Химические формулы бывают следующих видов:
а) молекулярные – показывают сколько атомов элементов входят в состав молекулы вещества, например Н2О – одна молекула воды содержит два атома водорода и один атом кислорода.
б) графические – показывают в каком порядке связаны атомы в молекуле, каждая связь изображается черточкой, для предыдущего примера графическая формула будет выглядеть так: Н—О—Н
в) структурные – показывают взаимное расположения в пространстве и расстояния между атомами, входящими в состав молекулы.
Необходимо иметь в виду, что однозначно идентифицировать вещество позволяют только структурные формулы, молекулярные или графические формулы могут соответствовать нескольким или даже многим веществам (особенно в органической химии).
Международная единица атомных масс равна 1/12 массы изотопа 12C - основного изотопа природного углерода.
1 а.е.м = 1/12 m (12C) = 1,66057 10-24 г
Относительная атомная масса (Ar) - безразмерная величина, равная отношению средней массы атома элемента (с учетом процентного содержания изотопов в природе) к 1/12 массы атома 12C.
Средняя абсолютная масса атома (m) равна относительной атомной массе, умноженной на а.е.м.
Ar(Mg) = 24,312
m (Mg) = 24,312·1,66057 · 10-24 = 4,037 · 10-23 г
Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода 12C.
Mr = mг / (1/12 mа(12C))
mr - масса молекулы данного вещества;
mа(12C) - масса атома углерода 12C.
Mr = S Aг(э). Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов с учетом индексов.
Примеры.
Mr(B2O3) = 2 · Ar(B) + 3 · Ar(O) = 2 · 11 + 3 · 16 = 70
Mr (KAl(SO4)2) = 1 · Ar(K) + 1 · Ar(Al) + 1· 2 · Ar(S) + 2· 4 · Ar(O) == 1 · 39 + 1 · 27 + 1 · 2 · 32 + 2 · 4 ·16 = = 258
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на а.е.м. Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют специальную единицу измерения - моль.
Количество вещества, моль. Означает определенное число структурных элементов (молекул, атомов, ионов). Обозначается n, измеряется в моль. Моль - количество вещества, содержащее столько же частиц, сколько содержится атомов в 12 г углерода.
Число Авогадро (NA). Количество частиц в 1 моль любого вещества одно и то же и равно 6,02 · 1023. (Постоянная Авогадро имеет размерность - моль-1).
Пример.
Сколько молекул содержится в 6,4 г серы?
Молекулярная масса серы равна 32 г /моль. Определяем количество г/моль вещества в 6,4 г серы:
n(s) = m(s) / M(s) = 6,4г / 32 г/моль = 0,2 моль
Определим число структурных единиц (молекул), используя постоянную Авогадро NA
N(s) = n(s) · NA = 0,2· 6,02· 1023 = 1,2· 1023
Молярная масса показывает массу 1 моля вещества (обозначается M).
M = m / n
Молярная масса вещества равна отношению массы вещества к соответствующему количеству вещества.
Молярная масса вещества численно равна его относительной молекулярной массе, однако первая величина имеет размерность г/моль, а вторая - безразмерная.
M = NА · m(1 молекула) = NА · Mг · 1 а.е.м. = (NА · 1 а.е.м.) · Mr = Mr
Это означает, что если масса некоторой молекулы равна, например, 80 а.е.м. (SO3), то масса одного моля молекул равна 80 г. Постоянная Авогадро является коэффициентом пропорциональности, обеспечивающим переход от молекулярных соотношений к молярным. Все утверждения относительно молекул остаются справедливыми для молей (при замене, в случае необходимости, а.е.м. на г) Например, уравнение реакции: 2Na + Cl2 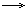 2NaCl, означает, что два атома натрия реагируют с одной молекулой хлора или, что одно и то же, два моль натрия реагируют с одним молем хлора.
2NaCl, означает, что два атома натрия реагируют с одной молекулой хлора или, что одно и то же, два моль натрия реагируют с одним молем хлора.
Date: 2015-05-22; view: 660; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |