
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Свойства веществ
1. Амфотерный характер имеет оксид:
1) Na2O
2) CO
3) CuO
4) Al2O3
2. Среди приведенных реакций укажите уравнение гидролиза:
1) BaCl2 + Na2SO4→ BaSO4↓ +2NaCl
2) HClO4 + NaOH → NaClO4 + H2O
3) Na2CO3 + 2HCl→ CO2↑ + H2O + 2NaCl
4) ZnCl2 + H2O↔ZnOHCl + HCl
3. Степень окисления азота в аммиаке NH3 равна:
1) +1
2) +2
3) +3
4) -3
4. Уравнение реакции гидролиза имеет вид:
1) ZnSO4 + 2NaOH = Zn (OH) 2 + Na2SO4
2) CaCl2 + 2AgNO3 = 2AgCl↓ + Ca(NO3) 2
3) Na NO3 + HCl = NaCl + HNO3
4) NH4NO3 + H2O ↔ NH4OH + HNO3
5. Химическая реакция между растворами хлорида калия и нитрата серебра является реакцией:
1) нейтрализации
2) гидролиза
3) обмена
4) окислительной
6. Для цепочки превращений Na2O ( H2O) → X1 HNO3→ X2 (t) → Х3 конечным веществом Х3 является:
1) NaNO3
2) NaNO2
3) NaOH
4) HNO2
7. Коэффициент перед молекулой восстановителя в уравнении реакции равен:
KNO2 + K2Cr2O7 + H2SO4 = KNO3 + Cr2 (SO4) 3 + K2SO4 + H2O
1) 1
2) 2
3) 3
4) 5
8. Формула высшего оксида элемента, образующего водородное соединение ЭН3 имеет вид:
1) ЭО
2) ЭО2
3) Э2О5
4) ЭО4
9. Уравнение реакции, практически осуществимой в водном растворе, имеет вид:
1) KCl + HNO3 → KNO3 + HCl
2) CaCl2 + 2NaOH → 2NaCI + Ca(OH)2 ↓
3) Al2(SO4)3 + 6HCl → 2AlCl3 + 3H2SO4
4) 2NaNO3 + H2SO4 → Na2SO4 + 2HNO3
10. BaH2+H2O→ Ba(OH)2 +..... Пропущенным веществом в схеме химической реакции является:
1) O2
2) H2
3) BaO
4) H2O
11. Для цепочки превращений Ca → (HCl) Х1 → (KOH) Х2→ (t) Х3 конечным веществом Х3 является:
1) Ca(OH)2
2) CaO
3) Ca
4) CaO2
12. При взаимодействии оксида углерода (IV) с избытком KOH образуется:
1) гидрокарбонат калия
2) карбонат калия
3) карбонат калия и вода
4) гидрокарбонат калия и вода
13. С кислотами и щелочами взаимодействует оксид:
1) железа(III)
2) железа(II)
3) алюминия(III)
4) меди(II)
14. Формула высшего оксида элемента, образующего водородное соединение ЭН2 имеет вид:
1) ЭО
2) ЭО2
3) Э2О5
4) ЭО4
15. Уравнение реакции, практически осуществимой в водном растворе, имеет вид:
1) KCl + HNO3 → KNO3 + HCl
2) CuCl2 + 2NaOH → 2NaCl + Cu(OH)2↓
3) Al2(SO4)3 + 6HCl → 2AlCl3 + 3H2SO4
4 2NaNO3 + H2SO4 → Na2SO4 + 2HNO3
16. Fe+HCl→....+.... Пропущенными веществами в схеме химической реакции являются:
1) H2 и FeCl2
2) FeCl2 и FeCl3
3) Cl2 и FeCl2
4) Cl2 и Fe2О3
17. Для цепочки превращений Zn→(HCl) Х1→(KOH) Х2→(t) Х3 конечным веществом Х3 является:
1) Zn (OH)2
2) ZnO
3) Zn
4) К2ZnO2
18. При взаимодействии NaOH с избытком оксида углерода (IV) образуется:
1) гидрокарбонат натрия
2) карбонат натрия
3) карбонат натрия и вода
4) гидрокарбонат натрия и вода
19. С кислотами и щелочами взаимодействует оксид:
1) калия
2) железа(II)
3) цинка(II)
4) углерода
20. Коэффициент перед молекулой восстановителя в уравнении реакции K2Cr2O7 + KI + H2SO4 → Cr2(SO4)3 + I2 + K2SO4 + H2O равен:
1) 8
2) 6
3) 4
4) 10
21. Ионная химическая связь имеется только в веществе
1) Н2O
2) CO
3) ZnCl2
4) NO
22. Уравнение реакции, практически осуществимой в водном растворе, имеет вид:
1)FeSO4 + 2HCl = H2SO4 + FeCl2
2)KCl + NaNO3 = KNO3 + NaCl
3)CaCl2 + 2HNO3 = Ca(NO3)2 + 2HCl
4)Pb(NO3)2 + 2KI = PbI2↓ + 2KNO3
23. Al2S3 + H2O →…+… Пропущенными веществами в схеме химической реакции являются…
1)Al(OH)3 + S
2) Al(OH)3 + H2S
3) H2S + Al
4) Al(HS)3 + H2
24. При взаимодействии избытка сероводорода с гидроксидом калия образуется…
1)сульфат калия
2) гидросульфат калия и вода
3)гидросульфид калия и вода
4)гидросульфит калия
25. Кислотным оксидом является:
1)оксид натрия
2)оксид меди(II)
3)оксид железа(II)
4) оксид фосфора(V)
26. 16) Коэффициент перед восстановителем в уравнении реакции КСIO3 + 6HCl → KCl + 3Cl2 + 6H2O
1) 1
2) 8
3) 6
4) 3
27. Реакция Me + H2O → MeOH + H2 характерна для:
1) Cr
2) Os
3) K
4) Ag
28. Невозможно протекание реакции:
1) Fe + HCl →
2) CuOHCl + HCl→
3) Na + H2O→
4) NaNO3 + H2SO4→
29. В реакции Na2O2+ H2O→ NaOH+Х веществом Х является:
1) Na2O
2) O2
3) H2O2
4) H2
30. Для схемы превращений Cu (+H2SO4)→ X1(t) → X2 (+H2) → X3 конечным веществом является:
1) Cu
2) CuO
3) Cu(NO3)2
4) O2
31. При спекании карбоната натрия с оксидом алюминия образуется;
1) Al
2) NaAlO2
3) Na2O
4) CO
32. С кислотами и щелочами взаимодействует:
1) Zn(OH)2
2) Ca(OH)2
3) Ba(OH)2
4) Fe(OH)3
33. В реакции CrCl3+Cl2+ KOH→ K2CrO4+ NaCl + H2O ион хрома;
1) окислитель
2) восстановитель
3) окислитель-восстановитель
4)радикал
34. Только сильные электролиты приведены в ряду:
1) NaOH H2S Ca(OH)2
2) KOH HCl HNO3
3) H2CO3 H2SiO3 Fe(OH)3
4) NaOH H3PO4 H2SO4
35. Уравнение реакции, протекающие до конца (необратимо) имеет вид:
1) AgNO3 + HCl → AgCl↓ + HNO3
2) BaCl2 + 2KOH → 2KC l+ Ba(OH)2
3) Fe2(SO4)3 + 6HNO3 → 2Fe(NO3)3 + 3H2SO4
4) KNO3 + HBr → KBr + HNO3
36. Сa3P2+ HCl →... Продуктами реакции в схеме являются:
1) PCl3 + CaCl2
2) CaCl2 + PH3
3) P + PH3
4) PH3 + H3PO4
37. В цепи превращений. Х2-это:
Алюминий → сульфат алюминия (+NaOH) → Х1(t) → Х2.
1) Al
2) Al2O3
3) NaAlO2
4) HAlO2
38. При взаимодействии 1 моля ортофосфорной кислоты с 2 молями гидроксида натрия образуется:
1) фосфат натрия
2) гидрофосфат натрия
3) дигидрофосфат натрия
4) оксид фосфора (V)
39. Реакция межмолекулярного окисления-восстановления:
1) Na2SO3→Na2SO4+Na2S
2) KMnO4+HCl→KCl+MnCl2+Cl2+H2O
3) KNO3→KNO2+O2
4) HNO2→HNO3+NO2+H2O
40. Какой из элементов имеет высшую степень окисления +7:
1) C
2) Mn
3) S
4) Au
41. Реакции Na2CO3 +2HCl = 2NaCl +CO2 +H2O соответствует сокращенное ионно-молекулярное уравнение:
1) CO3 2- +2H = СO2 +H2O
2) Na2CO3 + 2H = CO2 + H2O + 2Na
3) Na + Cl– = NaCl
4) CO3 2- + 2HCl = CO2 + H2O + 2Cl
42. В результате взаимодействия алюминия с избытком раствора NaOH продуктами являются:
1) Al(OH)3 и Na
2) Na и H2
3) Na[Al(OH)4] и H2
4) Na[Al(OH)4] и H2O
43. При взаимодействии хлора с горячим раствором KOH образуются:
1) KCl, KClO, H2O
2) KClO3, KClO4, H2O
3) KCI, KClO4, H2O
4) KCl, KClO3, H2O
44. Из перечисленных веществ амфотерными свойствами обладает:
1) Fe(OH)2
2) Na2O
3) Be(OH)2
4) Mn2O7
45. В реакции K2Cr2O7 + Na2SO3 + H2SO4 = Cr2(SO4)3 + Na2SO4 + K2SO4 + H2O восстановителем являются атомы:
1) Cr+6
2) S+6
3) S+4
4) Na+
46. Коэффициент перед молекулой восстановителя в уравнении реакции KMnO4 + Na2SO3 + H2SO4 → MnSO4 + Na2SO4 + K2SO4 + H2O равен:
1) 5
2) 2
3) 3
4) 1
47. Формула высшего оксида элемента, образующего водородное соединение ЭН4,имеет вид…
1)ЭО
2)ЭО3
3)ЭО2
4)ЭО4
48. Вещества, содержащие только ковалентные полярные химические связи, приведены в ряду…
1)PF5, Cl2O7, NH4Cl
2)F2, H2SO4, CH3COOH
3)H3PO4, BF3, CH3COONH4
4)NO2, SOCl2, P2O5
49. Уравнение реакции, практически осуществимой в водном растворе, имеет вид…
1)Ba(NO3)2 +2NaOH =2NaNO3 +Ba(OH)2
2)NaNO3 +HCl =NaCl + HNO3
3)CuSO4 +2KOH =K2SO4 +Cu(OH)2
4)Fe2(SO4)3 +6HNO3 =2Fe(NO3)3 +3H2SO4
50. Пропущенными веществами в схеме химической реакции LiH +H2O →… +….
являются:
1)Li2O и O2
2)O2 и Н2
3)LiOH и Н2
4)H2 и Li2O
51. Для цепочки превращений Fe + HCl2→ X1 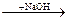 X2
X2 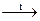 X3 конечным продуктом Х3 является….
X3 конечным продуктом Х3 является….
1)Fe(OH)2
2)Fe3O4
3) Fe2O3
4)Fe(OH)3
52. При взаимодействии оксида серы (IV) с избытком раствора NaOH образуется…
1)гидросульфит натрия
2)гидросульфат натрия
3)сульфит натрия и вода
4)сульфат натрия и вода
53. С кислотами и щелочами взаимодействует оксид…
1)хрома(III)
2)хрома(II)
3)хрома(VI)
4)магния
54. Коэффициент перед молекулой восстановителя в равнении реакции KMnO4 + Na2SO3 +H2SO4→MnSO4 +Na2SO4 +K2SO4 +H2O равен…
1)2
2)3
3)1
4)5
55. Для цепочки превращений Fe 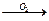 X1
X1 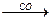 X2
X2 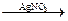 X3 конечным продуктом X3 является
X3 конечным продуктом X3 является
1)Fe2O3
2) Ag
3) H2O
4)Ag2O
56. Коэффициент перед молекулой восстановителя в уравнении реакции KMnO4 + KI + H2SO4 → MnSO4 + I2 + K2SO4 + H2O равен:
1) 6
2) 8
3) 10
4) 4
57. Приведенные схемы реакций
а) Na2ЭО4 + H2SO4 → Na2Э2О7 + Na2SO4 + H2O
б) Na2Э2О7 + H2SO4(конц) → ЭО3 + Na2SO4 + H2O
характерны для соединений элемента:
1)Fe
2)Cu
3)Cr
4)Zn
58. В водном растворе невозможна реакция:
1)KI + Cl2→
2)KI + F2 →
3)KBr + Cl2 →
4)KCl + Br2 →
59. В цепочке превращений Cu(NO3)2 → X → CuSO4 промежуточным веществом Х является:
1)Cu2O
2)CuNO3
3)CuO
4)CuCl
60. Водородное соединение элемента в оксиде Э2О7 имеет формулу:
1)Э2Н
2)Н2Э
3)НЭ
4)Н3Э5
61. Восстановителем в реакции Ag + HNO3 = AgNO3 + NO2 + H2O является:
1)N+5
2)H+
3)O2-
4)Ag
62. Восстановительные свойства SO2 проявляются в реакции:
1)+ H2S
2)+ KMnO4 + H2O
3)+ NaOH
4)+ H2O
63. Все вещества реагируют между собой в группе:
1)KOH, Ca(OH)2, Fe(OH)3
2)HCl, HBr, HI
3)SO3, CaO, Al2O3
4)BaO, MgO, CuO
64. Для получения сероводорода в лаборатории используется реакция:
1)FeS + HCl =
2)NaOH + S =
3)K2SO4 + H2 =
4)S + H2SO4 =
65. Для цепочки превращений Fe + Cl2 → X1 + NaOH → X2 + t° → X3 конечным веществом X3 является:
1)Fe2O3
2)Fe(OH)3
3)FeO
4)Fe(OH)2
66. Для цепочки превращений Fe + O2 + H2O → X1 + t° → X2 + Al t° → X3 конечным веществом X3 является:
1)Fe
2)Fe2O3
3)Fe3O4
4)FeO
67. Для цепочки превращений Cu + HNO3 → X1 + NaOH → X2 + t° → X3 конечным веществом X3 является:
1)[Cu(H2O)4]NO3
2)CuO
3)Cu2O
4)Cu(NO3)2
68. К числу наиболее вредных для организма человека относятся следующие металлы:
1)Co
2)Pb
3) Mn
4)Zn
69. Какая из перечисленных реакций приводит к образованию золя:
1)HCl + NaOH =
2)H2SO4 + K2S =
3)Cl2 + KOH =
4)AgNO3 + KI =
70. Наиболее сильной кислотой является:
1)HClO4
2)HClO3
3)HClO
4)HClO2
71. Образование осадка наблюдается при сливании растворов:
1)NaOH и H2SO4
2)K2CO3 и HNO3
3)CuSO4 и HNO3
4)CuSO4 и KOH
72. Окислителем в реакции
KMnO4 + KNO2 + H2SO4 = K2SO4 + MnSO4 + KNO3 + H2O является:
1)H2SO4
2)KNO2
3)MnSO4
4)KMnO4
73. Окислителем в реакции
KMnO4 + Na2SO3 + H2SO4 = K2SO4 + Na2SO4 + MnSO4 + H2O является:
1)KMnO4
2)Na2SO4
3)H2SO4
4)Na2SO4, H2SO4
74. Окислительные свойства оксида серы (IV) проявляются в реакции:
1)SO2 + O2 =
2)SO2 + KMnO4 + H2O =
3)SO2 + H2S =
4)SO2 + Ca(OH)2 =
75. Оксиды образуются при:
1)растворении хлора в воде
2)растворении негашеной извести
3)горении железа в хлоре
4)горении природного газа
76. При разложении нитрата серебра образуется:
1)Ag + N2O3 + O2
2)Ag2O + N2O5 + O2
3)Ag + NO2 + O2
4)Ag2O + N2O5
77. Пропущенным веществами в схеме химической реакции H2S +... = H2O + NaНS являются:
1)Na2S
2)S
3)NaOH
4)Na
78. Пропущенным веществом в схеме химической реакции
Al + HNO3 =... + NH4NO3 + H2O являются:
1)Al2O3
2)NO2
3)Al(NO3)3
4)NO
79. Пропущенным веществом в схеме химической реакции CaH2 + H2O = Ca(OH)2 +... являются:
1) CaO
2) H2
3) О3
4) O2
80. Пропущенным веществом в схеме химической реакции
Cl2 +... → KClO3 + KCl.+ H2O являются:
1) KСlO2
2)KOCl
3)KH
4)KOH
Date: 2015-05-22; view: 621; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |