
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт 3. Получение и коагуляция коллоидного раствора (золя) кремниевой кислоты
Коллоидный раствор возникает, если в гетерогенной системе имеются условия для образования особой частицы, называемой " мицелла". Центром мицеллы является ядро, представляющее собой ассоциат молекул нерастворимых веществ. В данном случае (см. схему 4.1) это молекулы метакремниевой (H2SiO3) и ортокремниевой (H4SiO4) кислот, образующихся в реакции, проходящей в водном растворе:
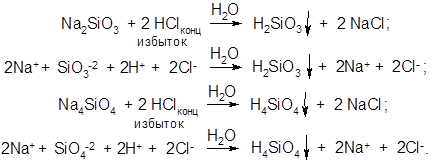
На поверхности ядра адсорбируются находящиеся в растворе в избытке частицы, которые в наибольшей степени подобны тем атомным группам, которые имеются в составе молекул, образующих ядро. В рассматриваемой реакционной системе это протоны в составе молекул HCl, выполняющие роль стабилизаторов коллоидной частицы (см. схему 4.1). В результате этой адсорбции происходит компенсация избыточной поверхностной энергии Gпов на границе раздела фаз в системе кремниевая кислота – водный раствор HCl. Ядро вместе с адсорбционным слоем протонов образует положительно заряженный агрегат. На поверхности агрегата адсорбируется часть противоионов (в рассматриваемом случае это анионы Cl-). При этом образуется гранула, имеющая тот же заряд, что и агрегат. Гранулы как раз и являются коллоидными частицами, которые в совокупности образуют дисперсную систему. Оставшиеся противоионы, не вошедшие в адсорбционный слой, гидратируются водой и распределяются по всему раствору, образуя диффузный слой. Гранула вместе с диффузным слоем образуется мицеллу, которая в целом электронейтральна.
Химическая формула мицеллы, образующейся в системе, изучаемой в данном опыте, имеет следующий вид (схема 4.1):
схема 4.1

В определенных условиях (нагревание, перемешивание, добавление других электролитов и др.) адсорбционные слои ионов на ядре частично или полностью разрушаются. В этом случае компенсация избыточной поверхностной энергии Gпов на границе раздела фаз происходит путем агрегации – слипания частиц дисперсной фазы (в проводимом опыте – частиц кремниевой кислоты). Этот процесс, приводящий к укрупнению частиц фазы без выпадения их в осадок, называется гелеобразованием (неполная коагуляция). При этом не происходит полного разрушения дисперсной системы.
Гелеобразование – процесс обратимый, и при соответствующих воздействиях на дисперсную гелеобразную систему гель можно опять превратить в коллоидный раствор (золь).
Если же укрупнение столь значительно, что под действием силы тяжести укрупненные частицы выпадают в осадок (т.е. осуществляется процесс седиментации), то происходит полное разрушение коллоидного раствора. В этом случае имеет место полная коагуляция с образованием осадка (коагулята).
Цель работы: получить представление об образовании коллоидного раствора кремниевой кислоты в воде при взаимодействии силиката натрия с избытком соляной кислоты и об условиях превращения этого золя в гель.
Используемые вещества: 37 %-ный раствор HCl, профильтро-ванный через стеклянный фильтр раствор силикатов натрия Na2SiO3 и Na4SiO4 (силикатного клея).
Посуда и принадлежности: пробирка на 20 см3, градуированная пипетка.
Методика проведения опыта. К 6 см3 37 %-ного раствора соляной кислоты медленно прилейте при интенсивном перемешивании стеклянной палочкой 1см3 раствора силикатного клея. Нагрейте раствор до кипения, а затем охладите. В наблюдениях отметьте, что происходило на всех стадиях опыта (при сливании, кипении, охлаждении).
В выводах:
– назовите и охарактеризуйте наблюдаемые вами физико-химические явления, объясните их причину;
– отметьте, почему и как происходит в данном опыте образование золя и гелеобразование;
– объясните, почему в присутствии большого избытка воды в отсутствие HCl нерастворимые кремниевые кислоты образуют коллоидные растворы. Изобразите формулу мицеллы, образующейся в этом случае, с учетом частиц, возникающих при диссоциации кремниевой кислоты:
H2SiO3  H+ + HSiO3- .
H+ + HSiO3- .
Объясните, почему в ряде случаев нерастворимые или малорастворимые вещества плохо образуют осадок и их трудно отделить от растворов, например, Al(OH)3, Zn(OH)2, Ca(OH)2 и др.
Тема № 5. Классы неорганических соединений, кислотно-основные свойства веществ, реакции обменного разложения в растворах электролитов и их использование в химическом анализе (с элементами УИРС) (базовый материал)
Date: 2015-05-08; view: 2706; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |