
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Приготовление растворов реагентов
Раствор серной кислоты (СМ = 0,2 М). При охлаждении и перемешивании осторожно растворяют 11 мл концентрированной серной кислоты в 500 мл дистиллированной воды в мерной колбе на 1 л и после охлаждения доводят объем раствора до 1 л дистиллированной водой.
Раствор А. Растворяют 26 г сульфата аммония в 100 мл 0,2 М раствора серной кислоты в конической колбе.
Раствор В. Растворяют 28 г нитрита натрия в 100 мл дистиллированной воды в конической колбе.
Посуда, принадлежности и оборудование: стеклянный стакан (примерно на 2 л), стеклянная палочка, мерный цилиндр или стакан на 1 л, мерный цилиндр на 100 мл, две конические колбы (250 мл), магнитная мешалка.
Методика проведения опыта. В стеклянный цилиндр налейте по 10 мл растворов А и В и быстро их перемешайте. Дальнейшее наблюдение за ходом реакции ведите при медленном перемешивании на магнитной мешалке. Отметьте начало выделения газа, затем оно прекращается. Отметьте начало нового газообразования (примерно через 8 с). Через минуту процесс выделения газа становится более энергичным и четким. Наблюдаемая колебательная реакция продолжается около 4 мин.
Напишите выражение скорости проведенной реакции по закону действия масс.
В выводе отразите, почему проведенная реакция является колебательной, и укажите характерные особенности таких реакций.
Тема 3. Химическое равновесие (базовый материал)
Рекомендуемая литература по теме 3 приведена на с. 24.
Химические реакции и физико-химические процессымогут быть необратимыми и обратимыми. Необратимые процессы протекают только в одном направлении и до конца, т.е. до полного расходования хотя бы одного из исходных веществ.
Реакции, которые могут одновременно проходить как в прямом, так и в обратном направлении, называются обратимыми. Обратимые реакции никогда не протекают до конца, т.к. ни одно из реагирующих веществ не расходуется полностью:
аА + вВ ⇄ cC + dD,
где A и B – исходные вещества; C и D – продукты прямой реакции; a, b, c и d – соответствующие стехиометрические коэффициенты.
Состояние химического равновесия устанавливается при равенстве скоростей прямой и обратной реакций: 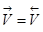 . В соответствии с законом действия масс получаем равенство:
. В соответствии с законом действия масс получаем равенство: 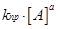 ·
· 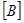
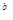 =
= 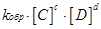 , откуда
, откуда
КР = 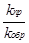 =
= 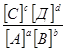 .
.
КР – константа равновесия, выражается через константы скоростей прямой и обратной реакций 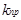 и
и 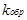 или через равновесные концентрации реагентов прямой ([A]а·[B]b) и обратной ([C]c·[D]d) реакций. В состоянии равновесия концентрации всех веществ в реакционной системе взаимосвязаны друг с другом, изменение концентрации любого из них вызывает изменение концентрации других. Поэтому соотношение этих концентраций, выражаемое константой равновесия, при данной темпера-туре остается постоянной величиной. Так, для системы: СО2(г) + 4Н2(г) ⇄ СН4(г) + 2Н2О(г) константа равновесия может быть выражена следующим образом:
или через равновесные концентрации реагентов прямой ([A]а·[B]b) и обратной ([C]c·[D]d) реакций. В состоянии равновесия концентрации всех веществ в реакционной системе взаимосвязаны друг с другом, изменение концентрации любого из них вызывает изменение концентрации других. Поэтому соотношение этих концентраций, выражаемое константой равновесия, при данной темпера-туре остается постоянной величиной. Так, для системы: СО2(г) + 4Н2(г) ⇄ СН4(г) + 2Н2О(г) константа равновесия может быть выражена следующим образом:
КР = 
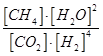 .
. 

Физический смысл константы равновесия определяется соотноше-нием констант скоростей прямой и обратной реакций 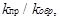 и показывает, во сколько раз скорость прямой реакции больше скорости обратной реакции при одинаковой концентрации всех веществ в системе, равной единице, и данной постоянной температуре. Величина константы равновесия зависит от природы реагирующих веществ и температуры, но не зависит от концентрации и присутствия катализаторов.
и показывает, во сколько раз скорость прямой реакции больше скорости обратной реакции при одинаковой концентрации всех веществ в системе, равной единице, и данной постоянной температуре. Величина константы равновесия зависит от природы реагирующих веществ и температуры, но не зависит от концентрации и присутствия катализаторов.
Смещением или сдвигом равновесия называется процесс изменения равновесных концентраций веществ, вызванный нарушением равновесия. Состояние химического равновесия может существовать сколь угодно долго, но нарушается при изменении концентраций реагирующих веществ и продуктов реакций, температуры и давления (последнее – только для газообразных веществ). Все эти параметры влияют на скорость реакции. Таким образом, чтобы нарушить состояние химического равновесия, необходимо изменить скорости прямой или обратной реакций и тем самым нарушить их равенство.
Для смещения равновесия и, как следствие, управления направленностью обратимого процесса может быть использован принцип подвижного равновесия  (принцип Ле Шателье): изменение одного из условий в равновесной системе (температуры, давления, концентрации) вызывает смещение химического равновесия в направлении того процесса, который противодействует произведенному изменению.
(принцип Ле Шателье): изменение одного из условий в равновесной системе (температуры, давления, концентрации) вызывает смещение химического равновесия в направлении того процесса, который противодействует произведенному изменению.
Так, в системе СН4(Г) + СО2(Г) ⇄ 2СО(Г) + 2Н2(Г), ΔΗ>0 равновесие смещается вправо, т.е. в направлении прямой реакции в следующих случаях:
– при повышении температуры, т.к. при этом равновесие должно смещаться в сторону эндотермического процесса;
– при увеличении концентрации метана и (или) оксида углерода (IV) или при уменьшении концентрации оксида углерода (II) и водорода, что вытекает из закона действия масс;
– при понижении давления в системе, поскольку количество газообразных молекул продуктов прямой реакции преобладает над количеством молекул исходных веществ.
В случае реакции, протекающей в растворе, процесс обратим, если хотя бы один реагент и один продукт реакции проявляют свойства слабого электролита. Например, в обратимой реакции гидролиза ацетата калия СН3СООК + Н2О ⇄ СН3СООН + КОН, ΔΗ>0 реагентами – слабыми электролитами являются: в прямой реакции – вода, в обратной реакции нейтрализации – уксусная кислота. При этом равновесие смещено в сторону образования более слабого электролита – воды, т.е. влево. Для смещения равновесия вправо следует увеличить концентрацию воды (разбавить раствор), уменьшить концентрацию КОН (путем добавления кислоты, связывающей образующиеся при гидролизе ионы ОН¯), повысить температуру (поскольку реакция гидролиза эндотермична). Изменением давления невозможно сместить равновесие в данной реакции, т.к. в ней не участвуют газообразные вещества.
Рекомендуемая литература: [1], гл. 6, 6.2.8; [2], гл. 5, § 5.5, гл. 6, § 6.1; [5], гл. V.
Лабораторная работа № 3.1 Смещение химического равновесия (с элементами УИРС)
Цель работы: изучение факторов, которые вызывают смещение химического равновесия и позволяют управлять направленностью обратимых процессов.
Опыт 1. Влияние концентрации веществ на смещение химического равновесия (УИРС)
При взаимодействии хлорида железа (III) с роданидом аммония протекает обратимая реакция с образованием слабого электролита – роданида железа (III), имеющего интенсивную кроваво-красную окраску:
FeCl3 + 3NH4SCN ⇄ Fe(SCN)3 + 3NH4Cl
красный
Поскольку остальные вещества неокрашенные (NH4SCN и NH4Cl) или слабоокрашенные (разбавленный раствор хлорида железа (Ш) имеет светло-желтую окраску), смещение равновесия легко наблюдать по изменению интенсивности красной окраски[1].
Реактивы: насыщенные растворы хлорида железа (III) и роданида аммония; кристаллические роданид аммония и хлорид аммония; дистиллированная вода.
Посуда и принадлежности: стандартные пробирки; два микрошпателя.
Методика проведения опыта. В пробирку добавьте по три капли растворов хлорида железа (III) и роданида аммония. Полученный темно-красный раствор разбавьте дистиллированной водой до светло-красной окраски. В этой системе установилось начальное состояние равновесия (пробирка №1, табл. 1.7).
Разделите полученный раствор на три пробирки. В одну пробирку (пробирка № 2) прибавьте 1-2 микрошпателя кристаллов роданида аммония, в другую (пробирка № 3) – 1-2 микрошпателя кристаллов хлорида аммония. Пробирку № 1 оставьте в качестве контроля для сравнения.
Сопоставьте интенсивность окрасок растворов во всех пробирках и отразите это в наблюдениях. На основании закона действующих масс напишите выражение для скорости прямой реакции, скорости обратной реакции и константы равновесия данной обратимой реакции.
Сделайте вывод о влиянии концентрации веществ на смещение химического равновесия и о причинах этого смещения. Объясните, почему изменение концентраций веществ влияет на скорость реакции.
Отметьте, сколько состояний равновесия Вы наблюдали. Определите, изменялась ли константа равновесия в ходе эксперимента или оставалась
постоянной и почему.
Результаты опыта занесите в таблицу 1.7.
Таблица 1.7 – Влияние концентрации веществ на смещение химического равновесия
| Номер пробирки | Добавленное вещество | Изменение интенсивности окраски | Направление смещения равновесия (вправо или влево) |
| контроль NH4SCN NH4Cl |
Date: 2015-05-08; view: 781; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |